Clear Sky Science · zh
在急性髓性白血病中,米多司他汀的应答受可被SMAC模拟物选择性靶向的祖细胞样细胞状态所塑造
为什么有些白血病药物会失效
对于许多患有一种称为急性髓性白血病(AML)的血液恶性肿瘤的人来说,新的靶向药带来了希望——但并非人人受益,且疗效常常会减弱。本研究提出了一个简单但关键的问题:为什么有些白血病细胞对一种广泛使用的药物米多司他汀无动于衷?我们能否找到一种明智的组合策略迫使这些顽固细胞死亡?
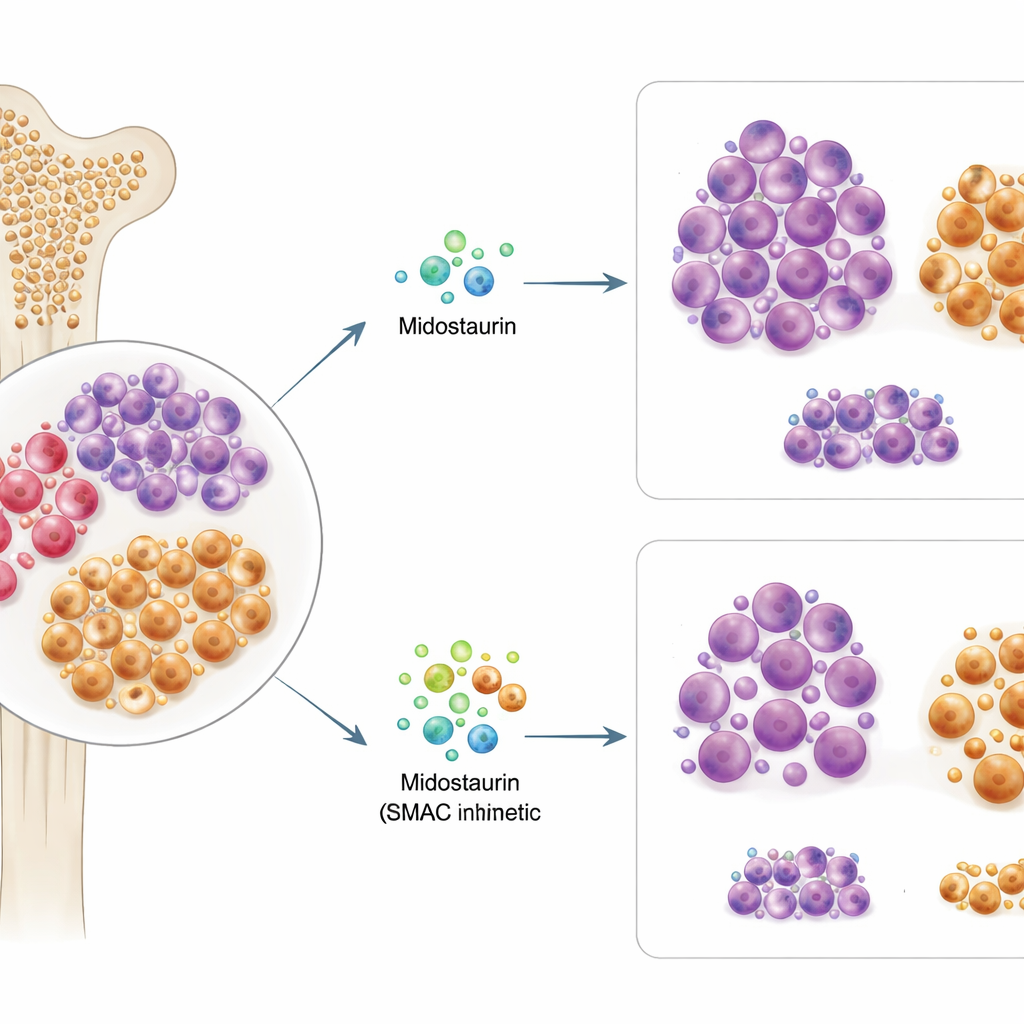
超越主要突变的视角
大约三分之一的AML患者携带称为FLT3的基因改变,该改变驱动白血病生长,也是开具米多司他汀的理由。研究者对来自63例FLT3突变AML患者的骨髓和血液样本进行了测试,将这些细胞在体外暴露于米多司他汀及500多种其他抗癌药物中。他们发现,患者细胞在体外对米多司他汀的敏感性,与该患者后来在临床上的反应高度一致。令人意外的是,FLT3突变的具体类型或其丰度并不能可靠预测米多司他汀的疗效,这表明仅靠遗传信息无法解释谁会受益。
隐匿的一小撮顽固“种子”细胞
深入分析时,团队比较了对米多司他汀敏感与不敏感细胞之间的整体蛋白和基因活动模式。不应答样本富含未成熟、干样祖细胞的特征——这些细胞更接近造血根源,被认为是能重新点燃白血病的“种子”。相反,应答样本更像部分成熟的免疫和髓系细胞。利用先进的单细胞方法,科学家们鉴定出一类由表面蛋白CD38和CD45RA标记的白血病细胞,表现出类似祖细胞的行为。这些细胞显示出异常的膜组织结构,暗示关键的信号分子以有利于存活的方式被重新排列。
生存接线:信号通路的转换
米多司他汀旨在阻断FLT3信号,该信号通常通过包括STAT5在内的一条信号链推动细胞生长。当团队在细胞系和患者样本中检测米多司他汀处理后的信号传导时,观察到两种不同模式。在对米多司他汀敏感的细胞中,STAT5活性迅速下降,与FLT3被有效抑制一致。然而在耐药细胞中,另一条通路占主导:PI3K/AKT,这是一条经典的生存通路,帮助细胞抵抗死亡。这些耐药细胞在治疗后维持甚至增加了AKT活性,并表现出更高水平阻止细胞凋亡的蛋白。换句话说,这些祖细胞样细胞内部的接线似乎被重路由,使其在FLT3被抑制时仍倾向于生存。
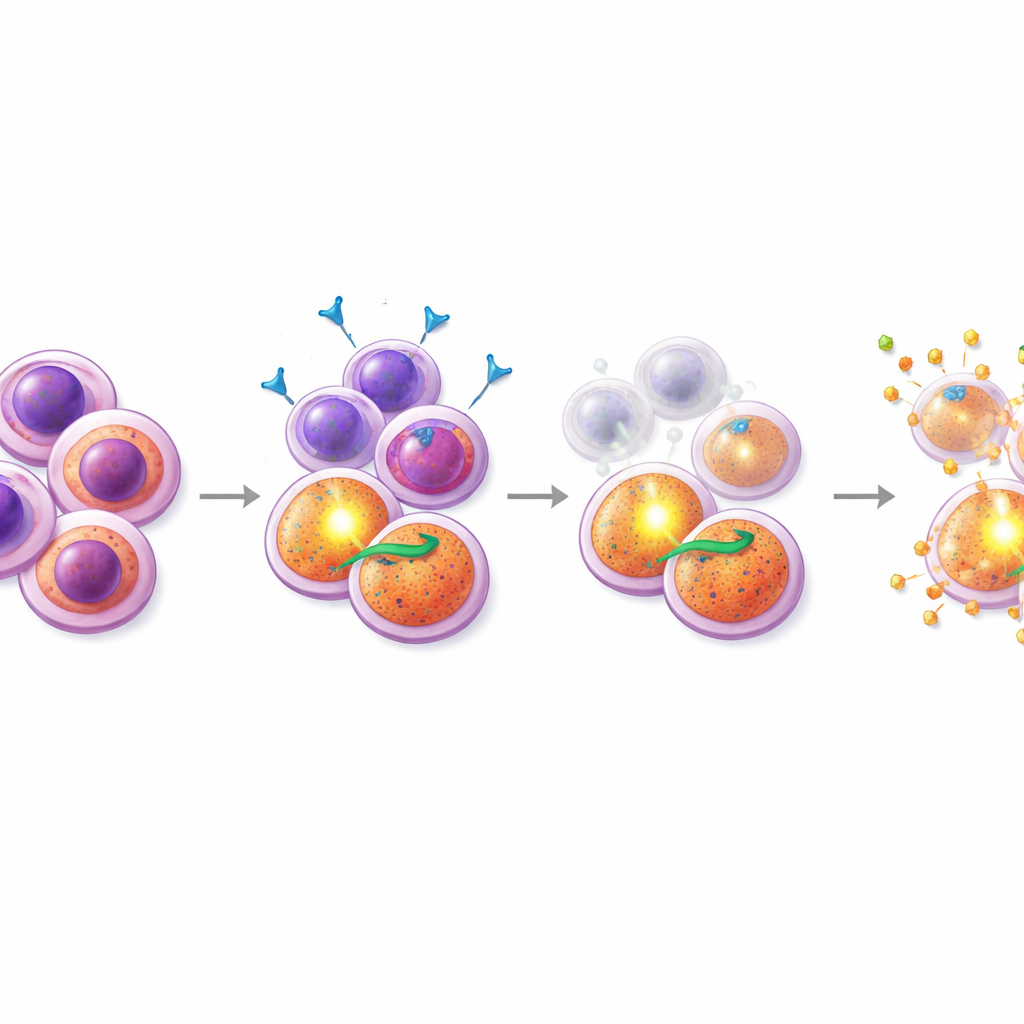
寻找打击薄弱环节的搭档药
有了这些见解,研究者筛查了米多司他汀与数百种其他化合物的组合,重点关注影响细胞死亡的药物。其中一类突出的是SMAC模拟物,这类药物可抑制PI3K/AKT驱动细胞所依赖的“凋亡抑制”蛋白。在耐药的患者样本和一株耐药的FLT3突变细胞系中,将SMAC模拟物(如birinapant)与米多司他汀联合使用产生了强烈的协同作用:联合用药比任何单药都杀死更多细胞。关键的是,详细的流式细胞术实验显示,米多司他汀—SMAC模拟物组合选择性地耗竭了CD38+CD45RA+祖细胞样群体并降低了其特征性表面标志水平,表明该疗法特别针对难以杀灭的“种子”。相比之下,与已获批的BCL‑2抑制剂venetoclax的组合对另一类CD34高表达的亚群更有效,但并未对耐药细胞表现出相同的针对性效应。
对患者意味着什么
这项工作表明,对米多司他汀的耐药性不仅与FLT3突变本身有关,还与白血病细胞的“状态”有关——包括其成熟度、膜组织以及偏好的生存通路。一个祖细胞样的CD38+CD45RA+亚群似乎是耐药的重要储备,它将信号从常见的STAT5路线转向有利生存的PI3K/AKT程序。通过将米多司他汀与SMAC模拟物配对,研究者能够在实验室中重新使这些细胞变得敏感并诱导其死亡。尽管仍需更大规模的临床研究,但这些发现指向一个未来:医生可能会使用功能性测试和细胞状态分型,而不仅是DNA测序,来选择针对FLT3的组合疗法,从而同时切除肿瘤主体及其最具抵抗力的“种子”。
引用: Struyf, N., Gezelius, H., Lundmark, A. et al. Midostaurin response in AML is shaped by a progenitor-like cell state selectively targeted by SMAC mimetics. npj Precis. Onc. 10, 117 (2026). https://doi.org/10.1038/s41698-026-01363-8
关键词: 急性髓性白血病, FLT3 抑制剂, 药物耐药, 白血病干细胞, SMAC 模拟物