Clear Sky Science · zh
COL3A1高表达的癌相关成纤维细胞协调代谢与免疫微环境,赋予乳腺癌化疗耐药性
为什么有些乳腺肿瘤对化疗无动于衷
化疗能挽救乳腺癌患者的生命,但许多病人会发现肿瘤对治疗逐渐失去反应,或从一开始就反应不佳。本研究不只关注癌细胞自身,而是考察它们所处的“邻里”——哪些周边细胞帮助肿瘤在治疗中存活,以及它们如何做到这一点?答案集中在一类特殊的支持细胞上:它们重塑肿瘤的营养供应和局部免疫,从而保护癌细胞免受化疗伤害。
肿瘤周围的隐形帮手
乳腺肿瘤不仅仅由癌细胞组成;它们是由血管、免疫细胞和称为成纤维细胞的结缔组织细胞组成的混合群落。当成纤维细胞出现在肿瘤中时,被称为癌相关成纤维细胞(CAFs),它们可以抑制或促进癌症发展。研究者将来自患者样本的多种强大基因组学分析——单细胞、空间和总体(bulk)分析——与体外和动物实验相结合,锁定了一类高表达COL3A1的CAF亚群。肿瘤中含有更多这类COL3A1高表达CAF的患者,更可能对化疗反应差且生存更差。
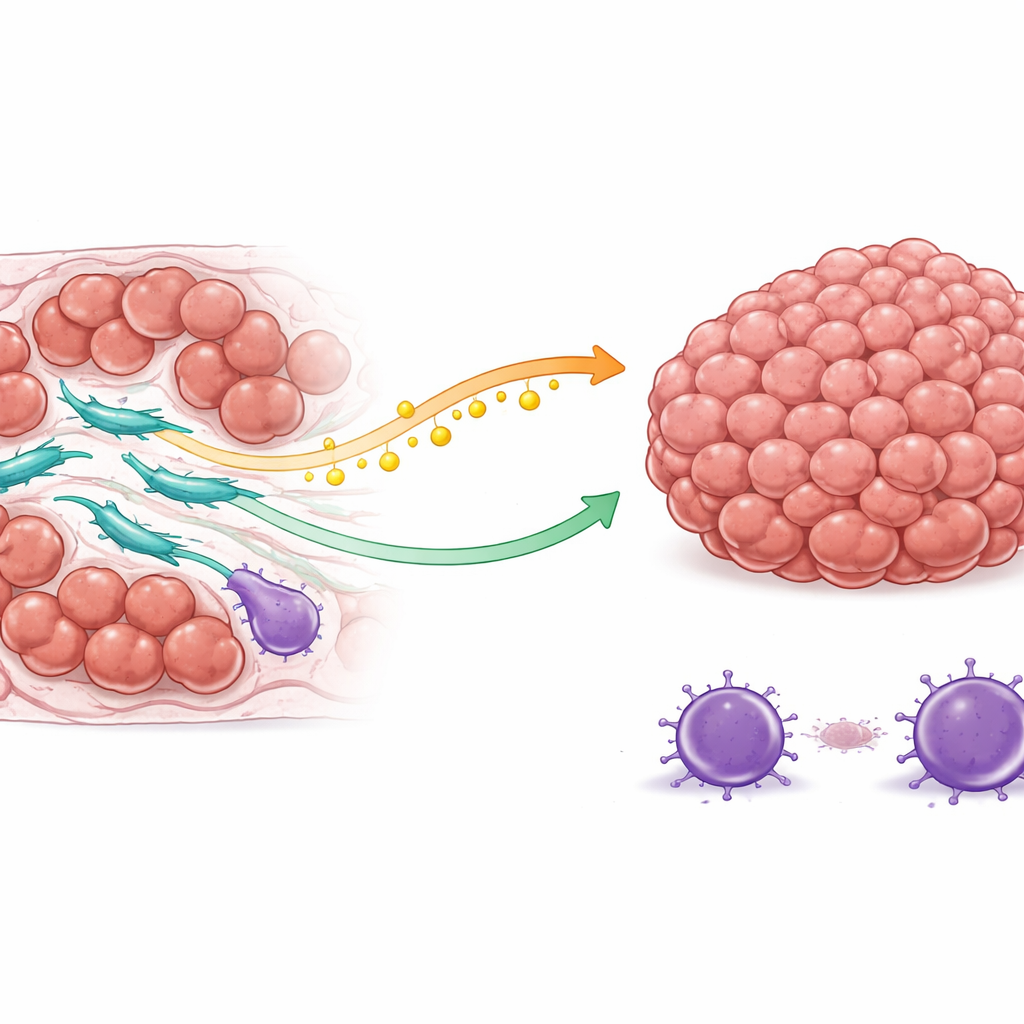
双重防护:燃料与屏障
研究团队发现,COL3A1高表达的CAF通过两条主要路径保护癌细胞。首先,它们改变脂质代谢。这些成纤维细胞提高了一种合成油酸的酶的活性(一种脂肪酸),并将生成的油酸释放到肿瘤微环境中。癌细胞通过表面蛋白摄取这些油酸,随后启动一条已知可帮助细胞抵抗死亡信号的内部生存通路。因此,当化疗试图触发癌细胞的自毁程序时,这些细胞更有能力抵抗并持续分裂。
塑造不利于免疫的微环境
第二,COL3A1高表达的CAF重塑局部免疫格局,有利于肿瘤生长。通过复杂的信号互作,它们吸引调节性T细胞——一种能抑制免疫攻击的免疫细胞,同时抑制或削弱本应攻击癌细胞的杀伤性T细胞。对真实患者肿瘤的空间定位显示,这些成纤维细胞常位于耐药癌细胞和免疫抑制性细胞附近,而有效的杀伤性T细胞则被推得较远。这样的排列形成了一个受保护的区域,使癌细胞在面对更少免疫威胁的同时,也变得更难被药物杀死。
来自细胞、鼠与患者的证据
为验证因果关系,研究者在体外将CAF的COL3A1下调。当乳腺癌细胞与这些改变后的成纤维细胞共培养时,癌细胞形成的侵袭性结构减少,对化疗药物紫杉醇更易敏感,并表现出更多程序性细胞死亡的迹象。在将乳腺癌细胞与CAF共同植入小鼠的模型中,阻断CAF中的COL3A1在化疗下减缓了肿瘤生长,并降低了脂肪合成酶和与油酸相关的癌细胞受体的水平。在72例接受术前化疗的患者队列中,COL3A1及其脂质代谢相关通路的高表达与较差的治疗反应和更短的无复发生存期密切相关。
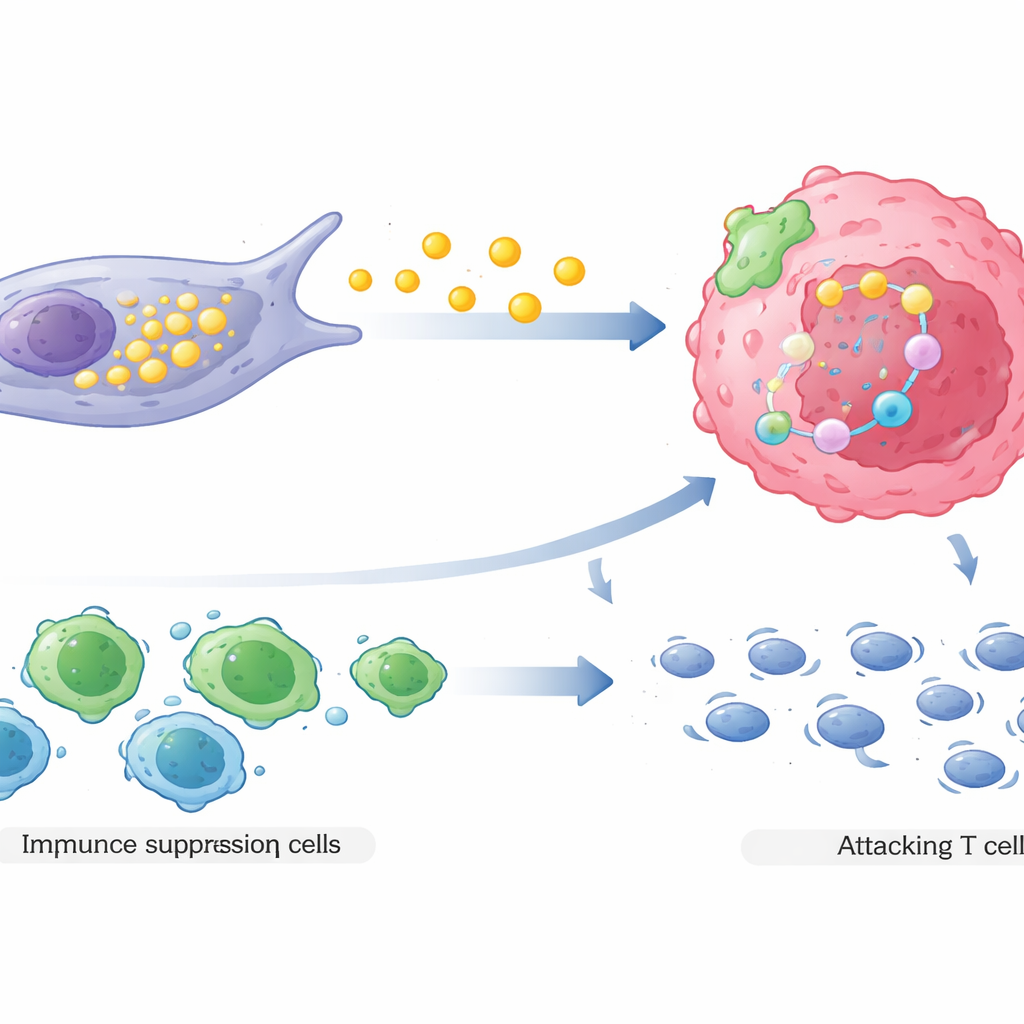
对未来治疗的意义
简而言之,该研究表明乳腺肿瘤中的一类特定支持细胞像保镖小队:它们为癌细胞提供一种基于脂肪的保护性“饮食”,并招募免疫盟友来削弱机体防御。这些联合作用使化疗效果下降。测量COL3A1高表达成纤维细胞的丰度可以提高医生预测患者是否对治疗有反应的能力,而它们所利用的通路——脂肪生成、癌细胞内的生存信号和免疫抑制——则提供了新的药物靶点。未来,将使这些成纤维细胞失能或重新编程的疗法与常规化疗联合,可能阻止肿瘤产生耐药性。
引用: Jiang, P., Li, X., Wang, Z. et al. COL3A1high cancer-associated fibroblasts orchestrate metabolic and immune microenvironments to confer chemoresistance in breast cancer. npj Precis. Onc. 10, 139 (2026). https://doi.org/10.1038/s41698-026-01338-9
关键词: 乳腺癌, 化疗耐药, 肿瘤微环境, 癌相关成纤维细胞, 脂质代谢