Clear Sky Science · zh
使用基于计算机断层扫描的基础模型预测同源重组缺陷及其治疗响应:一项前临床研究
这对患者和医生为何重要
那些损伤DNA的癌症治疗手段,例如某些化疗药物和新型靶向药物,在修复机制本就有缺陷的肿瘤中往往效果显著。问题在于如何在不依赖反复、侵入性活检的情况下识别出哪些肿瘤具有这些隐蔽弱点。本研究探索是否可以通过对小鼠进行常规医学风格的扫描,并由强大的人工智能模型来解读,进而揭示肿瘤的脆弱程度以及其对一种新型实验性药物的反应。
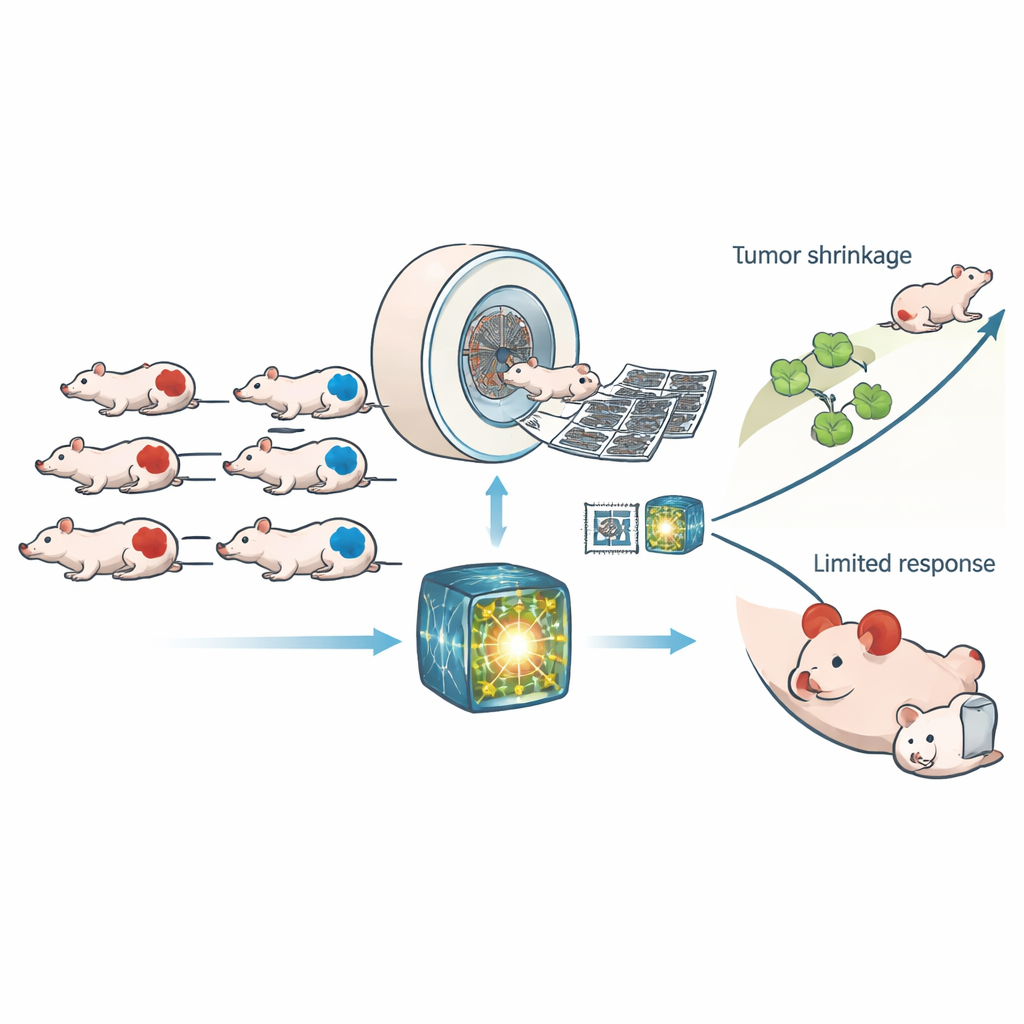
癌细胞的一个隐性弱点
许多肿瘤在一种关键的DNA修复通路——同源重组(homologous recombination)中存在缺陷。当该通路失效时,细胞在基因物质中积累损伤,这种状态称为同源重组缺陷(HRD)。HRD虽可增加癌症形成的风险,但也成为了阿喀琉斯之踵:进一步损伤DNA的药物能将这些已受压的细胞推向崩溃,从而比对健康细胞更有效地杀死肿瘤细胞。当前识别HRD通常依赖遗传检测或专门的实验室分析,既昂贵又耗时,且常需取肿瘤组织。作者们提出是否可以用影像——同门诊广泛使用的三维X线扫描——提供一种快速、无创的HRD观察窗口。
用智能扫描替代更多活检
研究人员使用了307只移植有人类肿瘤的老鼠,这些肿瘤在修复能力上要么为HRD状态,要么为正常。所有动物在接受对照处理或CP‑506(一种在肿瘤低氧区活化并能造成DNA交联的实验药物)前后,都进行了高分辨率计算机断层扫描(CT)。研究团队没有依赖少数人工设计的图像测量指标,而是采用了在大规模人类CT数据集上训练得到的现代“基础模型”,从每次扫描中提取数千种微妙模式。随后用这些模式训练了一个简单的分类器来判定肿瘤是否为HRD,并复用相同的学习到的特征来预测CP‑506会造成多少DNA损伤以及生长延迟。
影像模型的表现如何
该基础模型明显优于传统影像组学和从零开始训练的标准深度学习网络。在新的测试扫描上,它以约0.88的曲线下面积(AUC)区分出HRD与非HRD肿瘤,这一准确度在不同CT能量设置下均能保持。当两种AI方法在肿瘤类型上达成一致时,表现进一步提高。模型基于影像的HRD评分在若干前列腺与结直肠肿瘤系中与真实遗传状态高度一致,尽管一系因修复行为异常仍较难分类。更重要的是,与HRD相关的CT特征并非仅是统计学上的假象:它们还能预测CP‑506在治疗48小时后造成的持久DNA损伤程度,以及在平行实验中肿瘤再次生长到原来四倍大小所需的时间。
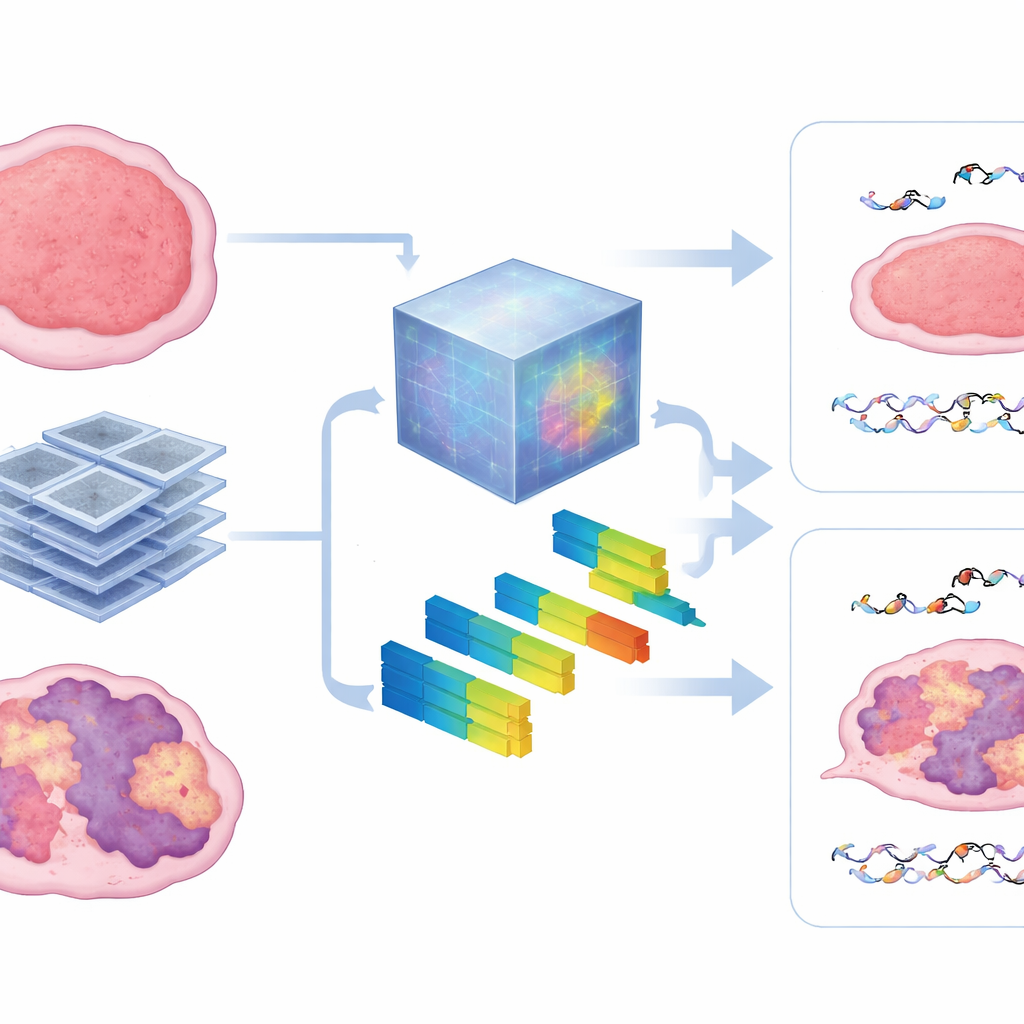
扫描所揭示的肿瘤内部信息
为了解开黑匣子,作者将基础模型学到的模式与描述图像纹理与强度的标准影像组学特征进行了比较。他们发现模型主要依赖于异质性度量——即肿瘤在CT上看起来多么斑驳、粗糙或不规则。具有更强HRD特征的肿瘤往往表现出更紊乱的纹理,而这些相同的特征也有助于预测微观层面的DNA损伤及宏观层面的肿瘤控制。当训练数据较少时,该方法仍保持稳健,这表明此类预训练模型能够克服动物研究中一个主要障碍:收集大规模影像数据集的困难。
从小鼠实验到未来的患者护理
这项前临床工作表明,利用强大、预训练的人工智能解读单次CT扫描即可捕捉到DNA修复缺陷的信号,并预测肿瘤对损伤DNA药物的敏感程度。对非专业读者而言,结论是常规外观的扫描可能很快就能兼顾两重功能——定位肿瘤并揭示其脆弱性——而无需额外程序。在成为常规护理的一部分之前,该方法必须在人类患者中接受测试与验证。如果这些努力成功,基于CT的HRD人工智能指纹有望帮助医生更精确地将患者与CP‑506及相关疗法匹配,既改善疗效,又避免让其他患者接受无效且有毒的药物。
引用: Kuang, S., Schuitmaker, L., Wu, M. et al. Predicting homologous recombination deficiency and treatment responses using a computed tomography-based foundation model: a preclinical study. npj Precis. Onc. 10, 121 (2026). https://doi.org/10.1038/s41698-026-01322-3
关键词: 同源重组缺陷, 癌症影像, 影像组学, 基础模型, 损伤DNA的治疗