Clear Sky Science · zh
用于诊断良性、交界性和恶性附件肿块的人工智能模型的开发与验证
这对女性健康为何重要
卵巢及其他附件肿块在盆腔超声中常见,但判断哪些是无害、哪些提示早期癌症仍然很困难,哪怕对专家而言亦然。本研究报告了一种新的人工智能(AI)系统,称为 Clinical‑OMTA,它读取超声图像并帮助医生将这些肿块分为三类——良性、交界性和恶性——以便让患者获得恰当的治疗,同时避免不必要的手术。
三类生长,三种截然不同的选择
并非所有附件肿块都相同。良性病变通常可以观察随访或通过简单手术切除。恶性肿瘤为危及生命的癌症,需要专科手术和化疗。交界性肿瘤处于两者之间:虽可复发,但常见于希望保留生育能力的年轻女性,外科医生因此尽量仅切除必要的组织。不幸的是,这三类在超声上可能非常相似。尤其是交界性肿瘤,既可伪装成无害的囊肿,也可与侵袭性癌症相似,使患者和临床医生在治疗决策上倍感压力。
把复杂的影像转换为更清晰的答案
超声通常是检测附件肿块时首先且最广泛可得的检查,但解读这些噪点多、差异大的图像需要丰富经验。现有评分系统和风险计算器(如广泛使用的 ADNEX 模型)将特定超声特征与年龄和血液标志物(CA125)等简单临床信息结合,然而它们仍依赖人工观察者正确描述影像。深度学习——AI 的一个分支,直接从像素中学习模式——的最新工作提供了机会,通过训练计算机识别不同肿瘤类型的细微影像特征,以减少这部分主观性。
跨多家医院训练的 AI 助手
在先前工作的基础上,作者设计了 Clinical‑OMTA,一种双路径 AI 模型:先将良性与非良性肿块区分开,然后再在交界性和恶性之间进行鉴别。该系统处理灰阶超声图像,并可选择接受年龄和 CA125 值作为输入。为训练和测试模型,团队汇集了大规模且多样化的数据集:来自中国 23 家医院的 2381 名女性,使用 38 种超声设备扫描。大多数病例由手术病理结果确诊;一小部分明显良性的囊肿通过至少六个月的超声随访确认。数据被划分为训练集、内部测试集和两个完全独立的外部测试队列,包含静态图像和卵巢短视频扫描。 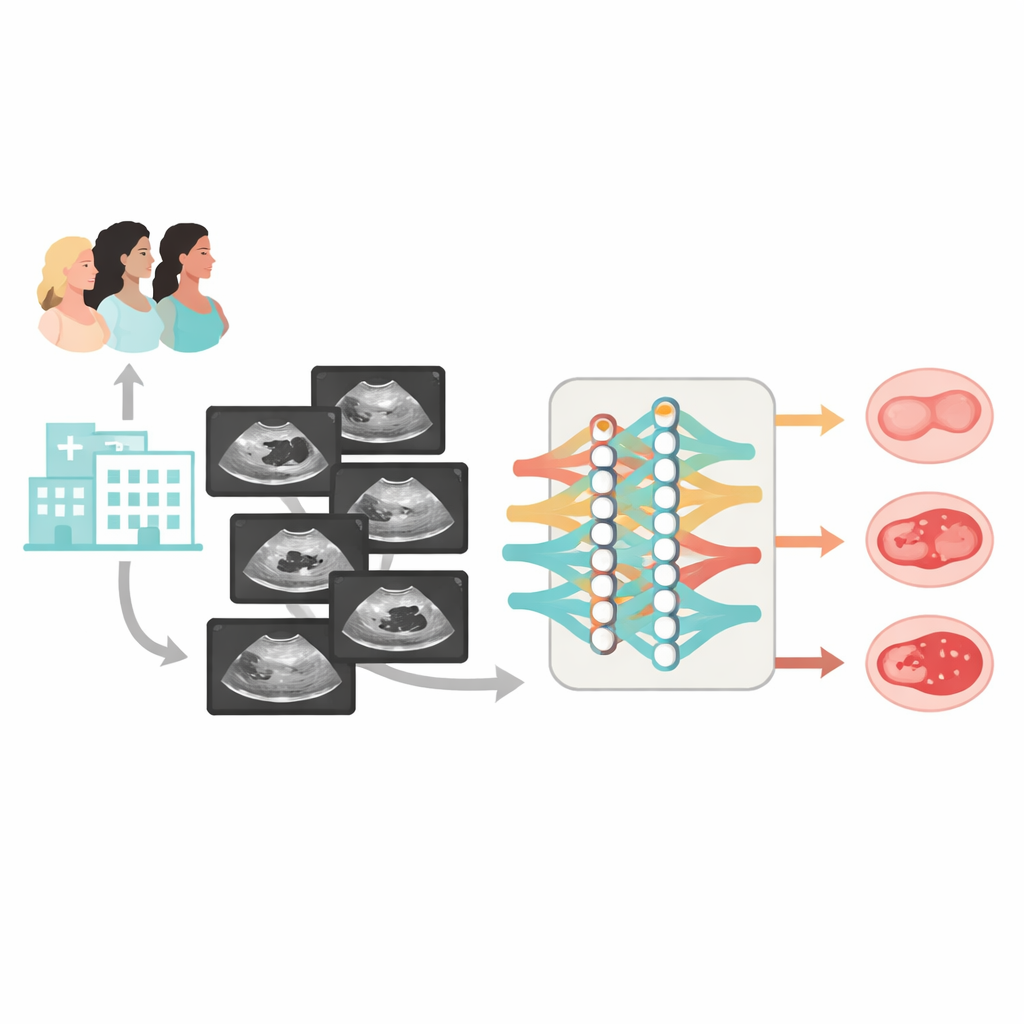
AI 在真实世界设置中的表现
在外部测试图像上,Clinical‑OMTA 将良性、交界性和恶性肿块正确区分的准确率与 ADNEX 模型和一位超声专家的判断相当。其在不同超声品牌、扫描方式(经腹或经阴道)以及两个外部医院之间的表现稳定,表明该模型并未过度依赖某一特定设备或中心。该系统在视频片段上也表现良好,而不仅限于静态帧。有趣的是,输入年龄和 CA125 并未比仅使用超声图像提高决策性能,这与早期研究一致:当有高质量影像时,该血液标志物的补充作用有限。 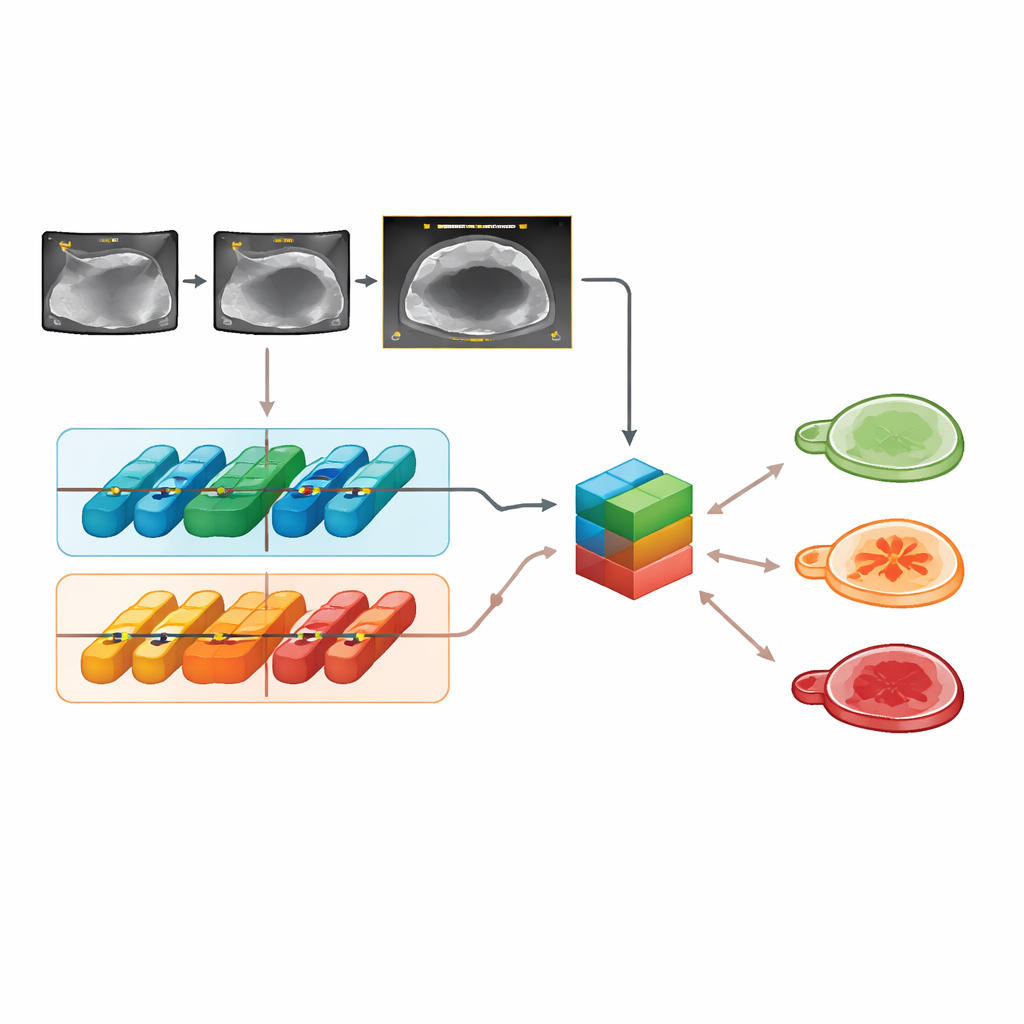
帮助经验不足的医生,但也有局限
研究者随后邀请了 11 位放射科医师——初级、中级和资深——对相同病例进行分类,先不借助 AI,然后在得到 AI 输出和强调模型认为重要区域的热图叠加后再次判断。在 Clinical‑OMTA 的帮助下,初级医生的准确率提高了约 18–20 个百分点,中级读片者也显著进步,达到了接近专家的表现。读者间的一致性(此前仅为公平到中等)在使用该工具后上升到很高水平。与此同时,研究指出这种强一致性可能反映“自动化偏差”,即临床医生在最模糊的交界性病例中过于依赖 AI。因此作者强调热图是研究工具,而非独立的解释手段,AI 指导必须谨慎地融入临床培训和决策流程。
对患者意味着什么
总体而言,Clinical‑OMTA 显示出在多样化超声数据上训练的 AI 系统,能够在将附件肿块分类为良性、交界性和恶性方面达到与专家相当的性能,同时显著提升经验较少的放射科医师的技能和一致性。由于它能在不同设备和中心间工作,模型最终可嵌入扫描仪或作为独立软件用于繁忙或资源不足的门诊中支持医生。作者警告,在常规使用之前仍需进一步的前瞻性和国际化研究,尤其是在低端设备或非专科操作人员的环境中。不过,他们的工作指向了这样一个未来:更多女性无论在何处接受治疗,都能受益于接近专家水平的卵巢超声判读,从而获得更个体化、及时的护理。
引用: Wu, Y., Dai, W., Li, X. et al. Development and validation of an artificial intelligence-based model for diagnosing benign, borderline, and malignant adnexal masses. npj Precis. Onc. 10, 106 (2026). https://doi.org/10.1038/s41698-026-01320-5
关键词: 卵巢超声, 人工智能, 附件肿块, 交界性卵巢肿瘤, 临床决策支持