Clear Sky Science · zh
Y 染色体相关 EIF1AY 缺失驱动多发性骨髓瘤的性别差异
为何某些血液肿瘤对男性打击更重
多发性骨髓瘤是一种发生在骨髓中产生抗体细胞的癌症。全球范围内,男性患病率和因病死亡率均高于女性,但其原因一直不明。本研究深入探讨了一个意想不到的嫌疑人:Y 染色体。研究者揭示了失去位于 Y 染色体上的单个基因 EIF1AY,如何促使男性的免疫微环境偏向支持肿瘤生长,指出了一个可能的精确治疗新靶点。
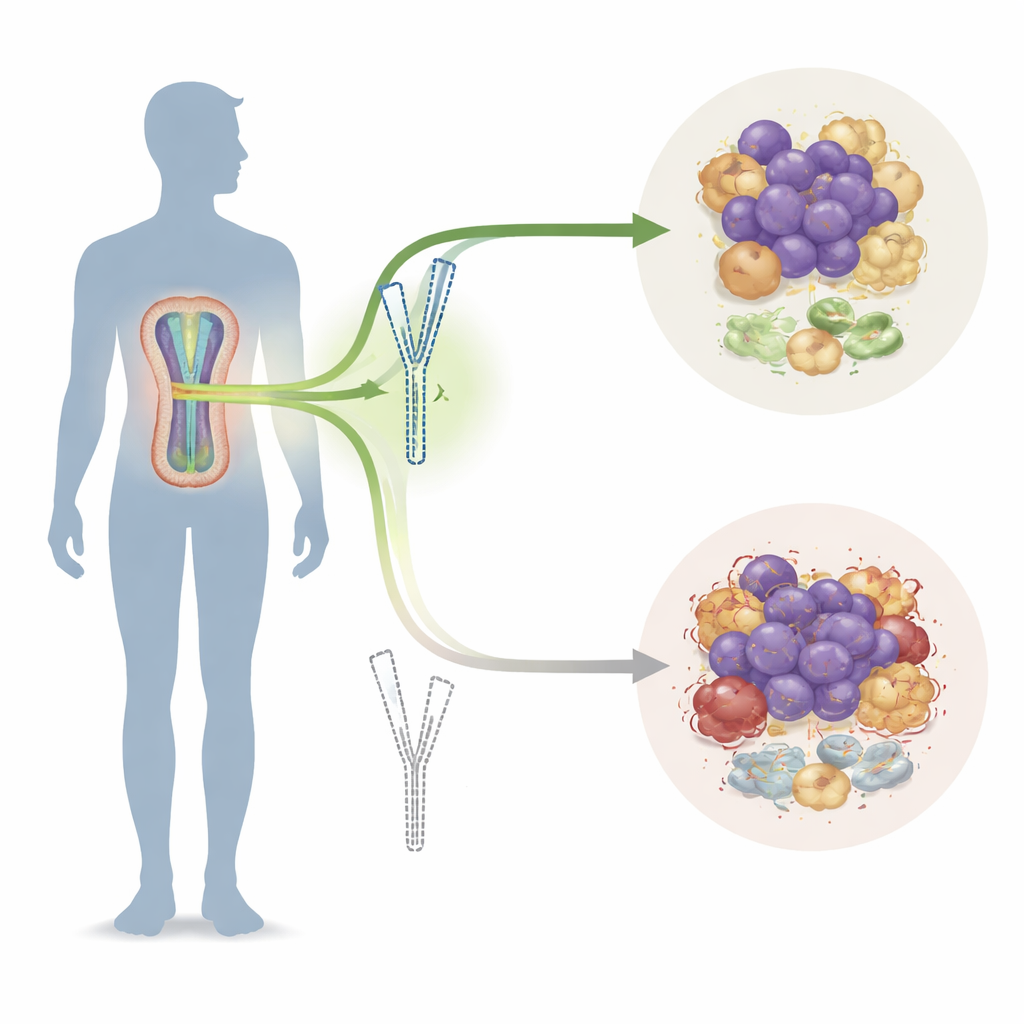
肿瘤 DNA 中隐藏的性别线索
研究者首先确认,多发性骨髓瘤的男性患者总体预后比女性更差,表现为发病率更高、确诊时病情更晚期以及生存期更短。随后他们扫描了大型基因和临床数据库,寻找在男女患者之间差异显著的基因。在众多候选基因中,有三个 Y 染色体基因在侵袭性疾病的男性中表达较低,且 EIF1AY 成为预测不良结局的最强指标。在男性患者的血液和骨髓样本中,EIF1AY 常常部分从 Y 染色体上缺失,尤其见于年长者以及晚期或染色体异常复杂的骨髓瘤患者。EIF1AY 水平较低的患者表现出更高的肿瘤负荷和对治疗的较差反应,表明该基因是一个关键的保护因子,但有些肿瘤会设法丢失它。
免疫细胞如何被转变为癌症的帮凶
团队接着探究 EIF1AY 如何影响肿瘤周围环境,尤其是巨噬细胞——一种既可以攻击癌细胞(“M1”状态),又可以支持癌症(“M2”状态)的免疫细胞。患者数据分析显示,男性骨髓瘤样本中 M2 样巨噬细胞比例高于女性样本。在体外与小鼠模型中,工程化表达更多 EIF1AY 的骨髓瘤细胞在培养皿和小鼠体内的生长更慢。其周围的巨噬细胞不太可能采用支持肿瘤的 M2 程序,也不易被招募进肿瘤。当 EIF1AY 水平降低或丢失时,情况恰好相反:更多 M2 极化的巨噬细胞聚集在肿瘤边缘和肿瘤内部,而这些经条件化的巨噬细胞反过来释放促使骨髓瘤细胞增殖的因子。本质上,EIF1AY 抑制了一种癌细胞与巨噬细胞之间的恶性合作关系。
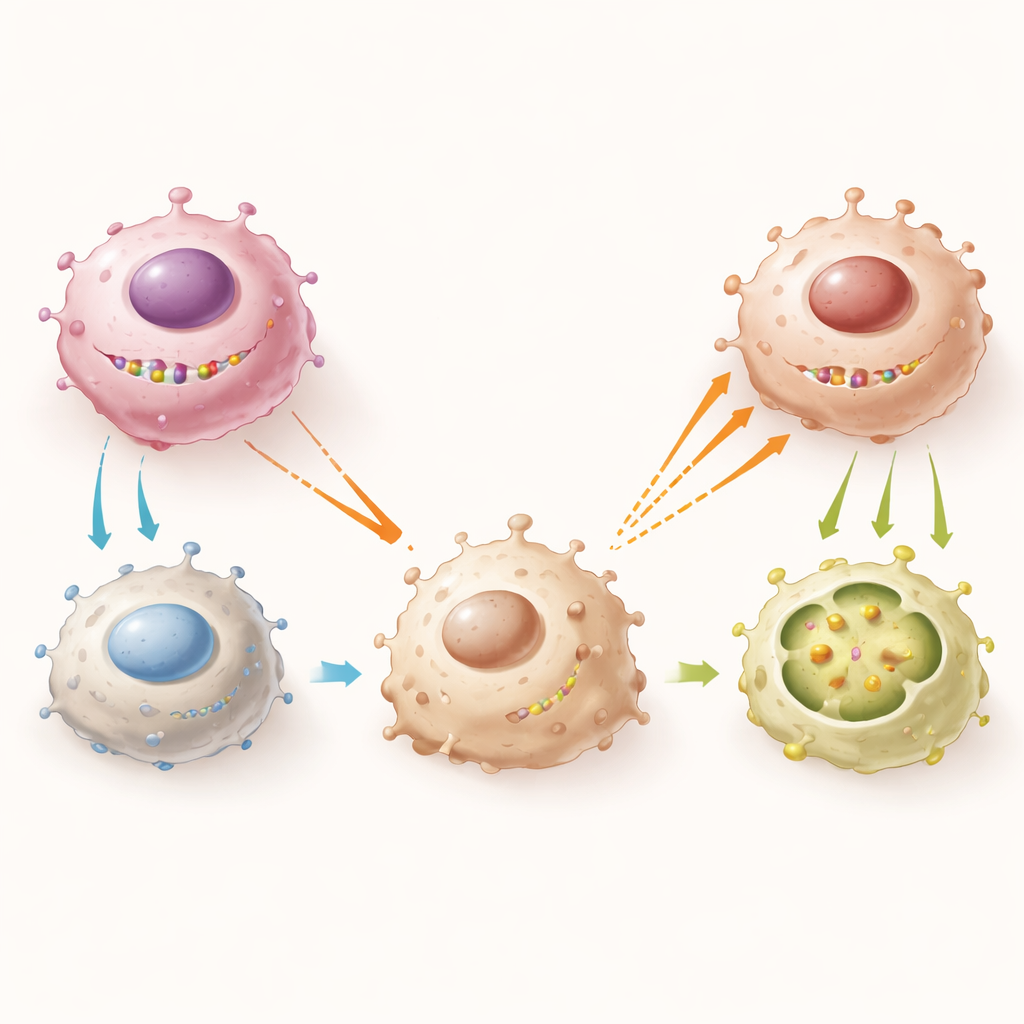
从肿瘤细胞到巨噬细胞的分子连锁反应
深入研究中,作者描绘了一条将肿瘤细胞内的 Y 染色体基因与邻近免疫细胞行为相连的分子链。EIF1AY 与另一个 Y 链蛋白 RPS4Y1 配合,形成一个复合体,该复合体物理结合并稳定骨髓瘤细胞表面受体 CD134 的信使 RNA。当 EIF1AY 与 RPS4Y1 存在时,CD134 水平维持在较高水平。反过来,这抑制了肿瘤细胞大量释放两种信号蛋白 IL‑4 和 IL‑13。IL‑4 和 IL‑13 水平较低时,巨噬细胞对胶原感受受体 DDR1 的表达减少,不太可能转变为 M2 样,也不易被吸引进肿瘤。当 EIF1AY 被删除时,这整个轴线崩溃:CD134 水平下降,IL‑4 和 IL‑13 上升,巨噬细胞上 DDR1 增加,更多 M2 型巨噬细胞涌入以滋养癌细胞。
连接男女版本的同一保护机制
有趣的是,女性不携带 EIF1AY 或 RPS4Y1,但她们在 X 染色体上拥有高度相关的基因 EIF1AX 和 RPS4X。研究发现,女性骨髓瘤患者中这些 X 链对应基因的高表达也与更好的结局相关。当研究者在来源于女性的骨髓瘤细胞系中实验性降低 EIF1AX 或 RPS4X 时,细胞生长加快,类似于男性在丢失 EIF1AY 和 RPS4Y1 时的情形。这提示两性都具备相似的保护通路,但男性更易受损,因为随年龄增长血细胞中可能发生部分 Y 染色体丢失,导致 EIF1AY 和 RPS4Y1 完全丧失,而女性的 X 链基因则更为稳定地维持。
对患者和未来治疗的意义
简而言之,这项工作表明,许多男性骨髓瘤患者丧失了一条保护性回路,该回路通常抑制肿瘤细胞的激活并阻止周围巨噬细胞转变为癌症同谋。当 EIF1AY–RPS4Y1–CD134 通路完整时,它能抑制特定免疫信号、阻止巨噬细胞获得有利于肿瘤的表型并减缓骨髓瘤生长。而当 Y 染色体的部分片段,尤其是 EIF1AY 被删除时,这种刹车被解除,导致炎性信号与支持性巨噬细胞之间的自我增强回路加速疾病进展。这些发现有助于解释为何男性在多发性骨髓瘤中预后较差,并提示检测 EIF1AY 状态或恢复其下游通路,可能为男性患者提供更有针对性的免疫治疗策略。
引用: Feng, Z., Bai, J., Li, Y. et al. Y chromosome-linked EIF1AY deletion drives sex differences in multiple myeloma. npj Precis. Onc. 10, 131 (2026). https://doi.org/10.1038/s41698-026-01317-0
关键词: 多发性骨髓瘤, Y 染色体, 肿瘤微环境, 巨噬细胞极化, 癌症中的性别差异