Clear Sky Science · zh
使用放射基因组学见解和预后相关性,通过非侵入性方法预测局限性透明细胞肾细胞癌的隐匿性 pT3a 升期
这对肾脏肿瘤患者为何重要
当医生发现肾脏肿瘤时,需要在仅切除肿瘤及其邻近组织与切除整个肾脏之间做出选择。这个决定取决于癌症实际扩散的程度。问题在于,影像检查有时会漏检早期的、隐藏在肾脏外的侵袭,因此术前看起来较轻的肿瘤术后可能被证实更危险。本研究引入了一种名为 RENALNet 的新型人工智能(AI)工具,它利用常规 CT 扫描更准确地识别这些隐匿的高风险肿瘤,旨在为更安全的手术和随访提供依据。
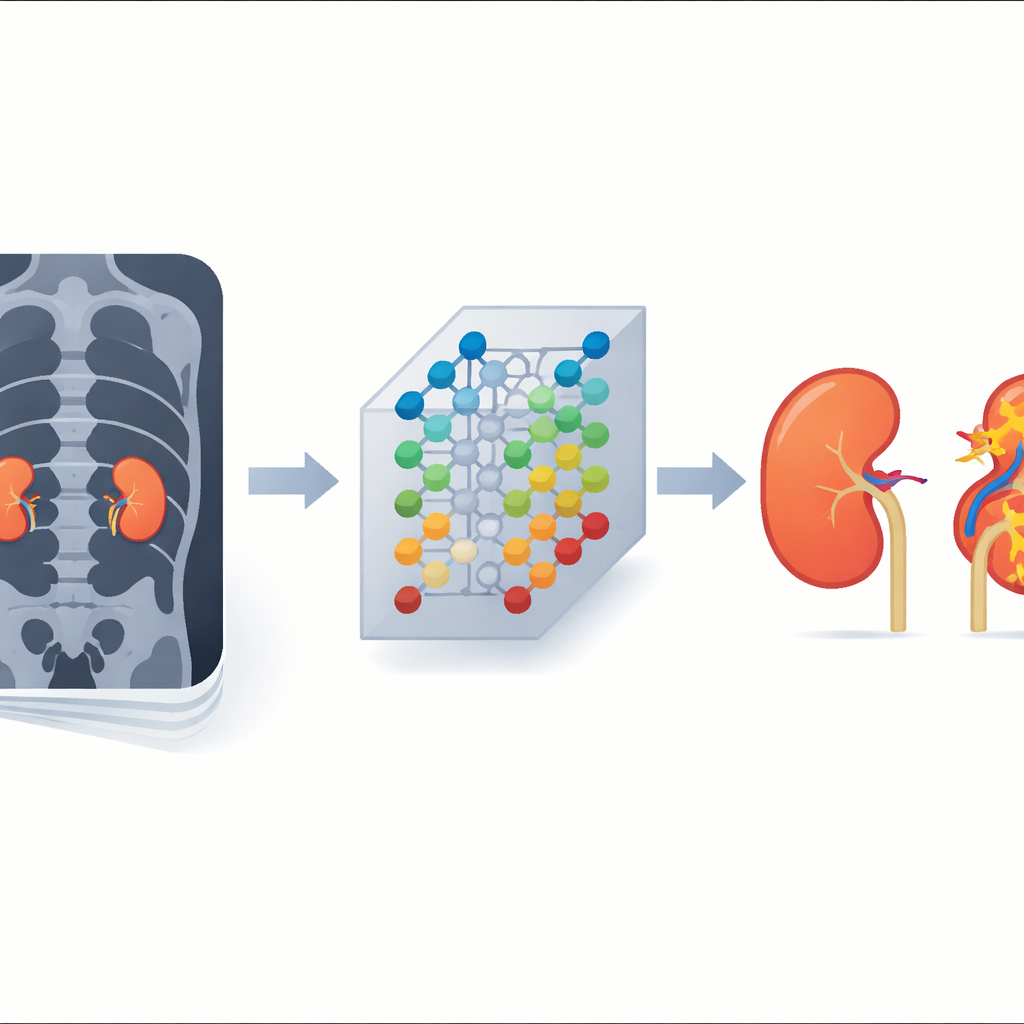
肾脏周围的隐性危险
研究者聚焦于透明细胞肾细胞癌,这是最常见的肾癌类型。许多此类肿瘤在影像上仍被归为“局限性”,即看似局限于肾脏。然而在 10–20% 的此类病例中,术后病理检查显示癌细胞已侵入肾周脂肪或邻近静脉。该分期称为 pT3a,与更高的复发率和死亡风险相关。常规 CT 或 MRI 往往无法发现这些微小的延伸,导致部分患者在本应进行更广泛切除时被选择实施保肾手术,从而存在风险。
教计算机读取细微线索
为了解决这一问题,团队收集了来自五家医院及一个公开数据集的 1661 名患者的 CT 影像和临床资料。他们先构建了传统的“放射组学”模型,测量肿瘤及其周围组织的众多手工设计特征,如形状和纹理。这些模型表现尚可,但仍难以捕捉相当一部分真实的侵袭性肿瘤。随后研究人员设计了 RENALNet——一种三维深度学习系统,直接查看肿瘤及其周缘的 CT 体积,学习自身的图像模式,而不只依赖预先定义的测量特征。
新工具与医生配合时的表现
RENALNet 在部分患者数据上训练,在剩余数据上测试,同时在四个外部医院队列上验证其泛化能力。在这些队列中,AI 模型在检测隐匿性更晚期肿瘤方面比放射组学更敏感,同时保持较高的准确性。重要的是,研究者还请初级、中级和高级放射科医生在有无 RENALNet 风险评分辅助的情况下解读 CT。当 AI 输出与各放射科医生的判断结合时,他们区分真实侵袭性肿瘤的能力得到提升,尤以经验较少的读片者为著,显示了人类专业知识与 AI 协同工作的潜力。
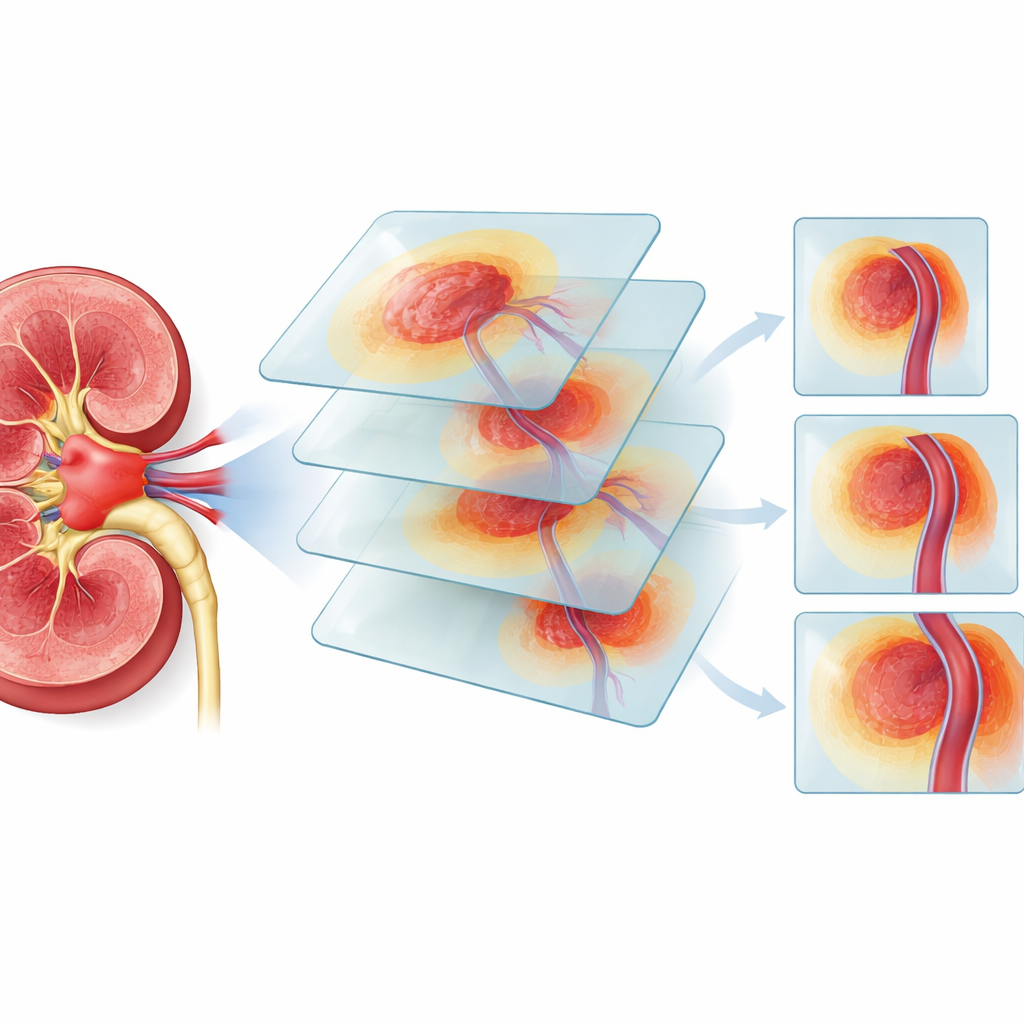
将影像与肿瘤行为相联系
研究进一步探问 AI 的风险预测是否反映真实的生物学侵袭性。在多个患者群体中,RENALNet 判为高风险的肿瘤显示出更高水平的 Ki-67(一种反映癌细胞分裂速度的标志物)。在 246 名有随访数据的患者中,AI 定义的高风险组在五年内疾病进展的可能性远高于低风险组。利用来自大型公开癌症计划的基因表达数据,团队发现高 RENALNet 评分与参与侵袭、炎症和癌细胞存活的分子通路激活相一致,提示模型所利用的 CT 模式与肿瘤内部更深层的遗传程序有关联。
这对临床护理可能意味着什么
综合来看,研究结果表明 RENALNet 能作为一种非侵入性的窗口,揭示肾脏肿瘤的真实危险性,即便在肉眼下 CT 扫描看似平静的情况下也是如此。通过标识更可能已突破肾脏界限的患者,该工具可帮助外科医生决定何时切除整个肾脏比尝试更小的切除更安全,何时需要更密切的随访。尽管该模型仍需在实时临床实践中验证并扩展到其它扫描类型和肿瘤亚型,但它提供了一个有前景的范例,说明同时“理解”影像与生物学的 AI 如何在未来增强癌症治疗决策的精确度。
引用: Li, S., Wang, C., Li, F. et al. Noninvasive prediction of occult pT3a upstaging in localized ccRCC with radiogenomic insights and prognostic relevance. npj Precis. Onc. 10, 104 (2026). https://doi.org/10.1038/s41698-026-01315-2
关键词: 肾癌, 医学影像人工智能, 深度学习, 外科计划, 放射基因组学