Clear Sky Science · zh
下一层:通过保结构与注意力引导的局部斑块到全局语境学习增强基础模型在计算病理学中的能力
教会计算机阅读癌症切片
病理学家在显微镜下检查癌症活检时,并不仅仅关注单个细胞——他们观察的是模式、邻域,以及肿瘤、免疫细胞和正常组织如何一起排列。现有的数字病理人工智能系统擅长在微小图像斑块中发现细节,但经常忽略更广泛的全局图景。本研究介绍了EAGLE-Net,一种新的人工智能方法,帮助计算机像人类专家一样观察癌症切片,同时兼顾局部细节与切片上组织的总体布局。

肿瘤组织的构型为何重要
肿瘤不仅仅是一团癌细胞。它存在于一个繁杂的邻里之中,充满血管、免疫细胞、结缔组织以及瘢痕或坏死区域。这些成分的排列——它们的距离、边界与混合方式——可能反映肿瘤的侵袭性以及患者对治疗的反应。传统病理学的人工智能系统通常将整张切片图像切成成千上万的小瓦片并几乎独立地分析它们,然后通过汇总所有瓦片的信息来推断诊断或结局。该策略常常忽略瓦片在空间上的相互关系,导致预测能力下降,并使AI生成的热图显得零散或难以解释。
捕捉更大图景的新方法
EAGLE-Net旨在弥合局部细节与全局结构之间的鸿沟。它以强大的“基础模型”为起点,这些模型已经能够从小斑块中提取丰富的视觉特征。在此基础之上,增加了一个新模块来编码每个斑块在切片上的来源位置,保留组织的真实几何结构,而不是将其挤压到畸变的网格中。通过多尺度滤波器,EAGLE-Net学习从微小的细胞级变化到更广泛的组织结构(如肿瘤边界和周围基质)的模式。随后使用注意力机制——本质上是一种为斑块和邻域分配重要性分数的方法——聚焦于对预测诊断或生存最为相关的区域。
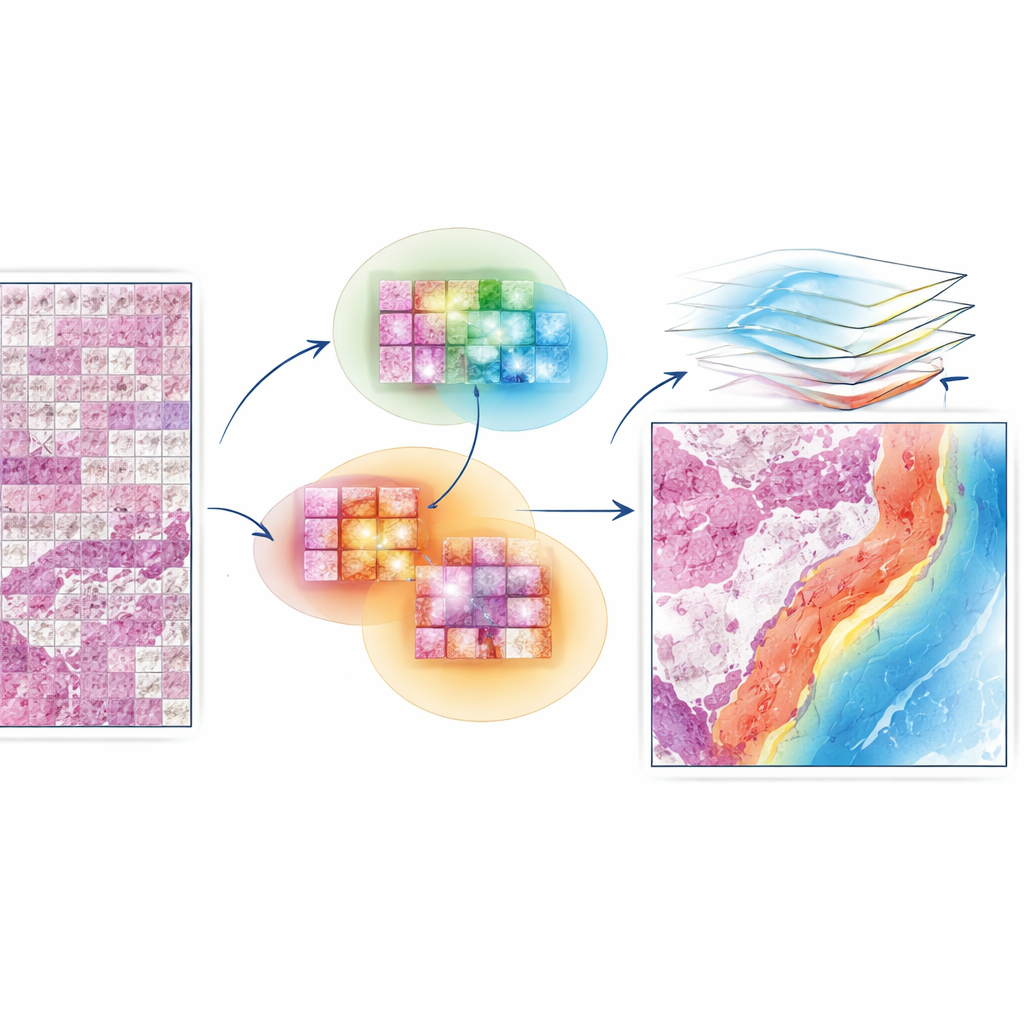
让模型从邻域中学习,而不仅仅是单点
EAGLE-Net的一项关键创新是教会网络不仅重视最重要的瓦片,也重视它们的邻近瓦片。在训练过程中,该方法反复识别模型认为信息量最大的瓦片,并鼓励模型将位于小半径内的周边瓦片视作同一有意义区域的一部分。这种“邻域感知”学习推动模型形成平滑、连续的注意力区域,与病理学家观察肿瘤前缘、免疫细胞簇和其他微环境时的视角相一致。与此同时,训练过程中的额外项主动促使模型忽略背景或空白区域,降低对杂质或空白处产生错误高亮的风险。
在多种癌症类型上验证其价值
研究人员在近1.5万张整片图像上测试了EAGLE-Net,覆盖包括肺、肾、胃、子宫、甲状腺、结直肠和前列腺肿瘤在内的10种不同癌症。他们评估了两项主要任务:预测患者生存期和对肿瘤类型或分级进行分类。在大多数癌症队列中,EAGLE-Net与若干领先的基于注意力的方法持平或表现更好,常常在生存预测分数和分类准确率上提升几个百分点——在群体层面上这是有意义的改善。它在与三种非常不同的基础模型配合时也表现稳健,显示其设计具有灵活性,并不依赖于单一的特征提取器。
看见模型推理的内部
除了原始准确性外,团队还仔细检查了EAGLE-Net在切片上“关注”的位置。与其他方法相比,其注意力图形成了更为平滑、连贯的区域,贴合肿瘤边界并捕捉侵袭边缘、坏死空隙和免疫细胞簇。与专家手绘肿瘤掩模的定量比较表明,EAGLE-Net高亮的区域与真实肿瘤的重叠更好,在正常组织上误报更少,且更忠实地再现复杂的肿瘤形状。该模型还将更大比例的注意力分配给肿瘤、坏死和免疫区室,而对正常肺组织或血管的关注较少,反映了病理学家在判断预后时的优先级。
这对未来癌症护理意味着什么
从实际角度看,EAGLE-Net证明在现有病理学AI之上加入空间意识和邻域推理,可以同时提升性能与可解释性。该方法不再将切片视为一袋互不相连的瓦片,而是学习识别具有生物学意义的小生态位——如肿瘤边界、免疫富集区和侵袭模式——这些都与患者结局相关。由于它可与多种不同的基础模型配合使用且不需要劳动密集型的像素级标注,EAGLE-Net能够广泛应用于大型数字切片档案。通过进一步验证并整合到临床工作流程中,此类系统可能帮助病理学家更精确地分层患者、发现新的基于组织的生物标志物,并最终指导更个性化的癌症治疗。
引用: Waqas, M., Bandyopadhyay, R., Showkatian, E. et al. The next layer: augmenting foundation models with structure-preserving and attention-guided learning for local patches to global context awareness in computational pathology. npj Precis. Onc. 10, 109 (2026). https://doi.org/10.1038/s41698-026-01312-5
关键词: 计算病理学, 癌症预后, 数字病理人工智能, 肿瘤微环境, EAGLE-Net