Clear Sky Science · zh
跨多种癌症类型的组织病理学全片图像中自动肿瘤分割的泛化
这对癌症护理为何重要
癌症诊断仍依赖专家在显微镜下仔细检查染色组织玻片——这是一项耗时的工作,且随着病例增多与病理学家短缺而愈发困难。本研究提出了一个简单但有力的问题:是否可以用一个人工智能系统在数字显微镜图像中可靠地找出多种肿瘤类型的癌变区域,而不必为每种癌症构建单独工具?若可行,这将减轻工作负担、加快诊断速度,并将先进分析扩展到数据稀缺的罕见癌症。
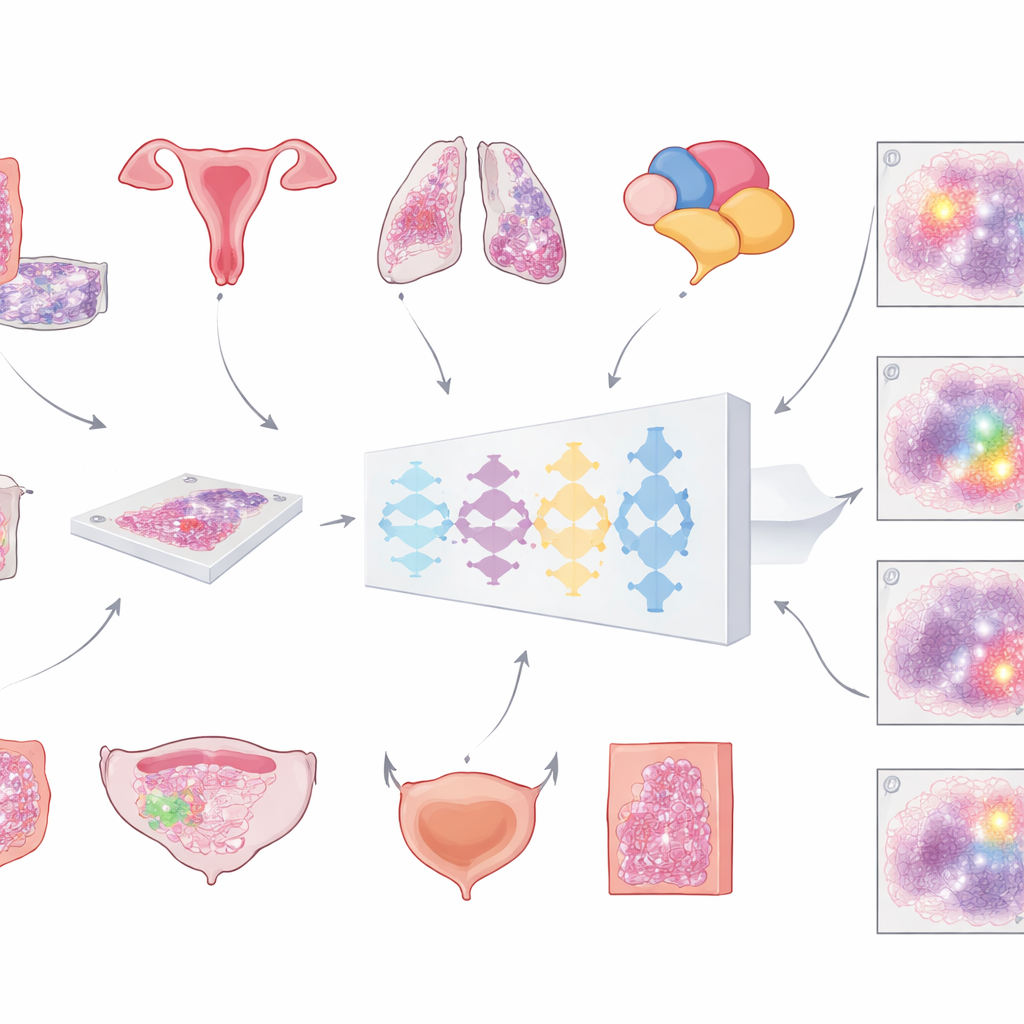
从玻片到数字助手
现代医院越来越多地将显微镜玻片进行扫描,生成巨大的、细节丰富的“全片图像”。任何基于计算的分析的第一步关键任务是把癌变组织与其他一切区分开——包括正常细胞、脂肪、空白玻片和各种伪影。迄今为止,大多数自动化工具都只在单一癌症类型上训练,限制了它们的适用场景。本工作团队旨在构建一个通用模型,能够在常规苏木精-伊红染色的切片上识别多种常见癌症的肿瘤区域。他们的愿景是一个可以插入多种诊断流程而无需每次重新设计的通用工具。
用一个模型识别多种癌症
为了构建该模型,研究者汇集了异常庞大且多样化的数字切片集:超过2万张全片图像,来自4000多名结直肠癌、子宫内膜癌、肺癌和前列腺癌患者。所有样本均来自标准的福尔马林固定、石蜡包埋组织,并在两种不同的高分辨率扫描仪上扫描。病理学家在每张切片上仔细勾画出肿瘤区域,提供了供计算机学习的“真实标注”。模型遵循多步流程:将每张巨幅图像切分为大尺寸重叠图块,通过深度神经网络为每个像素估计为肿瘤的概率,然后重组为平滑的概率图,最后转换为清晰的肿瘤与非肿瘤掩码。
对系统进行检验
关键在于,团队并未止步于训练集上的表现。他们在3000多名额外患者上测试了相同模型,覆盖六种癌症类型——其中包括训练时未使用的乳腺癌和膀胱癌——并使用来自多家医院和多款扫描仪的切片进行验证。准确性主要用标准重叠评分(Dice系数)衡量,当计算机的肿瘤轮廓与病理学家的完全一致时该分数为100%。对于结直肠癌、子宫内膜癌、肺癌、前列腺癌和乳腺癌中的大体完整样本,平均重叠超过80%,常常达到90%以上。在来自全球多个实验室与扫描仪的癌症基因组图谱(The Cancer Genome Atlas)大型外部集合中,性能同样保持在80%以上,表明模型能很好地泛化到其原始机构之外的数据。
它的局限与对比
主要弱点出现在早期的膀胱癌样本,这类样本通常通过一种产生微小、碎片化组织的取样程序获取。在这些情况下,模型常常未能标注任何肿瘤区域,尤其是当癌变面积非常小时。然而,一旦检测到肿瘤,其与病理学家轮廓的重叠率仍很高,对最终阈值进行简单调整即可改善结果——这暗示基础网络识别了模式,但后处理过于严格。研究者还训练了四个“专科”模型,每个专注于一种癌症,发现这些专科模型在其自身领域并未显著优于通用模型。而当专科模型应用到其他癌种时则大多表现不佳,而通用模型依然稳健。与一种流行但需要用户提示的通用医学分割工具相比,新模型通常表现相当或更好,且保持了完全自动化。
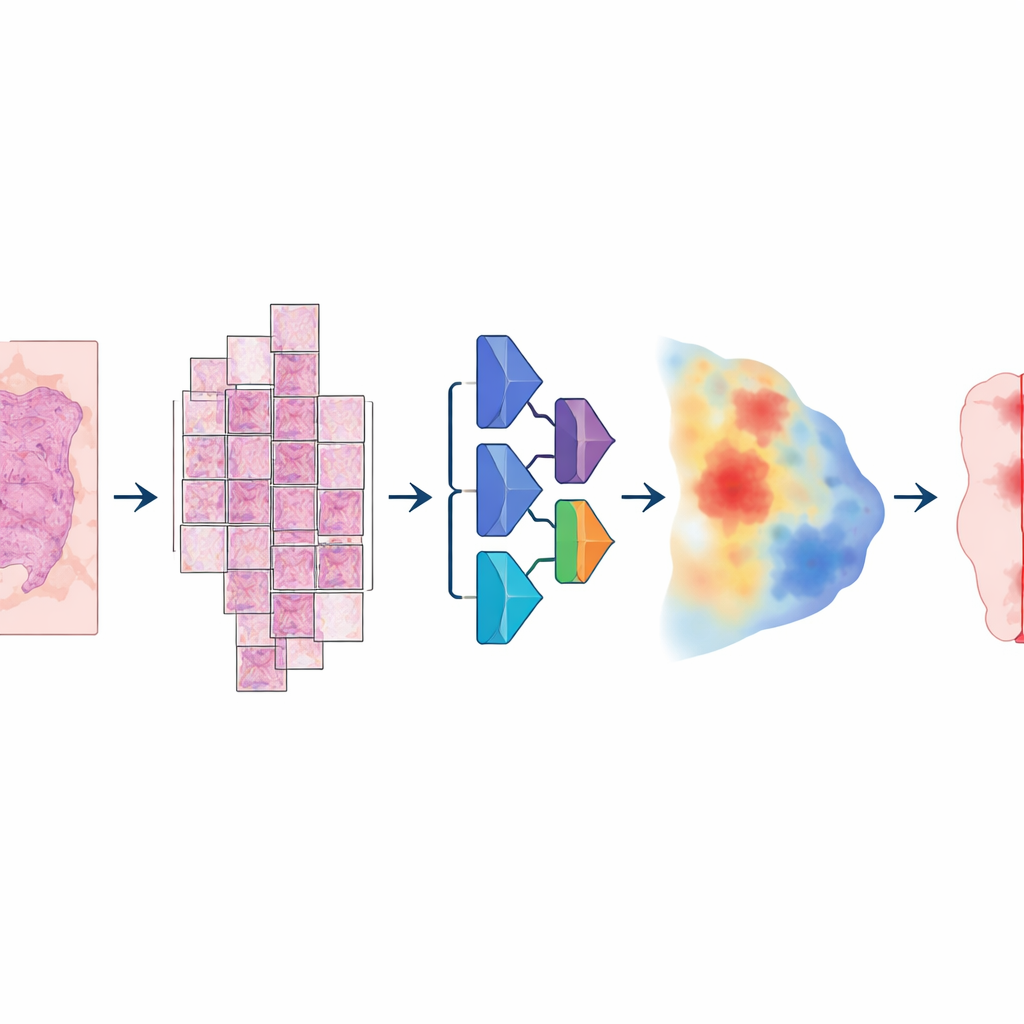
这对患者与医生意味着什么
对非专家而言,关键结论是:一个设计良好的AI系统能够在数字切片上可靠地标示多种主要肿瘤类型的癌变组织,而无需为每种疾病或扫描仪定制版本。它并不取代病理学家,但可以预先标出可能的肿瘤区域,支持一致的测量,并让专家把精力集中在最具挑战性的病例上。目前版本仍会漏检一些非常小或早期的肿瘤——特别是碎片化的膀胱样本及其他类似活检的组织——因此尚不适合检测最微弱的癌变痕迹。尽管如此,这项研究表明在真实世界条件下,广泛的“泛癌”肿瘤分割是可行的,并可作为未来自动化工具(例如评估肿瘤分级、预测治疗反应或指导精准治疗)的稳健第一步。
引用: Skrede, OJ., Pradhan, M., Isaksen, M.X. et al. Generalisation of automatic tumour segmentation in histopathological whole-slide images across multiple cancer types. npj Precis. Onc. 10, 107 (2026). https://doi.org/10.1038/s41698-026-01311-6
关键词: 数字病理学, 深度学习, 肿瘤分割, 全片成像, 泛癌模型