Clear Sky Science · zh
DDX41 通过相分离并激活 STING 通路促进 OSCC 中的 PD-L1 介导免疫逃逸
本研究为何重要
口腔癌常见且致死率较高,部分原因在于肿瘤能够学会躲避免疫系统的监视。本研究揭示了口腔鳞状细胞癌(OSCC)躲避免疫攻击的一种先前未被认识的机制。研究聚焦于一种名为 DDX41 的分子,展示了它如何帮助肿瘤细胞开启另一种蛋白 PD-L1 的表达,后者能有效令免疫细胞失去攻击能力。理解癌细胞与免疫系统之间这种隐秘的“对话”可能为更好的诊断与治疗开辟新途径。
口腔肿瘤中的一个棘手蛋白
研究者首先提出了一个基础问题:DDX41 在癌症中是否异常活跃?通过挖掘大型公共癌症数据库,他们发现包括头颈部癌在内的多种肿瘤类型中,DDX41 水平高于正常组织。将视角聚焦到 OSCC 时也观察到相同模式:患者的肿瘤样本中 DDX41 明显高于邻近的健康口腔组织。肿瘤中 DDX41 较高的患者随访预后较差,提示该蛋白与侵袭性疾病和较低生存率相关。对 DDX41 的检测在区分癌变与非癌变口腔组织方面也显示出潜力。
DDX41 如何助力肿瘤生长与扩散
为了超越相关性的描述,团队在体外培养的 OSCC 细胞中操纵了 DDX41。当降低 DDX41 时,癌细胞分裂减慢、形态发生改变,并且迁移与穿越人工屏障的能力下降——这些行为与降低转移能力一致。增强 DDX41 则产生相反效应,加快生长与运动。在将缺乏 DDX41 的 OSCC 细胞移植入小鼠体内的实验中,尽管动物总体健康良好,肿瘤却生长更小、更慢。综上实验表明 DDX41 并非旁观者,而是肿瘤进展的主动驱动因子。
一种隐藏的免疫逃逸开关
研究进一步探讨了 DDX41 如何改变肿瘤与免疫系统的关系。通过基因谱和蛋白质检测,作者显示 DDX41 在癌细胞内激活了一条被称为 STING–TBK1–NF-κB 的信号链。这条通路最终促进 PD-L1 的产生,PD-L1 位于肿瘤细胞表面,可与 T 细胞上的受体结合并抑制其杀伤功能。当降低 DDX41 水平时,关键的信号蛋白和 PD-L1 都下降,体外培养的 T 细胞变得更活跃、更能有效攻击肿瘤细胞。在小鼠肿瘤中,抑制 DDX41 降低了 PD-L1 水平,增加了数量和功能更强的抗癌 CD8⁺ T 细胞,并减少了具有免疫抑制作用的髓源性抑制细胞。
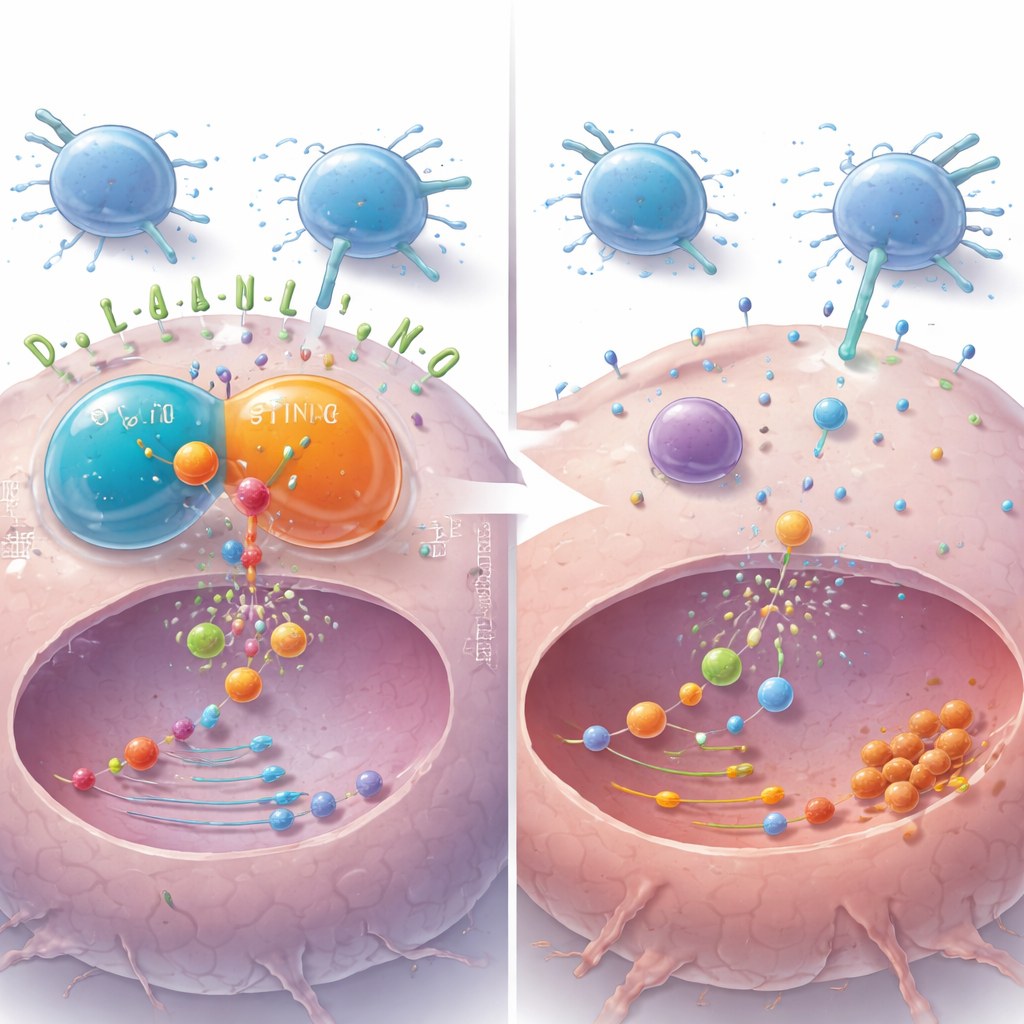
重塑信号的肿瘤液滴
该研究一个引人注目的发现是 DDX41 通过细胞内微小的类液滴结构发挥作用。研究中观察到该蛋白形成微观的球状凝聚体,表现出类似液滴的融合与物质交换行为。DDX41 与另一蛋白 STING 在物理上发生结合,并在细胞液相中共同形成共享的液滴。当研究者向肿瘤细胞引入 DNA 片段——模拟癌细胞中可能出现的异常 DNA 时,这些液滴数量增加,STING–TBK1–NF-κB 通路的信号被增强,最终推动 PD-L1 表达上升。破坏这些液滴或阻断通路部分环节的化学物质能削弱该效应,强调液滴状态有助于组织化并放大免疫逃逸信号。
对患者意味着什么
在来自 OSCC 患者的肿瘤样本中,高水平的 DDX41 与更活跃的信号蛋白、更多 PD-L1、更丰富的免疫抑制细胞以及更少有益的 CD8⁺ T 细胞并存。这描绘出一个一致的图景:DDX41 感知癌细胞内的异常 DNA,与 STING 形成液滴以增强信号级联,从而上调 PD-L1 以沉默免疫攻击。对患者而言,这些发现表明 DDX41 可作为识别更具侵袭性的口腔癌的标志物,也可能成为新的治疗靶点。阻断 DDX41 或其与 STING 的液滴依赖性合作或能降低 PD-L1,恢复 T 细胞活性,并提高现有免疫治疗的疗效。
引用: Tian, Z., Cui, H., Sun, S. et al. DDX41 facilitates PD-L1-mediated immune escape in OSCC via the phase separation and activation STING pathway. npj Precis. Onc. 10, 126 (2026). https://doi.org/10.1038/s41698-026-01308-1
关键词: 口腔鳞状细胞癌, 肿瘤免疫逃逸, PD-L1, STING 通路, DDX41