Clear Sky Science · zh
大规模单细胞分析与体外扰动模拟揭示肝细胞癌的动态演化:从起始到治疗靶向
为何肝癌的内部状态至关重要
肝细胞癌是最常见的肝癌类型,治疗难度大。许多病人对现有药物反应不佳,肿瘤常常复发或转移。其中一个重要原因是每个肿瘤由不断演化并持续与周围环境交流的多种细胞混杂组成。本研究利用强大的单细胞与空间基因检测技术,逐细胞观察这种演化过程,从早期肿瘤生长到晚期耐药疾病,并定位可能被新疗法利用的薄弱环节。
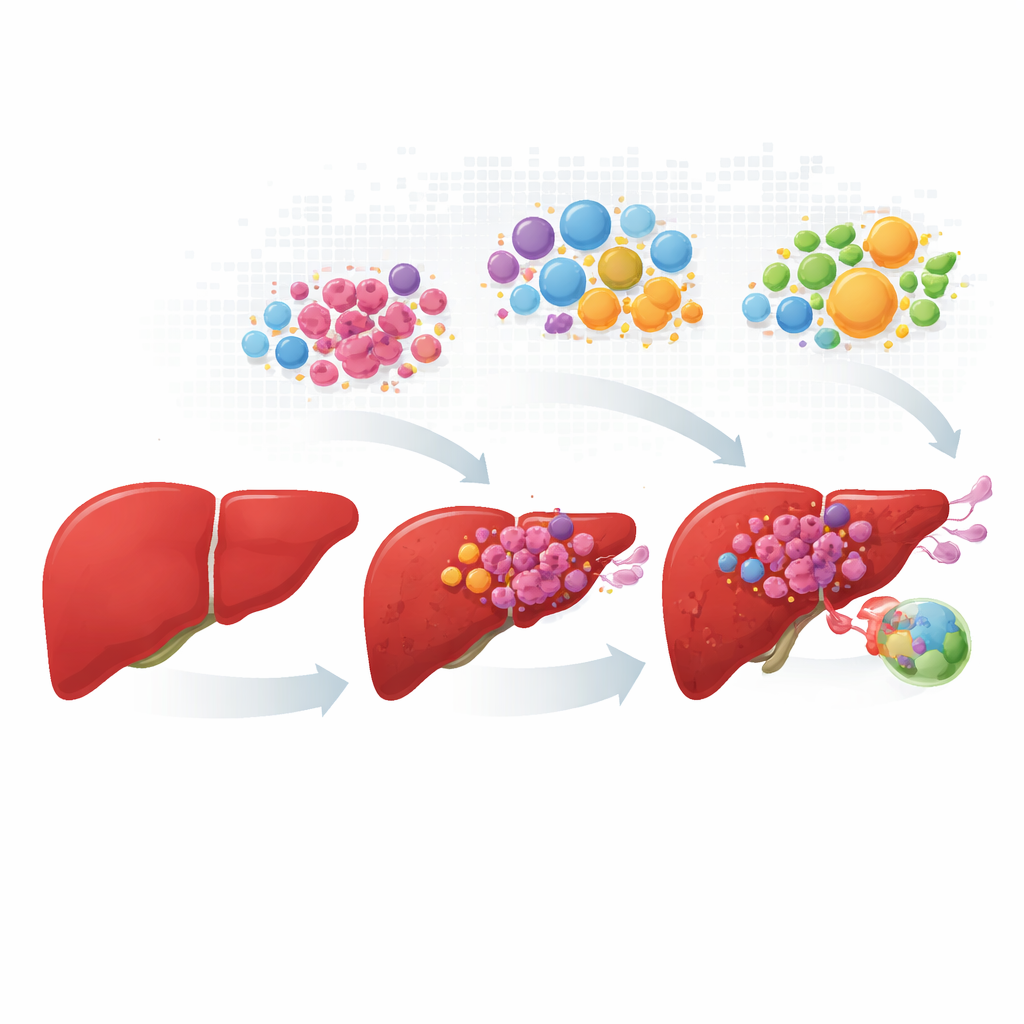
追踪癌细胞从早期改变到扩散的路径
研究者汇集并整合了来自一百多位病人的数据,涵盖正常肝脏、原发肿瘤、血管内病灶和淋巴结转移。与把每个肿瘤视为均质团块不同,他们对成百上千个单细胞进行分型,然后将这些细胞映射回实际组织切片的位置。癌性肝细胞呈现出四种重复出现的“性格”。一类保留了许多正常肝功能与代谢任务;其余三类则表现为应激驱动的生长、MYC生长通路高度活跃,或与侵袭性和炎症相关的行为。随着疾病进展,这四种状态的比例发生变化,快速增殖和侵袭性细胞在血管及淋巴结病灶中占主导。
四种肿瘤“性格”,不同的预后
这四种癌细胞状态并非仅为学术分类;它们与患者预后密切相关。富含类肝、代谢活跃状态的肿瘤与较好生存期相关,而以另外三种侵袭性状态为主的肿瘤往往预后更差。但即便是“有利”的状态也有隐患:该状态在未从肝癌药物索拉非尼获益的患者中明显富集,可能因为这些细胞保留了可使药物失活的解毒机制。通过重放细胞沿发育路径的运动,团队显示侵袭性、炎症相关细胞可以分化为更分化或更高增殖性的分支,表明肿瘤细胞可切换身份,可能逃避针对单一状态的疗法。
配角:免疫与基质细胞的共谋
癌细胞并非独自行动。研究发现了既能抗肿瘤又能暗中助长肿瘤的专门免疫细胞与支持细胞。在巨噬细胞群体中,部分类型产生有助抗肿瘤免疫的炎性信号,而另一些则在代谢上被重编程,抑制有益信号并促进血管生成与侵袭。这些“坏角色”巨噬细胞在晚期样本中扩增。同样,某些内皮细胞(血管内皮)与构建基质的成纤维细胞形成了与差预后相关的亚群。在晚期疾病中,一种特定内皮亚型与两类成纤维细胞形成紧密相连的中心,重塑细胞外基质,促进新血管形成,并与最具侵袭性的癌细胞状态相关联。
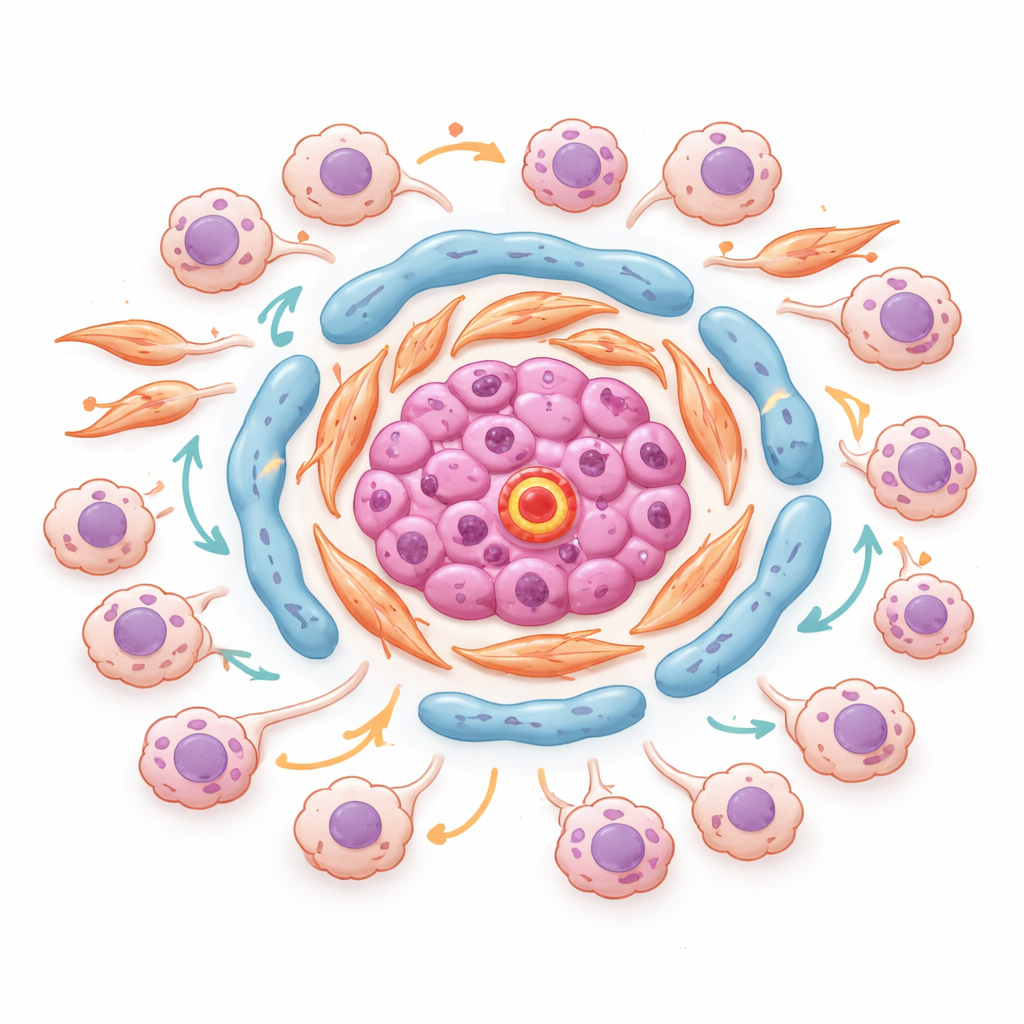
在肿瘤内部识别危险“街区”
借助空间转录组学——在不丢失组织位置信息的情况下测量基因活性,作者鉴定出肿瘤内部的有序“街区”。在一个代表性肿瘤中,富含ESM1分子的内皮细胞与偏好脂质、产基质的成纤维细胞聚集在间质岛的核心。围绕这些核心的是应激驱动和侵袭性癌细胞,所在区域具有强烈的TGF‑β信号和低氧特征。控制细胞对应激与炎症反应的关键转录因子在这些癌细胞状态间共享,并在肿瘤细胞接触这些基质中心的部位最为活跃。这提示肿瘤‑基质交界处的特定微环境积极推动癌细胞状态转换、增强侵袭性并促成耐药。
寻找共同的弱点以开发新疗法
为了从描述走向干预,团队使用在数百万细胞上训练的机器学习模型模拟“虚拟敲除”基因,预测哪些改变可将有害细胞推回更健康的状态。对比巨噬细胞、内皮细胞与癌细胞,他们发现一小组基因的去除有助于三类细胞的正常化。其中HSP90B1尤为突出:癌细胞系对其严重依赖,它在肝肿瘤中特别是对靶向药物和免疫疗法耐药的肿瘤中过度表达,高表达预示更差生存。HSP90B1编码细胞蛋白折叠工厂中的应激处理伴侣蛋白,支持多种表面受体和信号通路。由于已有选择性针对该伴侣蛋白的药物且这些药物能够重塑免疫环境,研究提出HSP90B1作为有前景的靶点,可在与现有肝癌疗法联合时克服耐药。
对患者与治疗的意义
总体而言,这项工作表明肝癌不是一种单一疾病,而是一个随着肿瘤生长与转移而变化的细胞状态与微环境生态系统。通过将特定癌细胞性格、支持细胞和空间“街区”与患者结局及药物反应关联起来,该研究为更精确的治疗提供了路线图:匹配疗法到占优细胞状态,破坏培养侵袭性行为的基质中心,靶向如HSP90B1之类被多类肿瘤与微环境细胞共同依赖的脆弱点。尽管还需进一步的实验室与临床验证,该团队构建的图谱为将肿瘤内部复杂性从障碍转化为更智能、更持久肝癌治疗机遇提供了详尽蓝图。
引用: Xia, P., Shuang, S., Fu, D. et al. Large-scale single-cell analysis and in silico perturbation reveal dynamic evolution of HCC: from initiation to therapeutic targeting. npj Precis. Onc. 10, 100 (2026). https://doi.org/10.1038/s41698-026-01307-2
关键词: 肝细胞癌, 单细胞分析, 肿瘤微环境, 空间转录组学, HSP90B1