Clear Sky Science · zh
基于人工智能的虚拟筛选平台识别出用于靶向癌症治疗的新型NSUN2抑制剂候选物:一种计算药物发现方法
击败顽固癌症的新途径
许多癌症致命,不仅因为它们发生,还因为它们学会了躲避我们最有效的药物。本研究探讨了一种有前景的新方法,通过人工智能在真实试验管混合之前,在计算机上筛选超过一亿种潜在药物,从而关闭肿瘤生长的关键助推器。
癌细胞内的隐藏开关
在细胞深处,一种名为 NSUN2 的酶类似于对 RNA 的化学荧光笔,RNA 是将基因转化为蛋白质的分子。通过在 RNA 上添加微小的化学标记,NSUN2 可以使与生长相关的信息更稳定、更易被读取。包括肺癌、胃癌、胰腺癌和乳腺癌在内的许多肿瘤会提高 NSUN2 的表达,从而增强其分裂、扩散和对靶向药物的耐受性。然而,尽管其重要性明显,能安全降低 NSUN2 活性、尤其是可逆抑制剂的候选物仍然很少。
让人工智能在分子海洋中搜索
传统的药物发现方法在实验室测试数百万种分子以对抗 NSUN2 时会遇到困难,因为每次实验都需要复杂的 RNA 和辅助化学品混合。研究人员因此构建了一个全数字化的流程。他们从 AlphaFold 生成人类 NSUN2 的预测三维结构开始,AlphaFold 是已革新结构预测的人工智能系统。为确保该模型可信,他们将其与一类通过 X 射线研究已知结构的密切相关酶进行了比对。NSUN2 与其天然辅助分子结合的关键口袋被发现高度保守,这使团队有信心将潜在药物虚拟对接到该位点是有意义的。
从数亿到寥寥数个
确定了靶点口袋后,团队转向了一个庞大的可购买分子公共数据库。他们首先将一组训练化合物对接到 NSUN2 口袋,并利用得到的评分训练机器学习模型以识别最有希望的分子形态。该模型随后快速筛查了约 3.5 亿种分子,并标记出大约 1.01 亿个可能的“命中”分子。为进一步缩小范围,对得分最高的一部分进行了更精确的重对接,仅保留约 12,000 个预测结合力强的分子。随后,这些分子经过一系列基于计算的安全性评估,以估算每个候选物在体内的吸收、分布、代谢和耐受性。经过这些筛选后,仅有 34 个分子在活性与药物相似性方面同时表现出色。
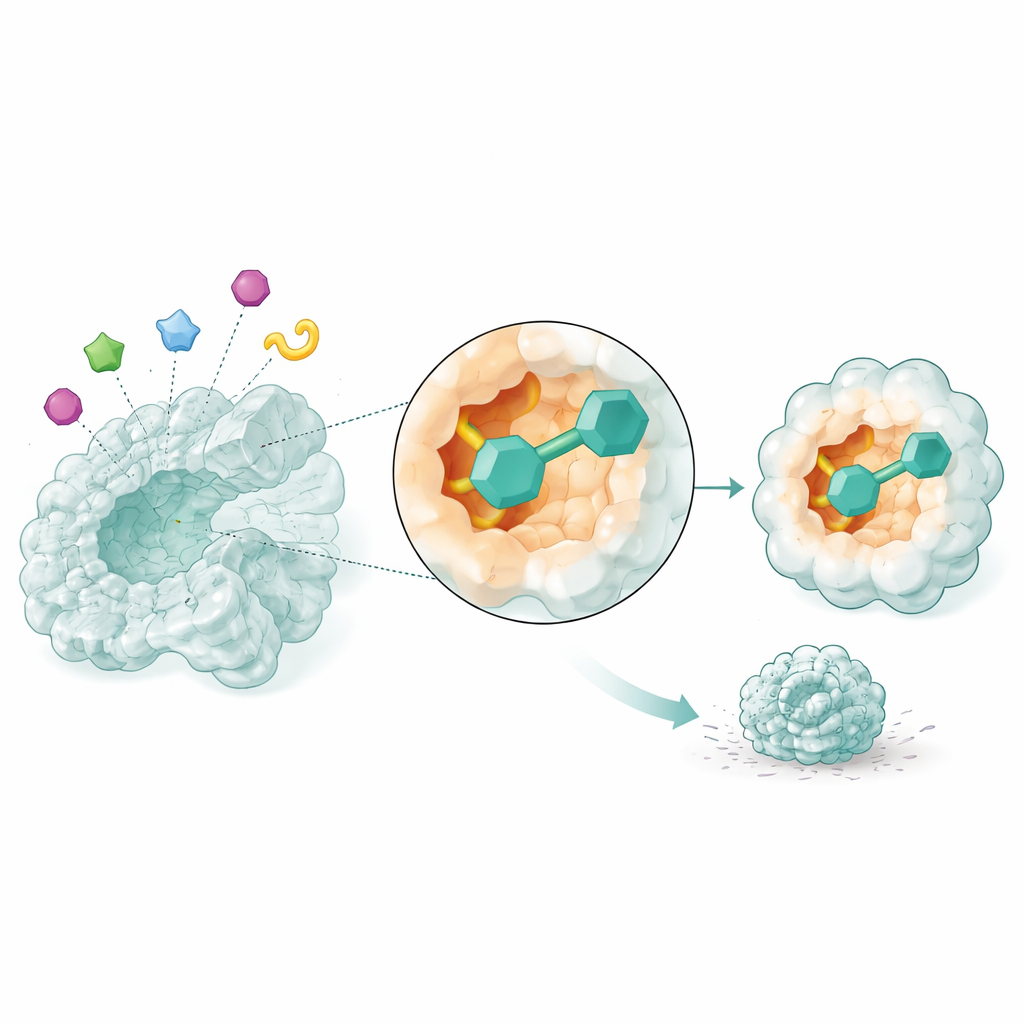
观察候选药物的动态表现
静态快照不足以判断药物是否能真正牢牢结合其靶点。因此研究人员使用了分子动力学模拟,模拟原子随时间的运动,观察最有前途的三个候选分子在 50 纳秒内与 NSUN2 的相互作用。其中两种仅以数据库编号识别的化合物形成了特别稳定的复合体:酶结构保持紧凑,其关键区域保持稳定而非松散,小分子在口袋内保持紧密配合并形成持久的接触。这些模拟表明,这两种化合物有望在真实细胞中可靠地抑制 NSUN2 的活性。
这对未来治疗意味着什么
尽管本研究的所有结果均来自计算模拟,仍需在实验室中验证,但该研究提供了一份现实的起点清单,用于开发新的 NSUN2 抑制药物。由于 NSUN2 帮助癌细胞稳定生长和生存信号,此类药物可能削弱肿瘤并有望使其对现有靶向疗法重新敏感,尤其是那些已产生耐药性的肺癌。同样重要的是,该研究展示了使用人工智能与基于物理的建模快速且低成本探索庞大化学空间的一般方法,为下一代精准癌症治疗提供了强有力的捷径。
引用: Yu, S., Peng, Q., Wei, W. et al. AI-driven virtual screening platform identifies novel NSUN2 inhibitor candidates for targeted cancer therapy: a computational drug discovery approach. npj Precis. Onc. 10, 98 (2026). https://doi.org/10.1038/s41698-026-01296-2
关键词: NSUN2, 表观转录组学, AI 虚拟筛选, 癌症药物发现, RNA 甲基化