Clear Sky Science · zh
APOLLO11:一种用于肺癌临床与转化研究的生物数据驱动模型
这对肺癌患者为何重要
过去十年里,得益于免疫治疗和靶向药物,肺癌治疗发生了巨变,但许多患者仍未能从这些进步中获益。本文介绍了APOLLO11,这是一个意大利全国性项目,旨在系统收集肺癌患者的真实世界数据和生物样本,并利用人工智能来弄清谁会对哪种治疗产生反应。对于患者和家庭来说,这指向了一个未来:治疗选择不再依赖反复试错,而是由对每位患者肿瘤和免疫系统的深入解读来指导。
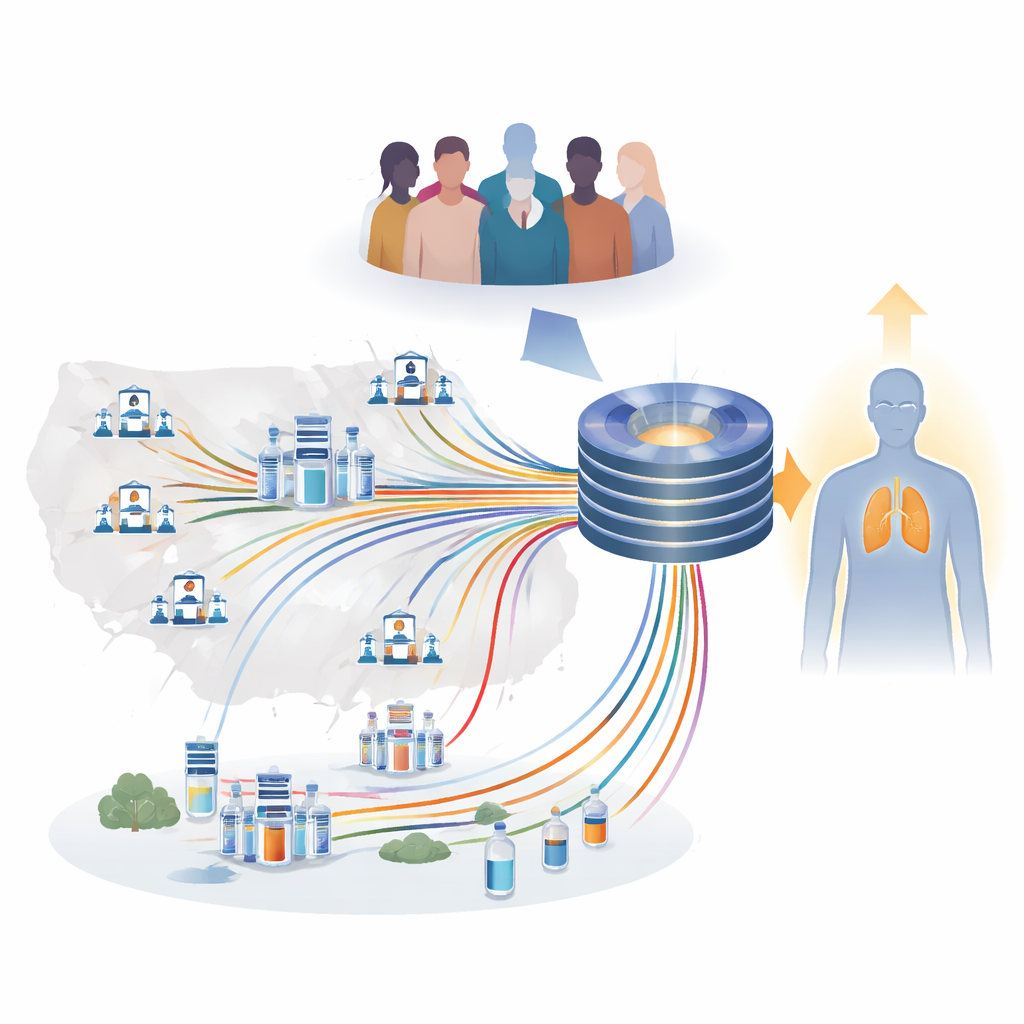
从一刀切走向数据引导的护理
作者指出,尽管出现了强效新药,大约一半的晚期肺癌患者要么从未响应,要么很快产生耐药。现有的血液和组织检测过于粗糙,无法可靠预测免疫治疗或靶向治疗的获益。传统临床研究通常一次检验一个假设,且在高度选择的患者群中进行,难以跟上新药和药物组合迅速涌现的步伐。APOLLO11的设立就是为了解决这一空白:构建一个长期、持续更新的资源,将来自意大利日常临床中数千名患者的常规临床信息、影像、实验室检测和高级生物学测量汇聚在一起。
构建全国性的学习网络
该项目连接了数十家医院,采用“枢纽-辐射”式组织:大型癌症中心和大学附属医院与较小的地区医院协同工作。每个地点使用安全的电子平台记录标准化信息,并在可能的情况下将肿瘤组织、血液、粪便等生物样本存放在本地低温库。中心不将所有物质集中运送到单一仓库,而是在原地保留样本,同时由中央团队记录样本的存在及存放位置。这种结构使得服务大量患者但可能缺乏科研基础设施的小医院也能有意义地参与进来,并有助于确保数据反映全国范围内肺癌患者的真实多样性。
从影像到细胞追踪疾病进程
APOLLO11对每位接受“创新”治疗(本质上指除传统化疗外的现代治疗手段)的参与患者采集多层次信息。临床数据包括年龄、疾病分期、所接受的治疗、毒副作用及生存情况。影像数据包括在关键时间点的CT、MRI和PET等扫描,利用“影像组学”方法将影像中微妙的模式转换为数千个量化特征。生物样本用于研究肿瘤DNA、基因表达、蛋白质、代谢物、机体免疫细胞,甚至肠道与口腔微生物。在部分患者中,免疫细胞会通过单细胞测序逐一分析,以揭示T细胞、中性粒细胞及其他可能影响免疫治疗反应的细胞行为细节。
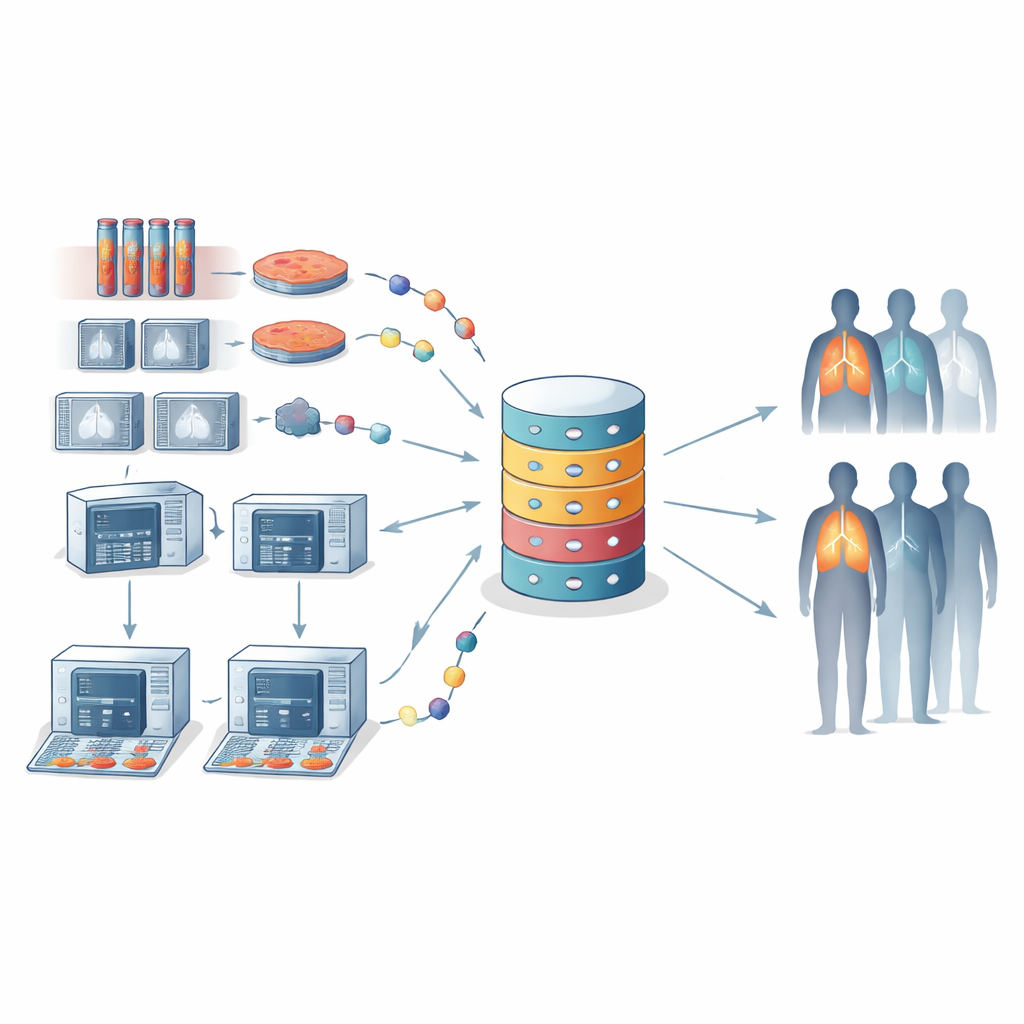
教计算机识别治疗模式
由于没有单一检测可以捕捉癌症的全部复杂性,APOLLO11计划使用机器学习将所有这些数据类型结合起来。许多分析不会将敏感的原始数据发送到单一中央服务器,而是采用“联邦学习”:各医院训练本地模型,仅共享模型更新,而非患者级记录。最终算法将被设计为可解释的:工具会展示哪些特征——例如特定的免疫细胞模式、影像特征或基因变化——在个体患者的预测中起主导作用。联盟内的早期工作已在探索血液中免疫细胞谱与晚期非小细胞肺癌免疫治疗结局之间的关系。
在保护隐私的同时共享知识
该网络也是未来科学问题的一个平台。参与中心的研究者,甚至联盟外的团队,都可以提出研究计划。一个指导委员会会根据临床重要性、新颖性、紧迫性和可行性对每项提案进行评估。当外部团队参与时,项目可以生成模拟数据集,这些数据在不暴露个人患者信息的前提下模拟真实数据,从而在开放性与像欧洲GDPR这样的严格隐私规则之间取得平衡。该治理模式旨在使访问公平、透明,并聚焦于能够真正改善护理的工作。
这对患者可能意味着什么
通俗地说,APOLLO11正在把肺癌患者的日常护理变成一个大型的、不断运作的实验室。通过系统地从多家医院的真实经验中学习,并将影像、血液检测、肿瘤分析与先进计算相结合,该项目旨在构建工具,在治疗开始前就能告诉医生哪些患者可能从免疫治疗或靶向药物中获益、谁可能面临严重副作用、以及谁可能需要不同策略。尽管仍面临保持一致的数据质量和长期资金等挑战,作者认为这种以数据为驱动、可解释且注重隐私的网络,是将精准医学变为现实——而不仅仅是承诺——的蓝图,对于肺癌患者具有重要意义。
引用: Prelaj, A., Provenzano, L., Miskovic, V. et al. APOLLO11: a bio-data-driven model for clinical and translational research in lung cancer. npj Precis. Onc. 10, 96 (2026). https://doi.org/10.1038/s41698-026-01295-3
关键词: 肺癌, 免疫治疗, 人工智能, 真实世界数据, 生物样本库