Clear Sky Science · zh
消化系统癌症中的T细胞受体克隆型多样性与专化
这项研究对癌症患者的重要性
癌症免疫疗法已经改变了许多患者的治疗前景,但并非对所有人都同样有效。本研究深入解析肿瘤内免疫细胞的“条形码”——T细胞受体,聚焦消化系统肿瘤,包括结直肠癌和胃癌。通过大规模读取这些条形码,研究者展示了免疫系统如何识别肿瘤、不同癌种间这种识别如何差异化,以及结直肠癌转移时识别方式如何变化。这些见解可帮助医生更准确地预测预后并设计更精确、个性化的免疫治疗方案。
肿瘤内的免疫指纹
T细胞是机体的定向防御者,每个T细胞携带独特的受体,使其能够识别特定异常细胞,包括癌细胞。研究团队对来自145名结直肠、胃和肝癌患者的415份肿瘤样本进行了T细胞受体测序,并结合详尽的临床信息。他们分析了定义两大关键T细胞家族的若干受体链:主导大多数适应性免疫反应的经典αβ T细胞,以及更像快速反应哨兵的γδ T细胞。结果发现,αβ T细胞倾向于形成体量大且高度多样的克隆群,而γδ T细胞则形成规模较小且更专一的群体。病情更晚期、存在血管入侵或发生远处转移的患者显示出更复杂的T细胞受体格局,提示肿瘤进展会将免疫系统推向更广泛、更复杂的对抗状态。
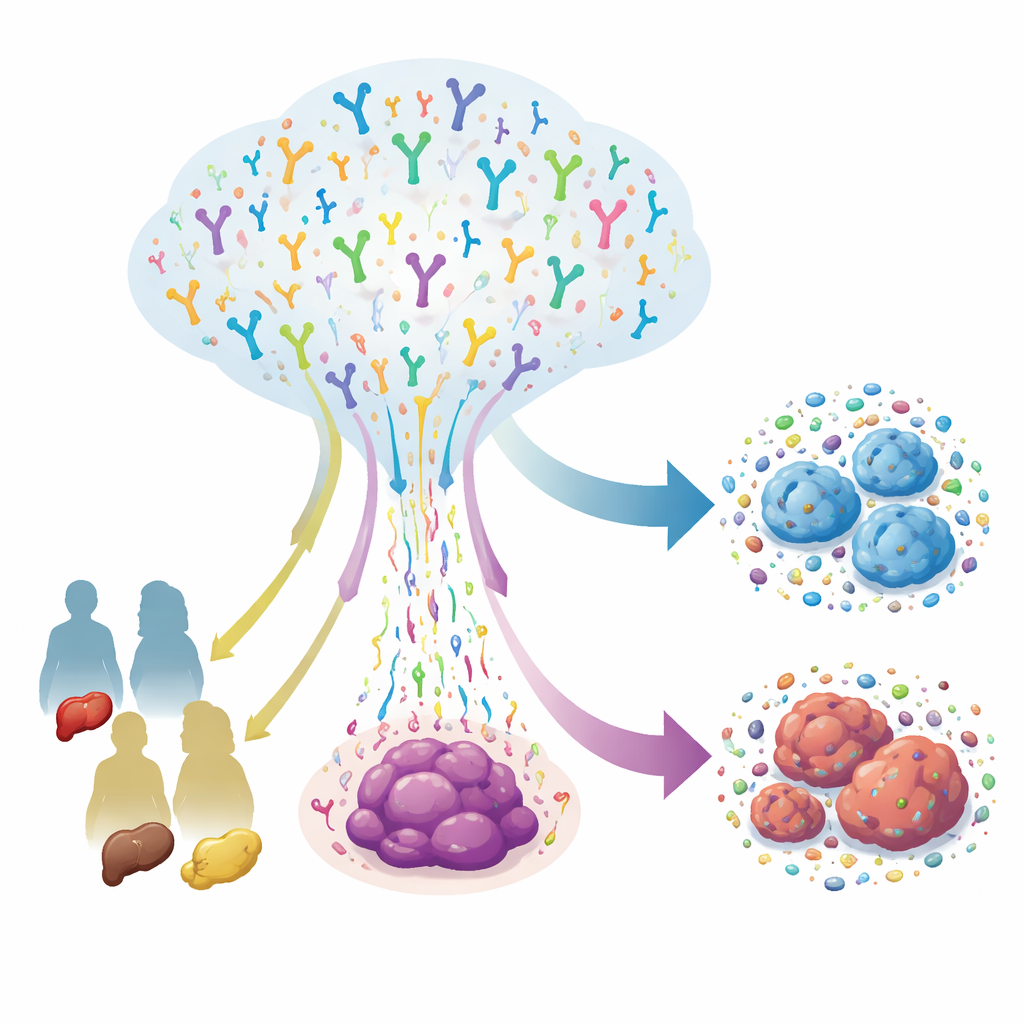
不同癌症,不同的免疫策略
尽管这些肿瘤都发生在消化系统,但它们对T细胞的吸引和塑造方式并不相同。结直肠癌在经典β链的受体基因片段组合上表现出富集,表明经典T细胞发挥了重要作用。相比之下,胃癌则更常使用γδ T细胞受体,暗示这些较少研究的哨兵细胞在胃肿瘤中可能具有特殊角色。当研究者聚焦于受体中实际接触靶标的关键部分——短环(CDR3)时,发现跨癌种存在共享的序列模式,这表明T细胞受到共同选择压力的引导。但同时在长度、氨基酸组成以及反复出现的小“基序”上也存在明显差异,提示每种肿瘤类型都迫使T细胞去解决略有不同的识别难题。
免疫攻击的共享与特异性靶点
利用已知T细胞-抗原对的全球数据库,作者将特定受体模式与其可能的靶点关联起来。一些抗原在结直肠癌和胃癌中均有出现,包括已知的驱动基因和免疫相关蛋白,如KRAS、SF3B1、BST2,以及若干经典的癌-睾丸抗原。这些共享靶点支持可跨多种肿瘤类型使用的“泛癌”策略。与此同时,各癌种也显示出自身的专属靶点。结直肠肿瘤与如MAGEA10、WT1及仅在癌细胞中发现的融合基因等抗原相关,而胃肿瘤则特有地表现出参与mRNA调控的PABPC1。这类肿瘤特异性抗原是高度选择性疫苗或工程化T细胞疗法的有吸引力候选靶点,能在不伤及健康组织的情况下发挥作用。
癌症转移时免疫签名如何转变
研究特别关注已发生转移的结直肠癌,比较了有无远处转移患者的肿瘤。转移性肿瘤体积更大、更易侵袭血管,且血液中的常规肿瘤标志物水平较高。它们的T细胞受体库也更为丰富和复杂,尤其是在β链上,这与更艰难且更多样化的免疫对抗一致。通过追踪在原发与转移环境间共享的克隆,研究者将它们归为稳定、萎缩或扩张的群体。一个显著发现是,一些最初在原发肿瘤中稀少的γδ T细胞克隆在转移性疾病中强烈扩张,且随着肿瘤增大变得更加丰盛。在经典T细胞中,一组特别扩张的克隆在β链中携带特定的序列基序,并频繁靶向MLANA这一肿瘤相关抗原。结直肠肿瘤中高表达的MLANA与患者更好的生存相关,提示该抗原可能标志着仍能被免疫系统识别并对免疫治疗有响应的肿瘤。
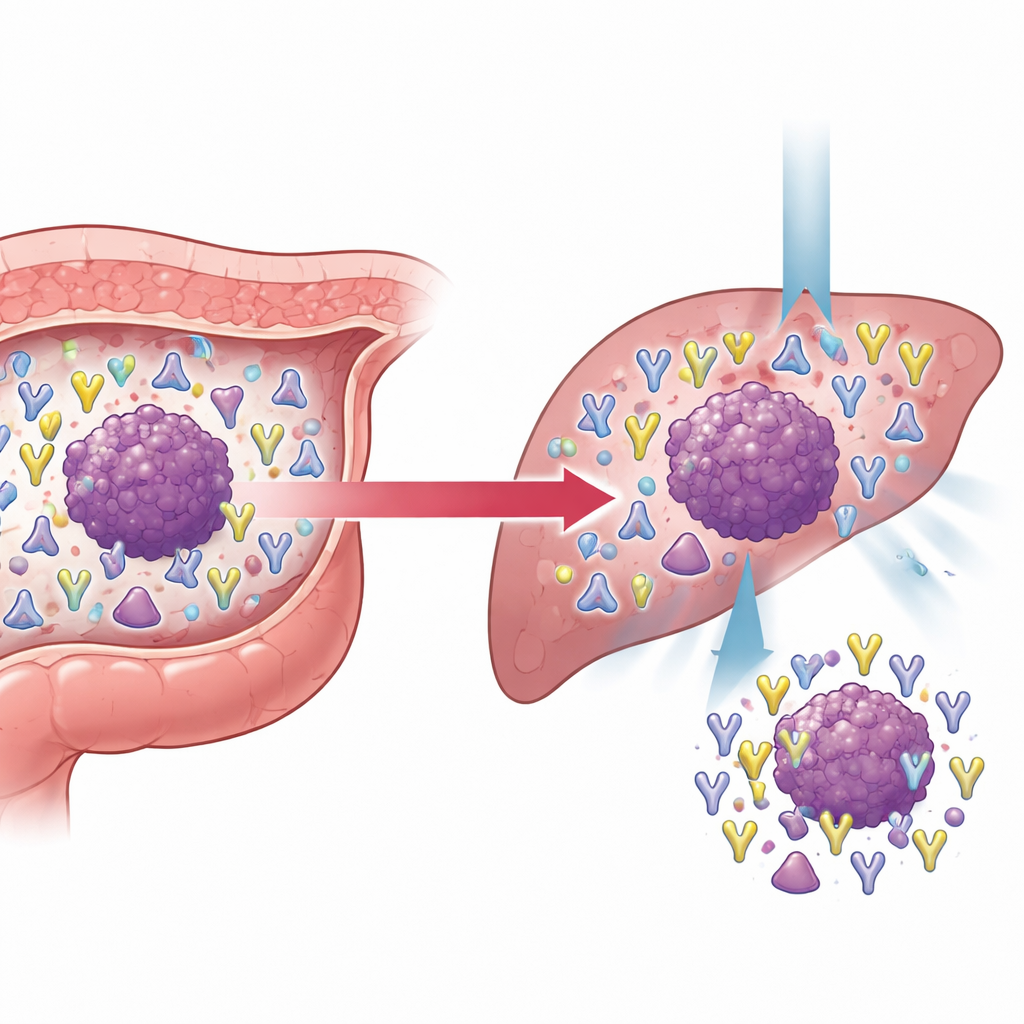
对未来癌症护理的意义
总体而言,这项工作表明消化系统癌症内的免疫格局并非随机,而是受癌种、分期和转移情况的共同塑造。特定的T细胞受体模式可作为可读的指纹,反映免疫系统如何与肿瘤互动,揭示了共享与癌种特异的抗原。对患者而言,这指向一个未来:医生可以从肿瘤样本中剖析T细胞受体库,以细化预后判断、更智能地选择免疫疗法,甚至设计基于最有效T细胞克隆的定制化治疗。在结直肠癌与胃癌中,此处识别的受体签名与抗原为此类精准免疫治疗努力提供了路线图。
引用: Li, L., Li, J., Wang, F. et al. T-cell receptor clonotypic diversity and specialization in digestive system cancers. npj Precis. Onc. 10, 91 (2026). https://doi.org/10.1038/s41698-026-01294-4
关键词: T细胞受体, 结直肠癌, 胃癌, 肿瘤免疫, 免疫治疗生物标志物