Clear Sky Science · zh
微小RNA-29b缺失通过DNMT3b介导的STING下调,削弱KRAS突变结直肠癌放疗诱导的抗肿瘤免疫
这项研究为何重要
对于许多直肠癌和结肠癌患者,放疗是术前治疗的重要组成部分。但有些肿瘤几乎不缩小,且癌症常复发或转移。本研究深入解析结直肠癌中一种常见基因改变——KRAS突变,说明为何这些肿瘤常对放疗和新型免疫疗法耐受,并提出一种可将机体免疫反应重新激活的策略。
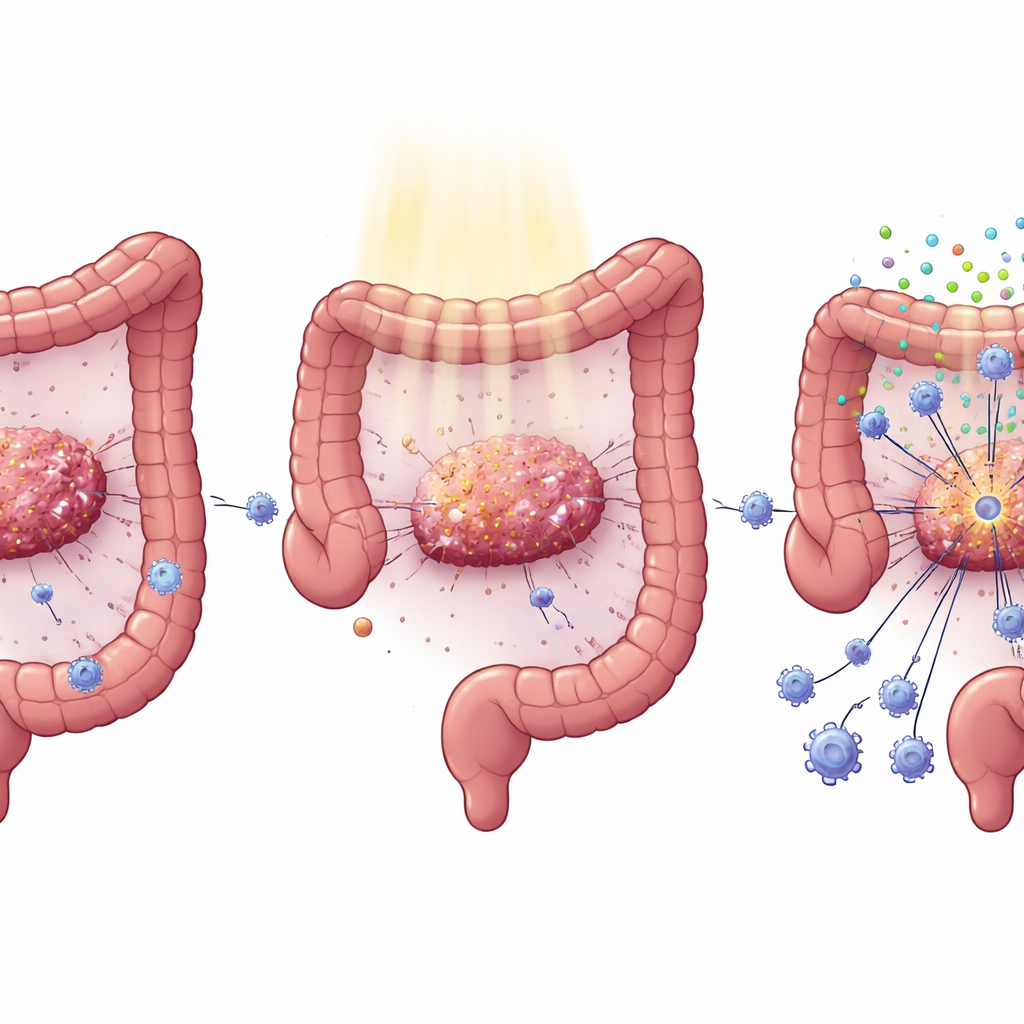
一种常见突变如何让肿瘤躲避免疫攻击
结直肠癌常携带KRAS基因突变,这是一种驱动肿瘤生长和转移的重要因子。临床上已注意到KRAS突变肿瘤对靶向药物和放疗的反应常较差。通过挖掘大型癌症数据库并分析患者样本,作者发现携带KRAS突变的肿瘤肿内致癌性CD8细胞较少,促免疫的干扰素信号活性也较弱。在接受根治性直肠癌术前常规放化疗的患者中,野生型KRAS的肿瘤在治疗后肿瘤内CD8细胞增加明显多于KRAS突变者,这有助解释其更好的临床结局。
癌细胞内缺失的报警系统
放疗不仅损伤肿瘤DNA;它还能像照明弹,促使癌细胞释放DNA片段,激活称为cGAS–STING的内源性报警通路。当STING活化时,细胞产生I型干扰素及其他信号,吸引并激活包括T细胞和树突状细胞在内的免疫细胞。研究者显示,在被工程化携带KRAS突变的结直肠癌细胞中,这一报警系统被削弱:放疗后这些细胞产生的干扰素及相关分子明显减少。在小鼠模型中,沉默KRAS可恢复肿瘤中的STING表达,增强干扰素信号,并导致CD4和CD8 T细胞增多、调节性T细胞减少以及更强的肿瘤控制——不仅局限于受照射肿瘤,也出现在远处未照射的“离位”肿瘤中。
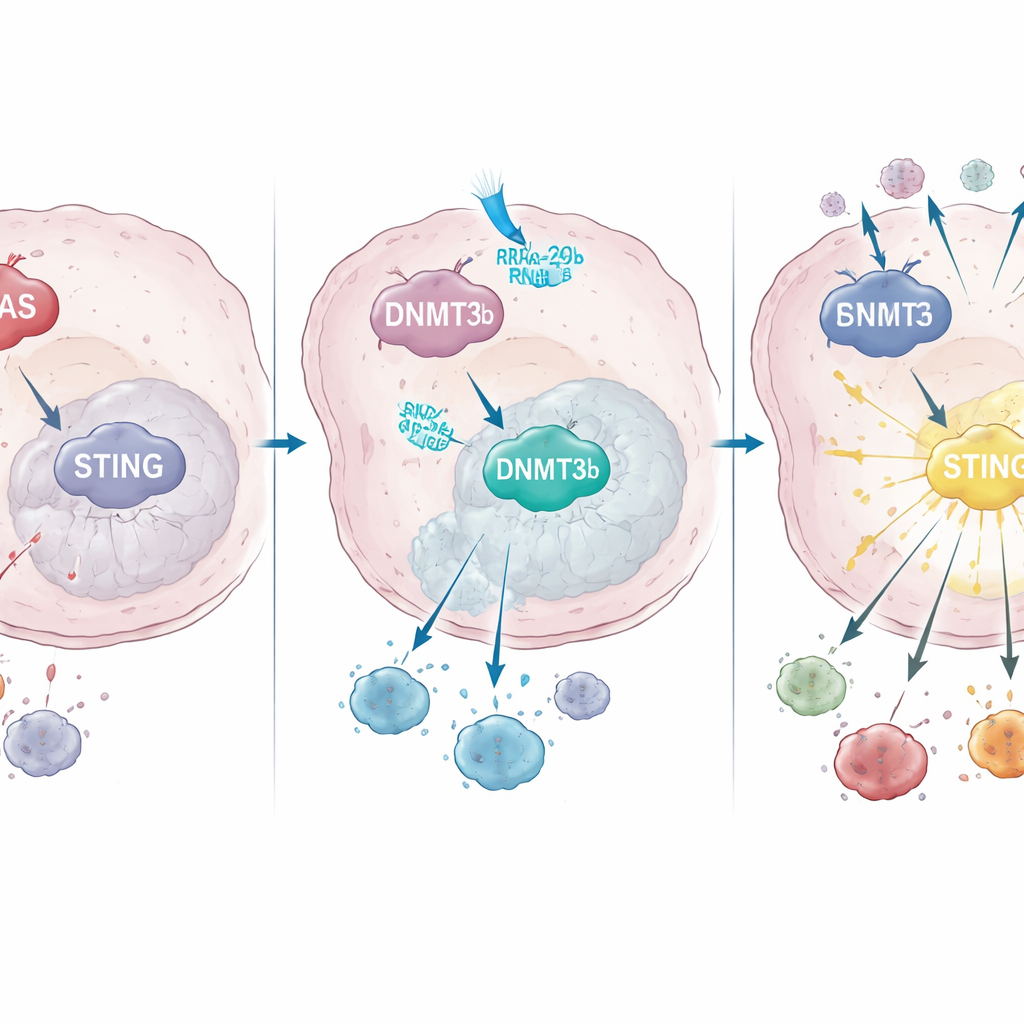
KRAS如何重编程基因调控以关闭STING
更深入的研究发现,KRAS突变促进了一种名为DNMT3b的DNA修饰酶的活性,此酶向特定DNA区域添加甲基基团,从而使邻近基因沉默。在细胞系和患者样本中,高表达的DNMT3b与低表达的STING密切相关。STING启动子(DNA“开关”区域)的一段关键序列在KRAS突变肿瘤中高度甲基化,而在野生型KRAS肿瘤中则不然。那些在放化疗后仍能上调STING的患者,其肿瘤有更多的CD8 T细胞浸润且生存更佳,强调了该通路对治疗成功的重要性。
一种可重新唤醒报警的小RNA
作者接着探究为何DNMT3b在KRAS突变癌中丰度偏高。通过微小RNA测序,他们鉴定出一种微小调控RNA——microRNA‑29b‑3p,正常情况下它可抑制DNMT3b,但在KRAS突变下被强烈抑制。将该microRNA恢复到体外培养的KRAS突变细胞中,可降低DNMT3b、恢复STING,并在放疗后增强干扰素产生;阻断该microRNA则产生相反效果。在肿瘤样本中,KRAS突变患者通常表现为microRNA‑29b‑3p低、DNMT3b高、STING低,且microRNA‑29b‑3p较高的患者生存更长,将这一分子链直接与临床结局关联起来。
一种靶向基因递送策略可增强放疗与免疫疗法
为将这些发现转化为潜在治疗,研究团队构建了一种无害的病毒载体(AAV),在主要在结直肠癌细胞中活跃的启动子控制下递送microRNA‑29b‑3p。在携带KRAS突变结直肠肿瘤的小鼠模型中,给予该AAV联合局部放疗显著缩小了受照射肿瘤和远处未受照射的肿瘤。肿瘤表现为DNMT3b降低、STING上调、干扰素信号增强,并有大量T细胞及其他免疫细胞浸润。当相同的microRNA‑29b‑3p治疗与针对PD‑1的免疫检查点抑制剂联合使用时,生存进一步提高,而这种益处依赖于CD8 T细胞,证实免疫系统在其中发挥了关键作用。
这对患者可能意味着什么
简而言之,这项研究揭示了KRAS突变结直肠癌如何“切断”放疗通常会触发的内源报警系统,从而逃避免疫攻击。通过恢复单一的小RNA——microRNA‑29b‑3p,研究者能够降低DNMT3b、重启STING,使免疫学上“冷”的肿瘤变为“热”的肿瘤,从而更好地响应放疗和免疫检查点抑制。尽管该研究仍处于临床前阶段,但它指向了未来将放疗与肿瘤靶向基因治疗配对以克服KRAS突变耐药性的可能路径,有望使现有疗法对更多患者有效。
引用: Chang, HY., Chen, JY., Ke, TW. et al. Loss of MicroRNA-29b promotes DNMT3b-mediated STING downregulation to attenuate radiotherapy-induced antitumor immunity in KRAS-mutated colorectal cancer. npj Precis. Onc. 10, 93 (2026). https://doi.org/10.1038/s41698-026-01290-8
关键词: KRAS突变结直肠癌, 放疗耐受, STING通路, 微小RNA-29b, 肿瘤免疫学