Clear Sky Science · zh
多组学深度学习提升基于FDG PET-CT的乳腺癌长期预后预测
这对患者和家庭意味着什么
当被诊断出乳腺癌时,患者通常首先会问:“这对我的未来意味着什么?”现有的分期系统和化验只能给出粗略的估计。本研究探讨将医学影像、医师报告和基本临床信息与先进的人工智能相结合,能否提供更清晰、更个体化的长期生存和复发风险预测。
窥探机体的能量使用情况
本研究的重要工具之一是称为FDG PET-CT的扫描。它不仅显示组织的形态(如常规CT),还展示组织的葡萄糖摄取量,进而反映肿瘤的代谢活性。临床上已有证据表明,这类扫描的一些数值——例如肿瘤的“亮度”或体积——与预后相关。然而,传统测量只捕捉了图像中丰富信息的一小部分,并且常依赖专家手工勾画肿瘤,耗时费力。
教计算机阅读影像与报告
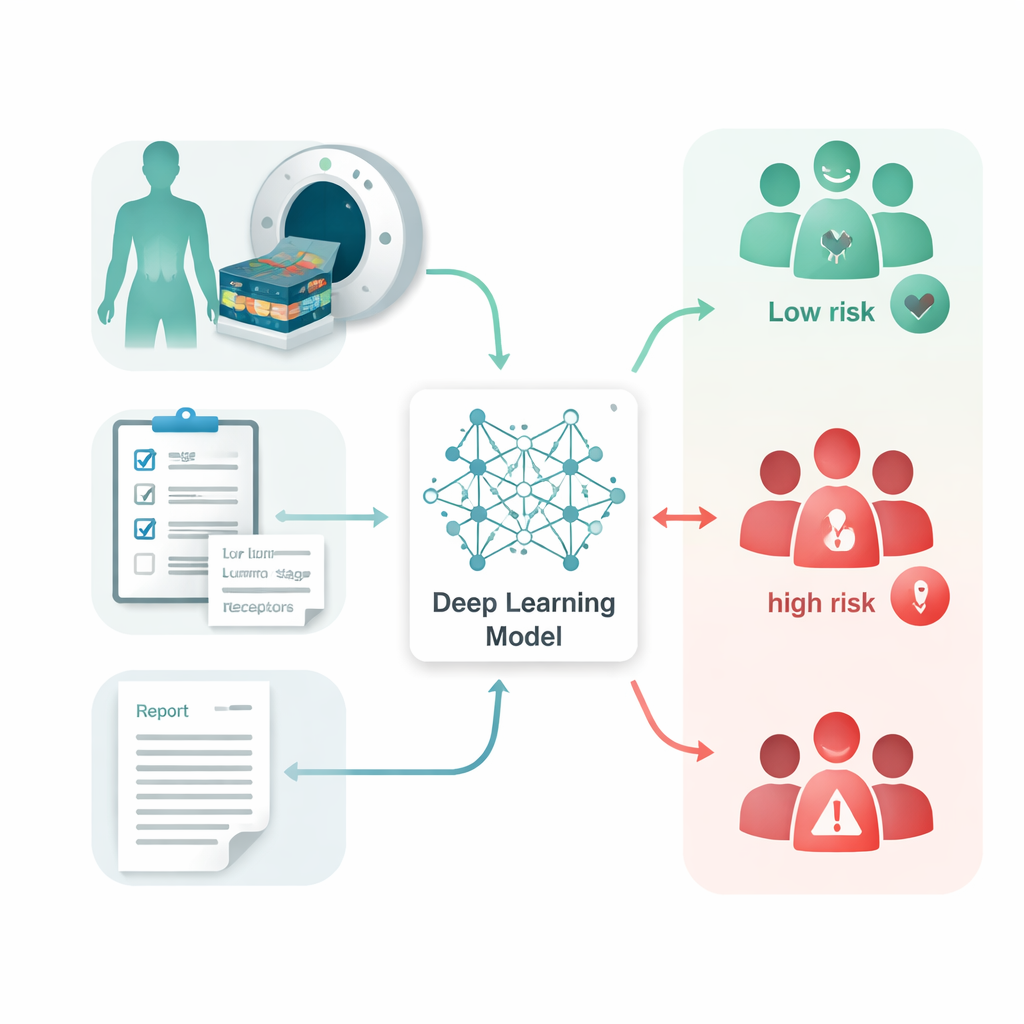
研究人员收集了荷兰一家癌症中心15年间1,210名乳腺癌女性患者的FDG PET-CT影像、相应的放射学报告和常规临床数据。入组时无远处可见转移。他们构建了一个名为多组学预后分层(Multi-Omics Prognostic Stratification,MOPS)的系统,采用深度学习——一种从大数据中学习模式的人工智能方法——将三类信息结合起来:影像本身、放射科医师的书面报告,以及年龄、肿瘤大小、淋巴结状况和激素受体类型等临床因素。一个自动程序首先勾画出乳腺肿瘤和受累淋巴结,使模型无需人工描绘即可专注于最相关的区域。
从多重线索中获取更多信息
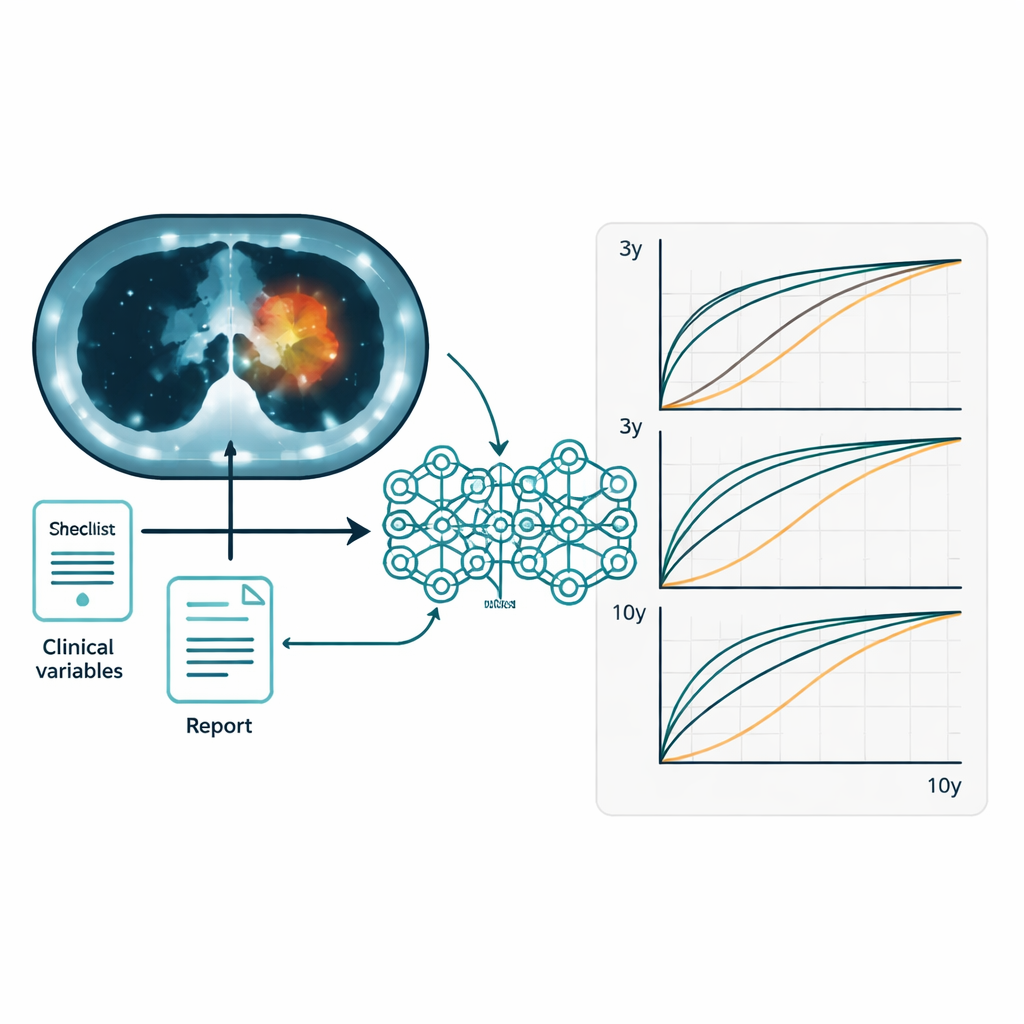
团队先评估了传统基于影像的指标在预测生存和复发方面的表现。反映总体肿瘤负荷的指标(如代谢肿瘤体积和总病灶糖酵解率)优于简单的峰值亮度度量,但其准确性仍然有限。一个分析整个胸部PET-CT的深度学习模型在这些传统参数之上有所提升。随后,研究人员分别测试了三类数据“流”:影像、书面报告和临床信息。在单一来源中,临床数据本身提供了最强的预后信息。然而,当三者在MOPS系统中融合时,性能进一步提高,在3年、5年和10年的总生存和无病生存预测上都更为可靠。
打开黑箱
鉴于影响治疗决策的工具需要可被信任和解释,团队在设计MOPS时兼顾了可解释性。叠加在CT切片上的热力图显示模型聚焦于原发乳腺肿瘤和受累淋巴结,而非图像中无关的区域。对于临床数据,模型突出了诸如肿瘤大小(T分期)、淋巴结状况和家族史等熟悉且影响力大的因素。在文本报告中,模型倾向于强调描述淋巴结、肿瘤位置和代谢活性的词语,呼应了放射科医师的判断。跨越不同肿瘤分期和生物学亚型,模型能够将患者分为高风险和低风险组,尽管对于非常小、早期且本就有极佳生存率的肿瘤,这种区分自然不如在更晚期病例中明显。
这对临床护理可能意味着什么
在实际层面,这项工作表明,经过慎重设计的影像、医师报告与常规临床信息的联用,能够比任何单一信息源更准确地估算乳腺癌患者的长期预后。如果在其他医院和不同扫描设备上获得验证,像MOPS这样的工具可以帮助医生识别确实需要更密切随访或更积极治疗的患者,同时减少对低风险患者的不必要治疗和相关焦虑。该系统并非取代临床医生,而是作为第二重视角,将复杂数据提炼为个体化的风险评分,支持更清晰的预后沟通和后续决策。
引用: Liang, X., Zhang, T., Braga, M. et al. Multi-omics deep learning improves FDG PET-CT-based long-term prognostication of breast cancer. npj Precis. Onc. 10, 74 (2026). https://doi.org/10.1038/s41698-026-01283-7
关键词: 乳腺癌预后, PET-CT 影像, 深度学习, 多组学, 生存预测