Clear Sky Science · zh
一种可解释的深度学习模型,用于从苏木精-伊红染色切片预测子宫内膜癌分子亚型
这对女性健康为何重要
子宫内膜癌起源于子宫内膜,是女性中最常见的癌症之一,其死亡率在全球范围内呈上升趋势。临床上已知道此类癌症实际上存在若干不同的分子“类型”,它们对手术、放疗、化疗及新型免疫治疗的反应各不相同。当前识别这些分子亚型通常需要昂贵且耗时的基因检测,许多医院难以广泛提供。本研究探讨了一种精心设计的人工智能(AI)系统是否能解读常规病理切片——即为每位患者常做的粉紫色组织图像——并准确推断出这些分子亚型,从而有望使精准诊疗更为普及。
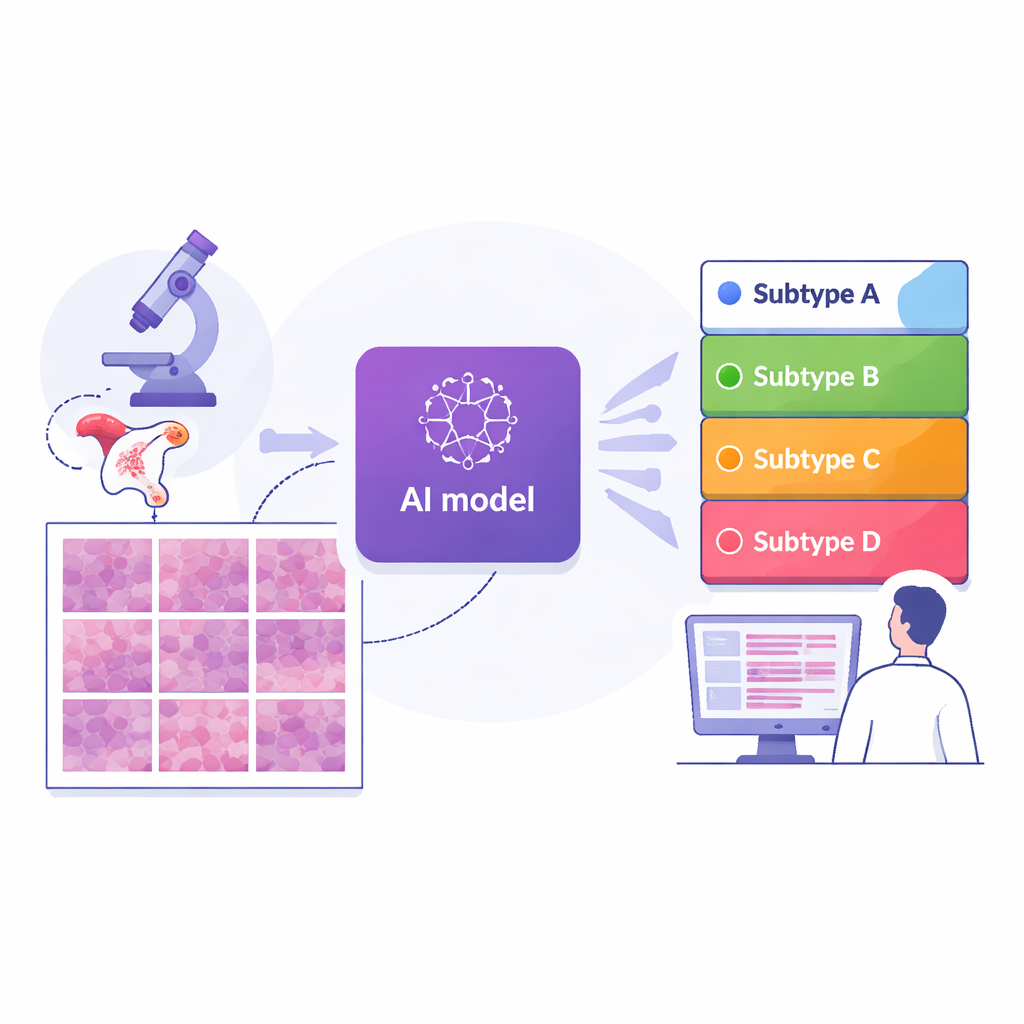
深入观察肿瘤的多样性
并非所有子宫内膜癌的行为都相同。有些生长缓慢且局限于子宫;有些则早期发生转移且更难治疗。现代指南基于DNA变化及细胞修复基因损伤的机制,将这些肿瘤分为四种分子亚型。这些类别有助于预测预后并指导决策,例如手术范围应多大、患者是否可能受益于免疫治疗。然而,所需的基因检测和特殊染色既昂贵又依赖专家解读,在较小或资源有限的医院常常无法获得。病理学家长期怀疑,许多分子差异会在显微镜下细胞及支持组织的形态上留下可见线索——但这些线索对人眼来说往往太微妙、太复杂,难以始终如一地判断。
教计算机读病理切片
研究者收集了来自上海一所大型癌症中心的324名女性的364张数字化切片图像,并采用了两组独立的对照:一组为国际公共数据集中的296张切片,另一组为苏州另一家医院的36张切片。每例均已通过先进的基因检测归类为四种分子亚型之一。研究团队将每张整片图像切分为数千个小瓷砖(tile),并训练了一种用于图像识别的深度学习模型,让它逐瓷砖地评估该区域属于各亚型的可能性。通过对整张切片上各瓷砖的预测取平均,系统为每位患者生成单一的亚型预测,这一流程与医生从整体上评估肿瘤的思路相呼应。
系统的表现如何
在上海主队列中,该AI达到了较高的准确度:区分四种亚型的总体得分(以一种标准统计量衡量,范围从0.5的随机猜测到1.0的完美分离)约为0.87。在采用来自不同医院和切片扫描系统的两组外部数据上,表现仍然稳健——约为0.84,表明该方法具有一定的泛化能力。与若干使用更复杂注意力机制或池化方案的领先AI策略相比,这个端到端模型(建立在现代图像分析骨干上)总体上表现更好。更重要的是,作者将系统设计为可解释的:他们使用可视化工具高亮显示AI在每个瓷砖上做出判断时依赖的具体区域。
AI在肿瘤微环境中“看到”的内容
为理解哪些特征驱动了预测,团队将AI生成的热图与经典病理学观察以及对单个细胞形状和排列的精细测量相结合。某些亚型的肿瘤在基质中表现出大量免疫细胞浸润,而另一些亚型则倾向于紧密堆积的结构细胞。第三类显示出更多由高度异常肿瘤细胞组成的致密片状结构,与侵袭性行为相关的亚型则表现为乳头状的指状结构和极不规则的细胞核。通过分割并分析大约2.45亿个细胞,研究者量化了细胞大小、变异性和间距等差异,并展示了某些特征组合如何对应特定亚型。这些发现支持了这样的观点:分子差异在组织结构上留下可识别的印记,机器可以系统地检测到这些印记。
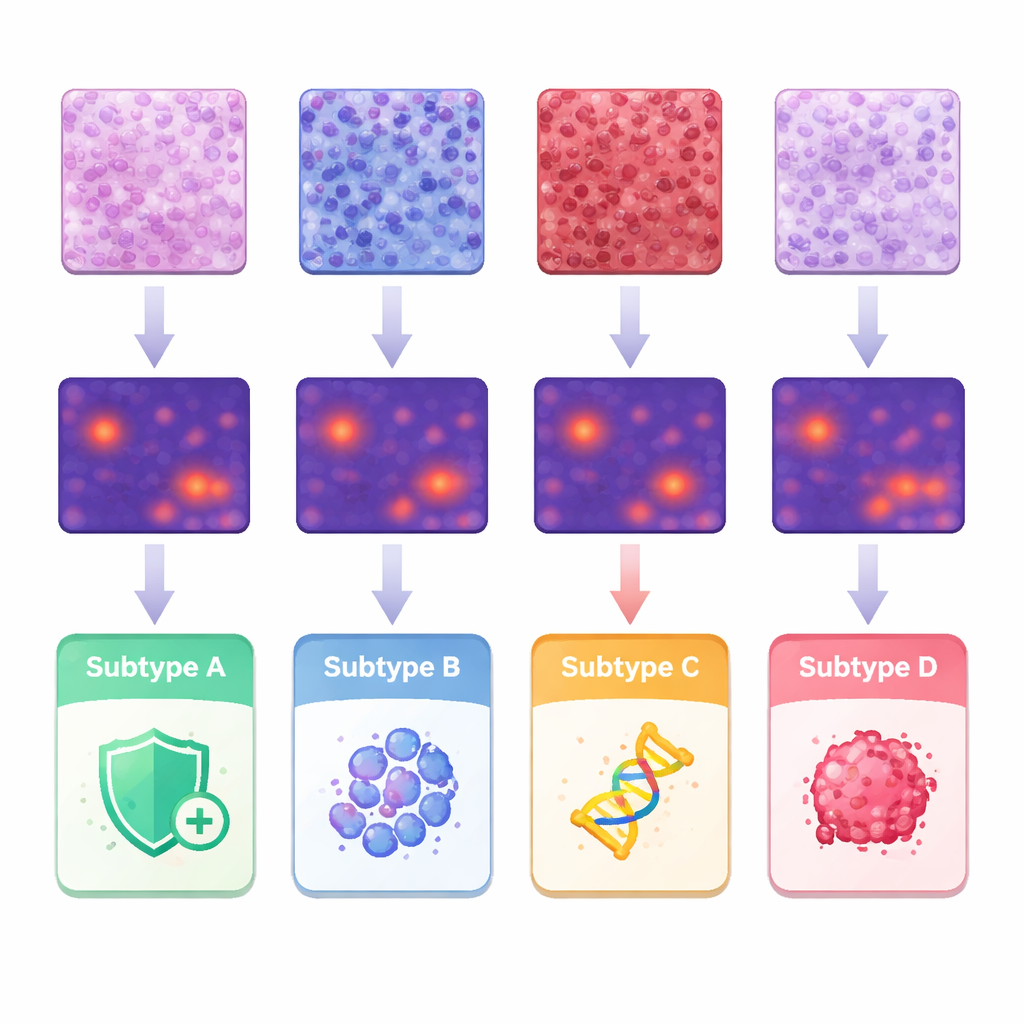
从概念验证到临床辅助
这项工作并不旨在取代基因检测;相反,它提出了一种以苏木精-伊红为首的分流工具,利用每次活检都已制备的标准染色切片。实际上,由AI生成的亚型概率图可帮助病理学家决定先做哪些确认性检测、在有限组织量时优先用于最有信息量的检测,以及加快治疗决策,尤其是在无法获得全面分子分型的医院中。研究也指出了当前的局限,如对最罕见亚型的表现较弱,以及在部署前需要更大、更具多样性的数据集。尽管如此,该研究令人信服地展示了常规显微镜图像中蕴含足够的隐藏信息,使AI能够近似复杂的分子标签,为子宫内膜癌患者提供更公平、数据驱动的护理开辟了道路。
引用: Guo, Q., Cui, H., Zhang, Y. et al. An interpretable deep learning model for predicting endometrial cancer molecular subtypes from H&E-stained slides. npj Precis. Onc. 10, 71 (2026). https://doi.org/10.1038/s41698-026-01280-w
关键词: 子宫内膜癌, 数字病理, 深度学习, 分子亚型, 精准肿瘤学