Clear Sky Science · zh
TheraMind:一种多LLM 集成系统,通过病例报告挖掘加速肺癌药物再利用
这对患者和医生为何重要
对于晚期肺癌患者而言,时间宝贵且可用治疗选项常常很快耗尽。开发全新药物可能需要十多年,而关于有帮助疗法的零散线索可能已经隐匿在已发表的患者病例报告中。本文介绍了 TheraMind——一种人工智能系统,它梳理数千篇病例报告,以发现可能安全再利用、能帮助难治性肺癌患者的现有药物。
为旧药寻找新用途的挑战
非小细胞肺癌是全球致死率最高的癌症,一旦疾病扩散存活率仍然很低。从零开始发现和测试新药既慢又昂贵且风险高。相比之下,“再利用”药物已被批准用于其他疾病,因此其安全性更为了解。临床肿瘤医师对这类药物感兴趣,尤其是对已耗尽标准治疗的患者,但他们需要真实世界的证据,证明某种药物确实帮助过肺癌患者——而不仅仅是有前景的实验室数据。这些临床线索常常出现在散落于医学文献深处的单个病例报告中,手工查找既困难又耗时。
一个能阅读数千篇患者故事的数字化读者
研究人员构建了 TheraMind,作为病例报告的孜孜不倦且谨慎的读者。从先前基因组和实验室研究建议的 18 个药物候选开始,系统自动从 PubMed(最大的医学文章数据库)提取了 10,023 篇病例报告。然后将每篇报告的文本分别输入三种不同的语言模型——这些模型是经过训练以理解医学写作的独立“读者”。对于每篇报告,模型回答相同的四个简单问题:患者是否被描述为患有非小细胞肺癌?研究用药是否专门用于治疗该病?治疗是否提前终止?以及患者是否出现了良好的临床结局?
AI 团队如何达成共同决定
当 TheraMind 将每篇报告转化为一组是/否答案后,多层决策机制开始发挥作用。一种方法使用手工设计的决策树,要求所有四个条件都满足,才将该病例判定为与药物再利用相关。另一种方法允许单一模型更灵活地权衡证据,既考虑是/否答案也考虑其生成的简短解释。最强的方法结合了三个基于不同模型的分类器,只有当三者中至少两者一致认为相关时才接受该报告。这种“多数投票”方法有助于抵消个别错误,类似于让几位独立医生共同审阅同一病历。
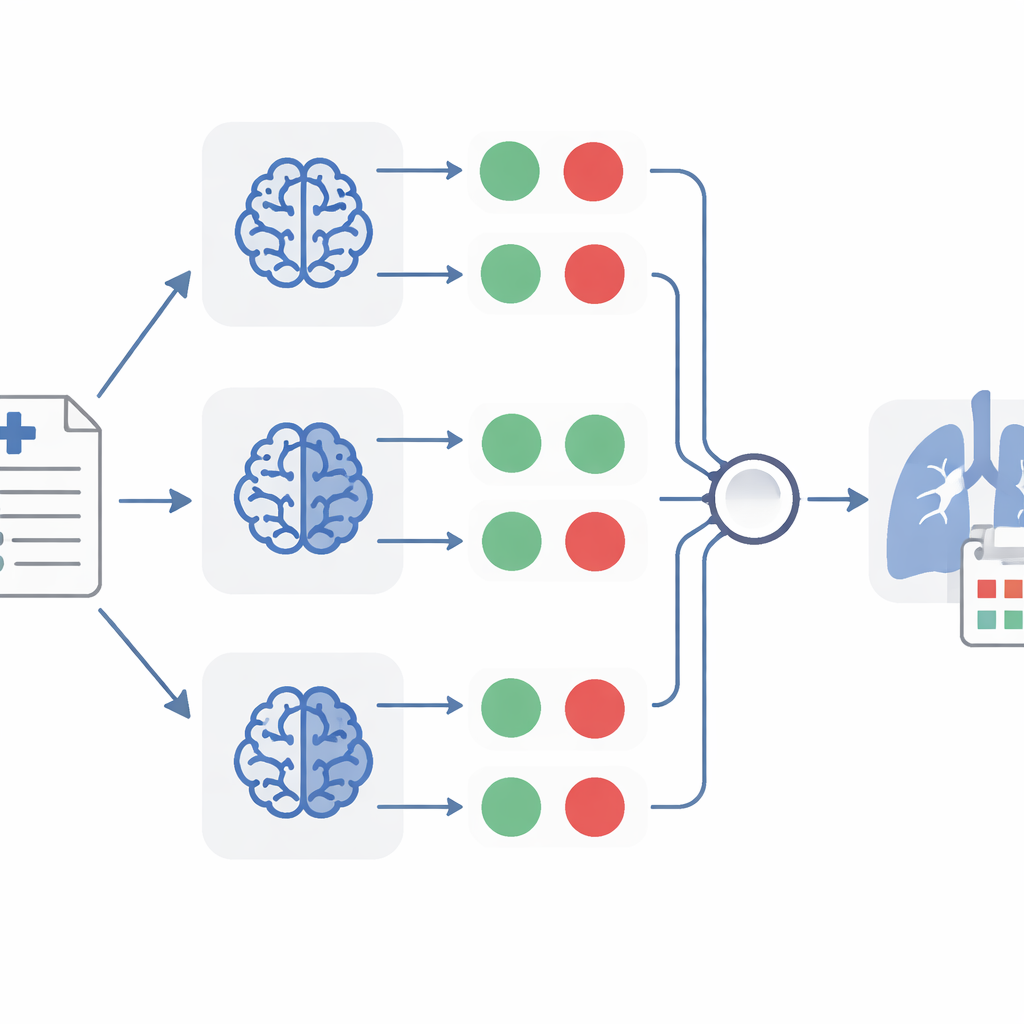
TheraMind 在肺癌病例报告中的发现
将 TheraMind 应用于大量病例报告后,系统标注出 26 篇强烈支持在非小细胞肺癌中使用十种不同药物的报告。该集成方法达到了约 92% 的召回率,意味着它捕获了几乎所有真正相关的报告,同时保持了 99.7% 的高度特异性,因此很少有不相关的报告被误判。对于每篇被选中的报告,系统还将关键的患者信息(例如年龄、性别、病史、病情和可疑药物)提取为一致的数据格式,并生成该病例的简短明白摘要。具有生物学和计算机科学背景的人类审阅者检查了这些输出,并确认其中一个模型特别在提取准确性和完整性方面表现优异。
超越肺癌并迈向临床
为测试系统的灵活性,团队还将 TheraMind 应用于乳腺癌和他们先前研究中识别的若干候选药物。在该情境下,系统没有报告匹配的病例报告,准确反映了现有科学记录而非捏造证据。作者认为,这种结合规则化逻辑与多位 AI 读者的结构化、透明流程,有助于缩小实验室发现与可供临床试验的治疗之间的差距。他们强调将类似方法应用于其他癌种的前景,同时指出若未来版本直接连接电子健康记录,则需谨慎处理患者隐私问题。
这对未来治疗的意义
通俗地说,TheraMind 将零散、非结构化的患者故事转化为医生和研究人员可以采取行动的有组织证据。通过快速筛出现有药物似乎对肺癌患者有帮助的报告,它可以指导哪些再利用药物值得在临床试验中进一步研究。虽然它不能替代医学判断,但这个多模型 AI 读者为在海量医学文本中筛选出简短且可信的、有前景的治疗选项清单,提供了一条可行路径,帮助那些迫切需要新选择的患者。
引用: More, V., Lu, L., Ding, Z. et al. TheraMind: a multi-LLM ensemble for accelerating drug repurposing in lung cancer via case report mining. npj Precis. Onc. 10, 95 (2026). https://doi.org/10.1038/s41698-025-01265-1
关键词: 药物再利用, 肺癌, 病例报告, 大型语言模型, 临床证据挖掘