Clear Sky Science · zh
破译上皮性卵巢癌脑转移:多模态分析与潜在生物标志物
这项研究为何重要
卵巢癌本身就是一种危险疾病,但在少数女性中,它后来会出现在更为脆弱的部位:大脑。尽管脑转移罕见,却常常致命,医生目前仍缺乏有效手段预测哪些人将面临风险或应采取何种最佳治疗。该研究在分子层面上追踪了从盆腔到大脑的演变,采用现代的DNA和RNA工具来理解卵巢肿瘤如何适应大脑环境,并识别可能在未来为个体化治疗提供预警信号的分子标志。
从常见癌症到罕见的脑部威胁
上皮性卵巢癌是发达国家致死率最高的妇科恶性肿瘤。大多数患者在手术和化疗后最初有反应,但约80%的患者最终会出现疾病复发并对药物产生耐药性。复发通常局限于腹腔内,只有少部分女性出现远处转移,如转移至大脑。随着治疗改进、患者生存期延长,癌细胞有更多时间播散到大脑,临床上这类转移病例也有所增多。一旦出现脑转移,典型生存期降至不足一年,凸显出理解其发生机制的紧迫性。
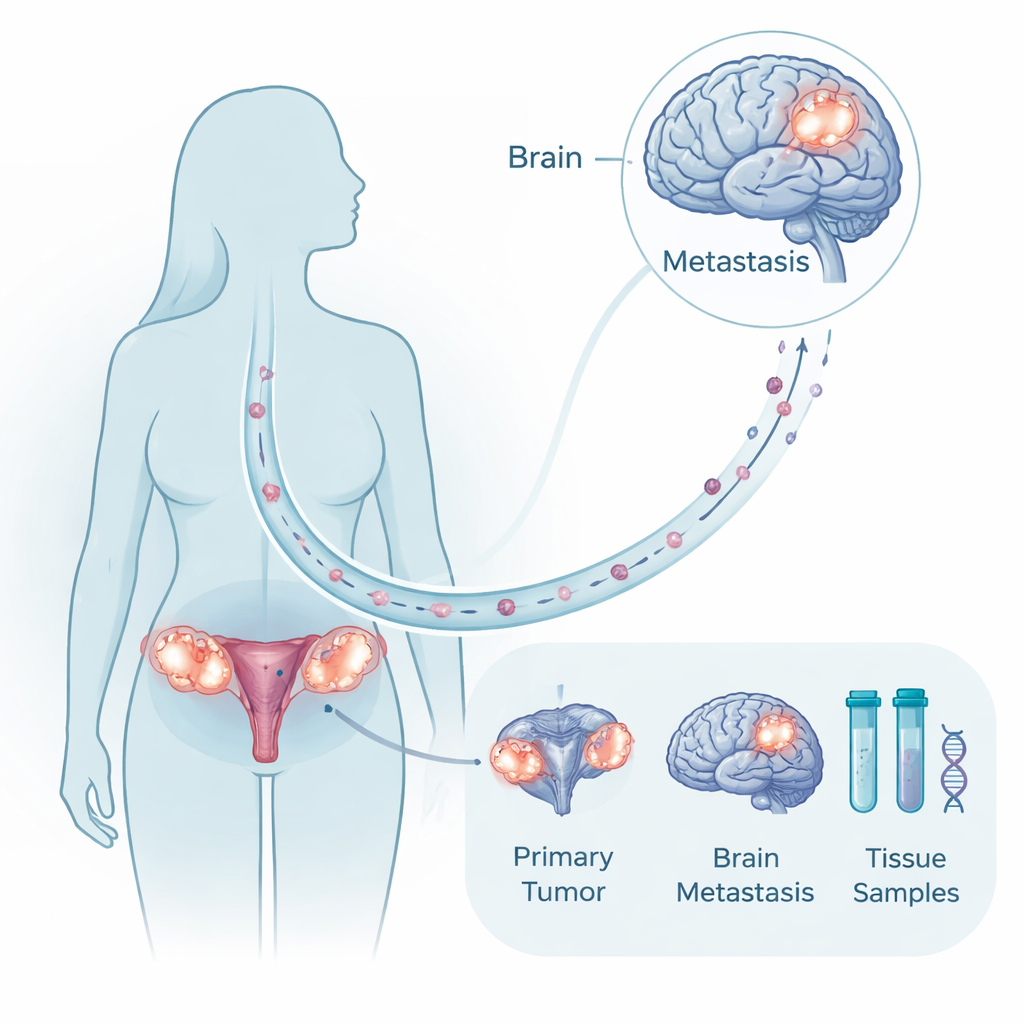
稀有但重要的组织样本收集
由于许多患者不适合或无法接受脑外科手术,能同时获得同一患者原发卵巢肿瘤及其配对脑转移灶的样本并不常见。研究者收集了来自十名患者、历时二十年的这种配对样本,并辅以健康脑与卵巢组织以及其他非脑转移的比较样本。他们分析了肿瘤的DNA以寻找突变和大范围染色体变动,并对RNA进行谱系分析以观察基因的开闭状态。这种多模态方法使他们能够探问脑转移灶是全新分支还是与原发肿瘤密切相关的“近亲”,以及细胞在扎根于大脑时发生了哪些分子层面的改变。
遗传学相对稳定,但行为发生新变化
DNA分析显示,原发卵巢肿瘤与匹配的脑转移灶在很大程度上非常相似。两者携带许多相同的致癌驱动突变,尤其是在TP53基因中,并具有总体上的“单克隆”起源,这意味着脑灶似乎来自同一祖先癌细胞。大尺度的DNA增益和缺失在脑灶中略为常见,但并不显著压倒性。这提示并非完全新的一组突变使肿瘤获得在脑中播散的能力。关键的变化更可能出现在基因活性层面:即哪些遗传指令被读取并为癌细胞所用,以适应大脑独特的微环境。
卵巢肿瘤如何学会在大脑生存
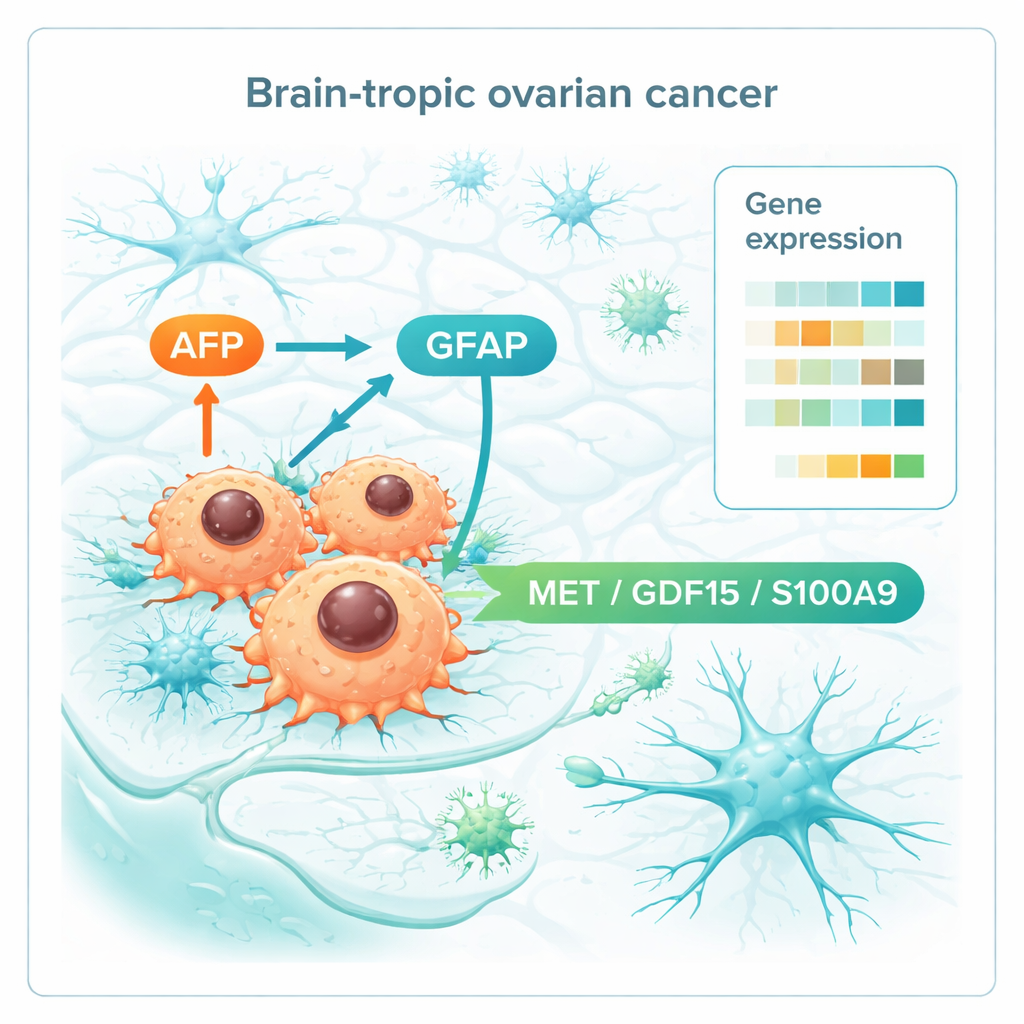
当团队比较所有组织的基因活性时,出现了一个明显的脑转移特征。脑灶显示出侵袭性生长的迹象,细胞周期程序被激活,这些程序由MYC和E2F等已知癌症调控因子驱动。它们还改变了构建和重塑组织支架的蛋白,帮助细胞在脑组织中侵入并固定。令人瞩目的是,一些与神经和胶质细胞相关的基因被激活,暗示卵巢癌细胞部分模仿脑细胞以便融入。其中比较显著的有AFP(通常在胎儿和某些肿瘤中活跃)和GFAP(脑支持细胞的标志性蛋白)。作者还鉴别出一小组在原发卵巢肿瘤中即已升高、但在长期无脑转移的幸存者中并不升高的基因,这种“前转移”模式涉及免疫调节、与类似神经信号的通讯以及代谢变化。
早期预警信号与分子间的对话
深入挖掘后,研究者将注意力集中在位于细胞表面或被分泌的分子上,因为这些分子是血液检测或药物靶点的首选候选者。他们锁定了三种在原发肿瘤(注定要发生脑转移者)和脑转移灶中均持续升高的分子——MET、GDF15和S100A9。这些分子参与细胞迁移、应激与营养感知以及塑造免疫环境,表明它们可能帮助卵巢癌细胞与大脑组织“对话”并将其重塑以利于肿瘤生长。连同AFP和GFAP,这些分子构成了一份潜在的生物标志物清单,未来可能用于识别高风险患者或指明可干预肿瘤——大脑通讯的药物方向。
对患者意味着什么
目前,这项工作不会立即改变临床治疗,且作者也承认其患者群体规模较小。然而,通过展示脑转移性卵巢癌在保留大部分原有基因构成的同时重塑基因使用方式,研究强调了早期发现问题的新途径。如果未来研究证实AFP、GFAP、MET、GDF15和S100A9等标志物能够可靠地提示向大脑播散的倾向,临床医生或可对特定患者进行更密切监测、调整治疗选择,或尝试阻断这些通路的药物。本质上,研究开始将这一令人畏惧的晚期并发症转化为可测量、可理解并最终可拦截的过程。
引用: Trozzi, R., Salvi, M., Karimi, M. et al. Deciphering brain metastasis in epithelial ovarian cancer: multimodal analysis and potential biomarkers. npj Precis. Onc. 10, 83 (2026). https://doi.org/10.1038/s41698-025-01206-y
关键词: 卵巢癌, 脑转移, 生物标志物, 基因表达, 精准肿瘤学