Clear Sky Science · zh
脂肪细胞驱动的 STAT3-ANGPT2-PTGIS 轴促进乳腺癌皮肤转移并构成可靶向通路
为什么乳腺癌在皮肤扩散很重要
当乳腺癌发生转移时,大多数人会想到骨、肝或肺。然而,对许多患者来说,癌症会在一个意想不到的部位复发:胸壁皮肤,有时是在原发肿瘤切除多年之后。这些顽固且疼痛的皮肤结节不仅是一个美容问题——它们是难治性侵袭性疾病的标志。本研究探究了为何某些乳腺癌偏好皮肤,揭示了癌细胞、邻近脂肪组织及供应肿瘤的血管和淋巴管之间一种令人意外的协同关系。
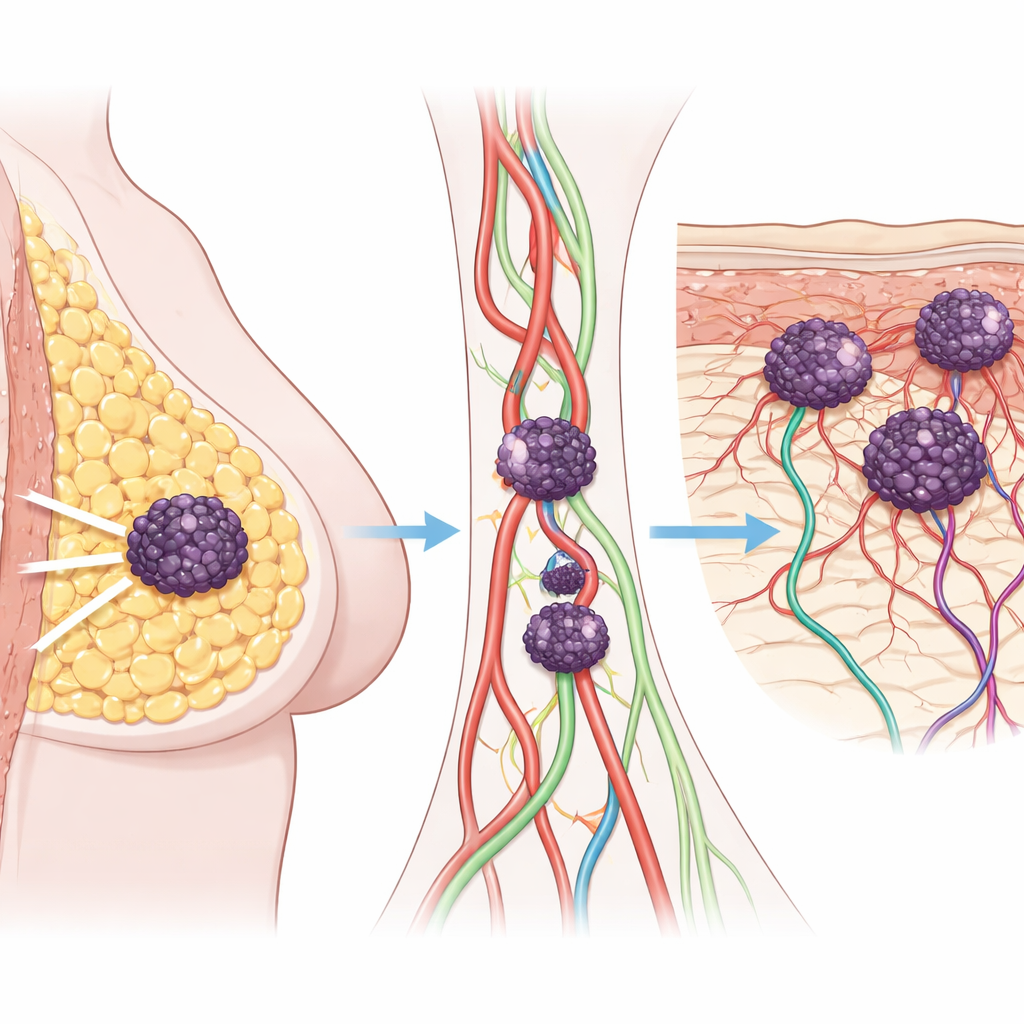
皮肤肿瘤作为一种警示信号
研究者首先审查了126例乳腺癌患者的病历,比较了那些未复发的患者、癌症转移到肺或骨等器官的患者,以及出现皮肤转移的患者。仅在皮肤出现复发的患者在诊断时已表现出更晚期且生长更快的肿瘤。其肿瘤显示出较高的细胞分裂速率和对血管与淋巴管的早期侵袭。尽管这些患者中有些人在影像学上没有发现远处器官转移,但其总体生存期和无病生存期均逊于无皮肤受累的患者,强调皮肤转移标志着一种特别侵袭性的乳腺癌类型。
血管与脂肪塑造皮肤生态位
为了解皮肤为何成为如此有利的土壤,研究团队随访了一位患者数年,收集了原发乳腺肿瘤及随后皮肤结节的样本。在显微镜下,乳腺和皮肤病灶均充斥新生的血管和淋巴管——这些微小通道帮助癌细胞迁移并扎根。基因表达谱分析显示,随着疾病进展,肿瘤启用了与血管生长、炎症以及脂类和脂肪酸处理相关的整套网络。尤其是分解常见膳食脂肪(如花生四烯酸和亚油酸)的通路变得更为活跃,提示来自脂肪的能量以及皮肤自身的脂肪层有助于推动肿瘤演化。
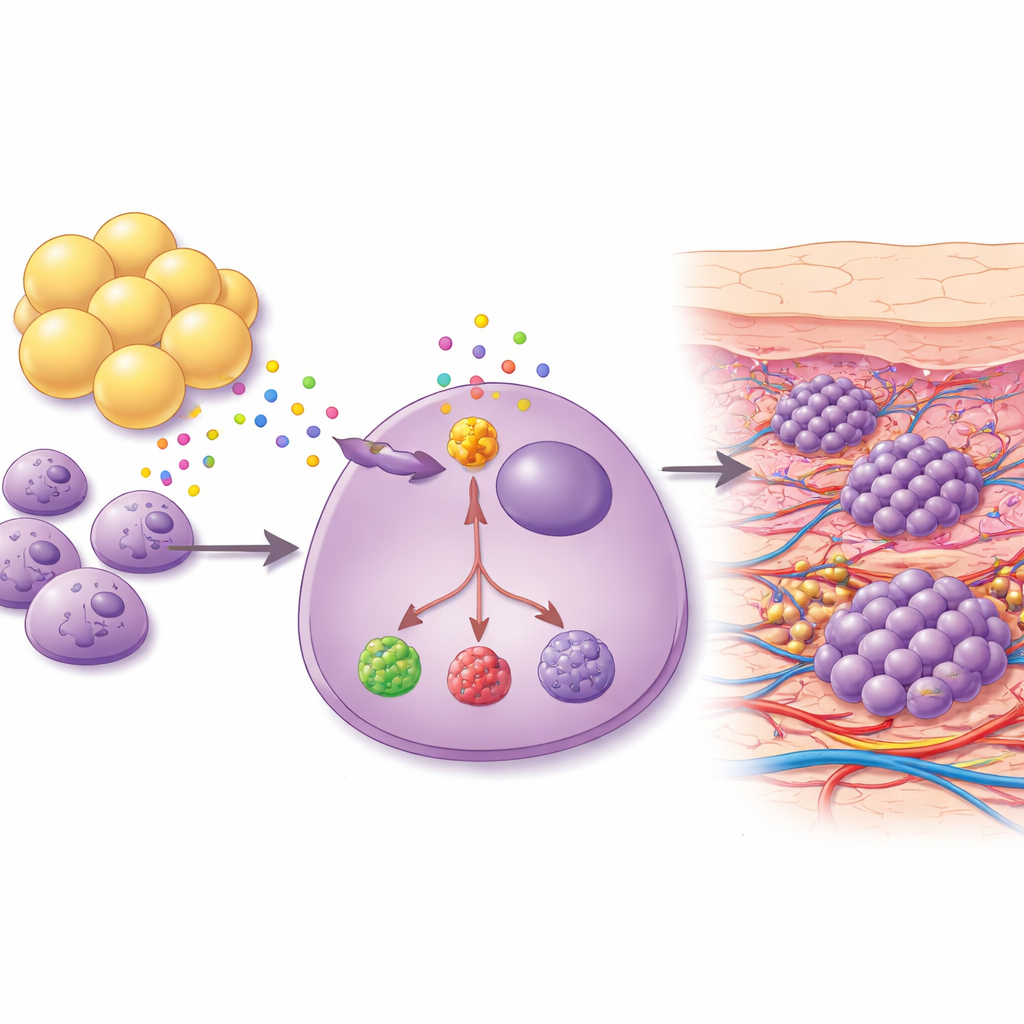
脂肪细胞发出强有力的生长信号
由于乳房及其下方胸壁富含脂肪,科学家们探究脂肪细胞本身是否会诱导癌细胞趋向皮肤。他们将来自同一患者的乳腺癌细胞与成熟脂肪细胞(脂肪细胞)共同培养,并收集脂肪细胞释放的混合分子组分。这种“鸡尾酒”显著增强了血管内皮细胞在体外形成管状结构的能力,这是血管生成的标志。在小鼠模型中,暴露于脂肪细胞来源的分泌物会导致在颈部和背部等富含皮肤与脂肪的区域出现新的肿瘤生长。从这些皮肤病灶分离的癌细胞更具干样特性、更抗凋亡,并产生更高水平的促生长和促炎因子,包括一种名为 ANGPT2 的蛋白和一种名为 PTGIS 的代谢酶。
可被关闭的信号开关
进一步挖掘时,团队比较了普通肿瘤细胞与趋皮性(向皮肤迁移)肿瘤细胞,发现细胞内一条常见的通讯通路——JAK–STAT 通路——被强烈激活,尤其是蛋白 STAT3。STAT3 被激活时像主控开关一样,上调 ANGPT2、VEGFC(淋巴管生长的驱动因子)和 PTGIS,这些因子共同促进血管形成并重塑肿瘤环境。用一种名为 Stattic 的药物抑制 STAT3 可降低小鼠皮肤肿瘤的生长并降低这些下游因子的水平。在患者肿瘤样本中,STAT3、ANGPT2 与 PTGIS 活性高与更差的无进展生存期和无病生存期相关,这些标志物在转移仅局限于皮肤的患者中特别升高。
这对患者意味着什么
总体而言,这项工作将皮肤转移性乳腺癌描绘为一种独特且危险的亚型,由癌细胞、周围脂肪与供应肿瘤的血管之间的三向相互作用驱动。来自脂肪细胞的信号在癌细胞内激活 STAT3,继而上调 ANGPT2 与 PTGIS 并重塑脂肪酸代谢,使皮肤成为肿瘤可以安顿并扩展的适宜生态位。对患者而言,这意味着皮肤转移并非简单的“局部”复发,而是侵袭性生物学的标志。令人鼓舞的是,驱动这一过程的通路也可能成为其弱点:针对 STAT3 或像 PTGIS 这样的关键代谢酶的药物,未来或可切断支持乳腺癌在皮肤定殖的“补给线”。
引用: Luo, CW., Ou-Yang, F., Chang, SJ. et al. Adipocyte-driven STAT3-ANGPT2-PTGIS axis promotes cutaneous metastasis in breast cancer and represents a targetable pathway. npj Precis. Onc. 10, 111 (2026). https://doi.org/10.1038/s41698-025-01184-1
关键词: 乳腺癌皮肤转移, 肿瘤微环境, 脂肪细胞信号传导, STAT3 通路, 血管生成