Clear Sky Science · zh
PiggyBac介导的转基因与CRISPR–Cas9敲除在大蜡蛾(Galleria mellonella)中的应用
一只小毛毛虫的重大医学潜力
想象一下,在不使用小鼠或其他哺乳动物的情况下测试新抗生素或研究危险感染。大蜡蛾(Galleria mellonella)的幼虫正成为一种低成本、伦理上更可取的替代实验对象。本研究展示了科学家如何迈出重要一步,将那些使果蝇和斑马鱼在生物医学研究中极具价值的遗传工具,同样引入到这种毛毛虫身上。
这类昆虫对人类健康为何重要
Galleria mellonella幼虫在模拟人体对病原体的反应方面出人意料地有效。它们可在37°C(人体温度)下饲养,并能被多种具有医学重要性的细菌和真菌感染。幼虫生病时会通过黑素化(melanization)过程身体变暗,为研究者提供直观的健康读数。作为无脊椎动物,它们避免了许多关于脊椎动物实验的法律和伦理障碍,而且饲养成本低、易于大规模繁殖。研究甚至发现这些幼虫可以分解常见塑料,提示其在环境研究中的潜在用途。
缺失的遗传学工具箱
尽管具有这些优势,蜡蛾幼虫长期缺乏经典实验动物所具备的复杂遗传操作手段。过去十年里,多个团队解读了该蛾的基因组并编目了其表达的基因和蛋白,但研究人员仍然难以方便地开启或关闭基因或加入有用的标记。这一空白限制了该模型的应用——例如无法构建在感染时发光的个体,或删除特定基因以测试其对免疫的影响。本文正面应对这一问题,将两种强大的基因工程系统PiggyBac和CRISPR–Cas9改造并用于Galleria mellonella。
构建会发光的报告幼虫
研究团队首先研究了蛾胚早期发育的时序,发现在产卵后约六小时的窗口期内,所有分裂的细胞核仍共享共同的细胞质。在此期间注入DNA可使新遗传物质被携带到后续所有组织,包括未来的精子和卵子。利用这一窗口,研究者引入了基于PiggyBac转座子的DNA构建体——一种可将较大DNA片段插入基因组的“剪切-粘贴”元件。通过测试不同的辅助质粒,他们找到了携带高活性PiggyBac酶的版本,成功建立了转基因系。这些幼虫在不同组织中表达出绿色和红色荧光蛋白,DNA分析显示该遗传盒插入在本土基因之间的无害区段。
观察细胞与基因敲除
接着,作者构建了更专用的报告系。一个构建将结构蛋白微管蛋白(tubulin)标记为绿色荧光以突显细胞内部骨架,另一个则将红色标记融合到缠绕细胞核中DNA的组蛋白上。这些系在肠道、脂肪体、丝腺等组织中呈现出特征性的荧光模式,允许研究者在活体或固定幼虫中可视化细胞结构。为了不仅是添加基因而是真正使其失活,团队使用了CRISPR–Cas9。他们将预组装的CRISPR蛋白–RNA复合体注入已经携带报告盒的胚胎,靶向绿色荧光标记。许多后代显示出绿色信号部分或完全丧失,而红色眼部荧光仍保留,DNA测序证实在预定的CRISPR切割位点出现了小的插入和缺失(indel)。
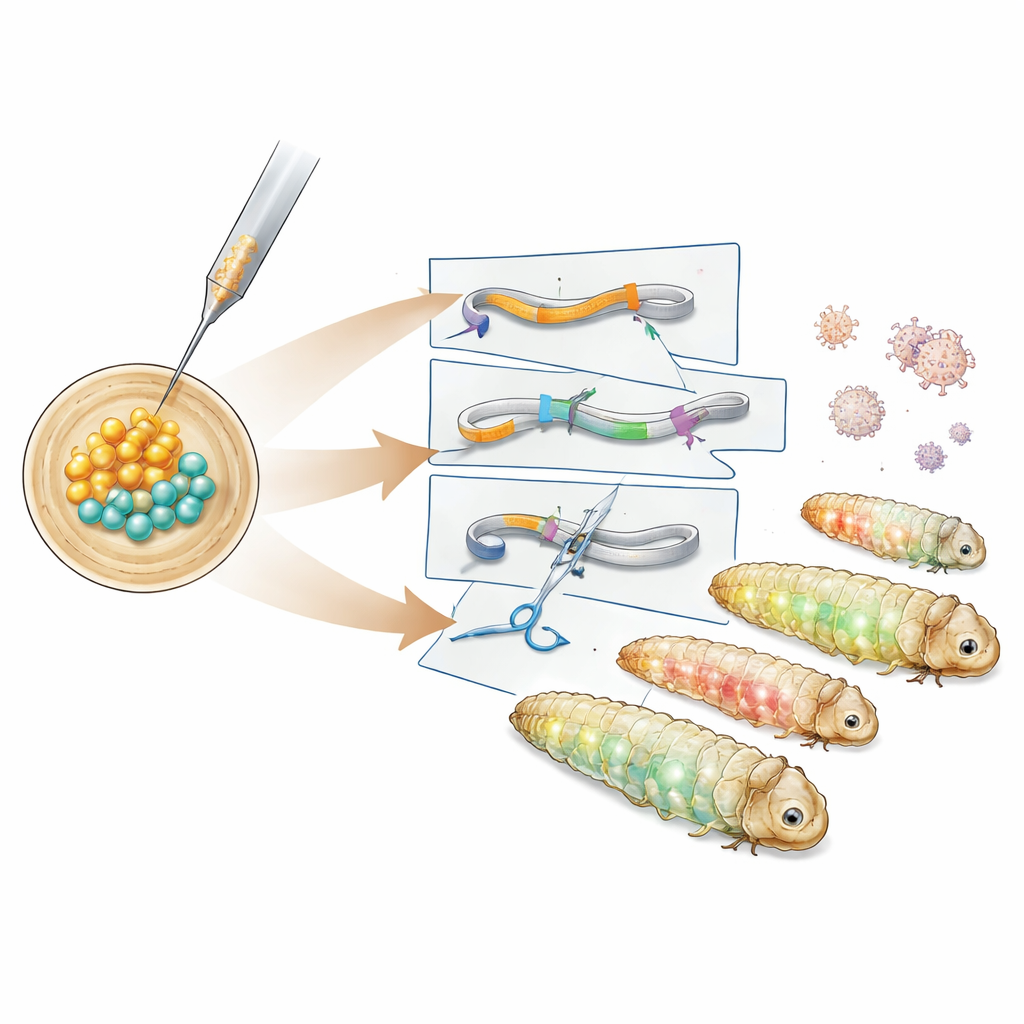
从技术进步到实际影响
尽管在这些蛾中PiggyBac和CRISPR的效率相较某些其他昆虫仍属中等,作者提出了通过优化启动子、酶的变体和注射策略等途径明确改进的方法。即便在目前阶段,该工具箱已足够强大,可用来生成稳定的系来可视化关键细胞成分或携带目标基因敲除。对非专业人士而言,核心结论是Galleria mellonella现在几乎可以像那些更知名的实验动物一样灵活地进行基因工程。这意味着研究者可以构建在感染时做出报告的毛毛虫、模拟人类疾病的某些方面,或以更快、更廉价且更人道的方式测试新药,从而有可能减少感染生物学及相关领域对哺乳动物模型的依赖。
引用: Pearce, J.C., Campbell, J.S., Prior, J.L. et al. PiggyBac-mediated transgenesis and CRISPR–Cas9 knockout in the greater wax moth, Galleria mellonella. Lab Anim 55, 95–102 (2026). https://doi.org/10.1038/s41684-025-01665-7
关键词: Galleria mellonella, 无脊椎动物感染模型, 基因工程, PiggyBac转基因, CRISPR敲除