Clear Sky Science · zh
用人源化单克隆抗体靶向癌细胞表达的EGFR
发现癌细胞的隐蔽标记
癌症治疗常在攻击肿瘤细胞与保护健康组织之间难以取得平衡。本文描述了一种新的人为设计的抗体,称为A10,能够将携带某种形式生长因子受体的癌细胞与正常细胞区分开来。A10识别的构象主要在受体发生改变或在肿瘤细胞上过度表达时出现,这为既强效又比许多现有方案更具选择性的疗法打开了可能性。
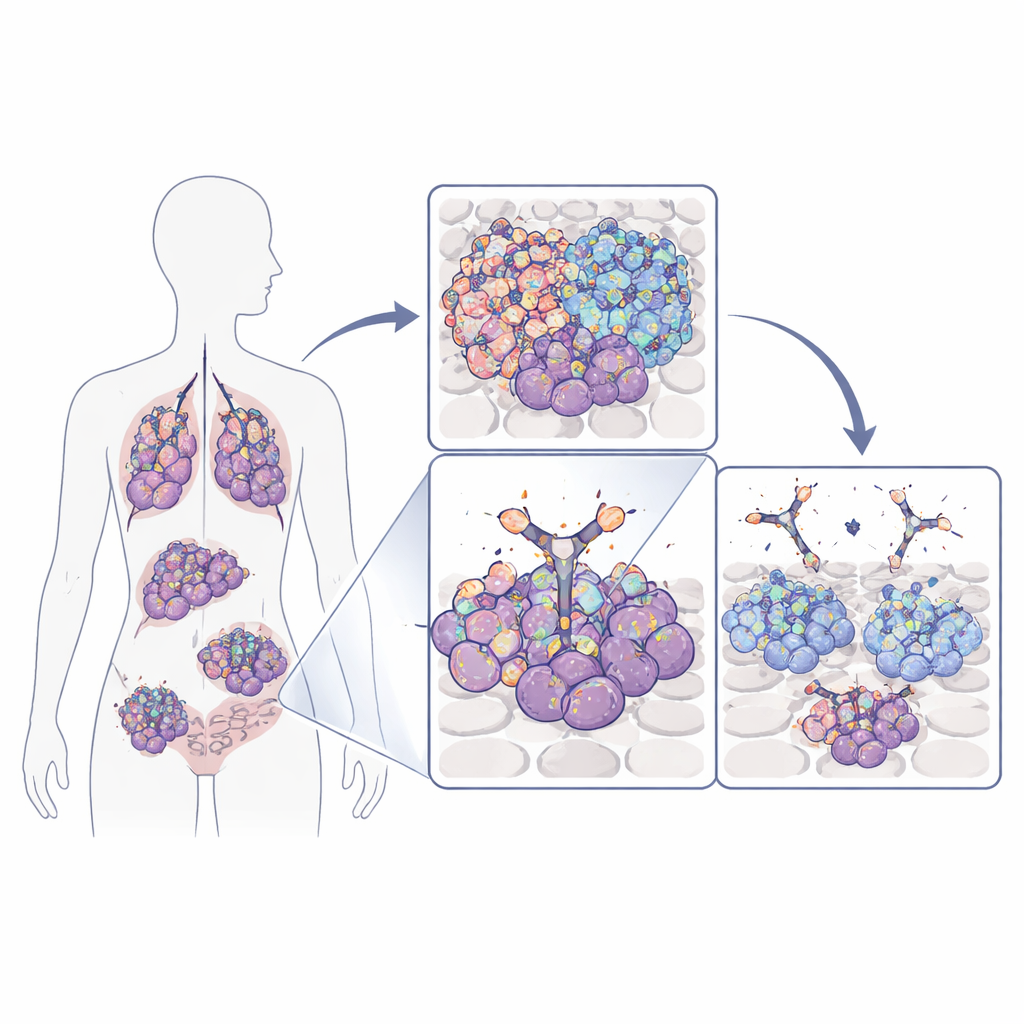
为何这一生长开关至关重要
许多肿瘤——包括侵袭性的大脑、肺、乳腺和结直肠癌——依赖一种称为表皮生长因子受体(EGFR)的表面蛋白来生长和存活。肿瘤细胞可以通过扩增其基因、发生突变或产生一种截短且持续激活的变体(称为EGFRvIII)来增加该受体的活性。标准的EGFR抑制药物常同时作用于癌细胞和正常组织,因为它们识别的受体部位在各处都存在。本研究团队转而关注EGFR上的一小段环状结构,该结构主要在癌细胞上明显暴露——要么因为EGFR异常高表达,要么因为EGFRvIII使受体截短。该环状结构像一个特异性的“旗帜”,理论上可以更安全地作为靶点。
将小鼠抗体转化为可用于人体的药物
研究人员先前发现了一种小鼠抗体40H3,能识别癌细胞上暴露的该EGFR环。但小鼠抗体在反复给药时可能引发免疫反应。为克服这一问题,团队采用蛋白工程方法,将40H3的关键结合片段嫁接到人源抗体框架上,产生了14个“人源化”候选分子及一个嵌合参考分子。在对过度表达EGFR的癌细胞进行测试时,三种变体结合力特别强,其中一款A10在保持对具有适度EGFR水平的正常细胞无反应的同时,表现出最强的结合力。在一系列具有不同EGFR突变和拷贝数的肿瘤细胞系中,A10始终显示出比原始小鼠抗体更高的结合,并保持对恶性细胞的明显偏好。
观察抗体如何抓握其靶点
为了解A10为何如此选择性,团队解析了抗体活性部位与EGFR环结合的高分辨率三维结构。该环折叠成由二硫键稳定的紧密发卡状,A10在其两臂之间形成的槽中包裹该构象,众多带电接触将其锁定。将此结构与已知的完整EGFR分子构象比较得出关键见解:在正常EGFR的不活跃“缠绕”构象和活性二聚体构象中,该环大多被邻近结构埋藏或部分遮蔽。这意味着A10难以接触到普通、适度表达的受体上的结合位点。相比之下,在癌特异性的EGFRvIII变体中,受体前端缺失,使该环高度暴露且可及。数据表明,A10主要识别EGFR在某些过渡构象中,以及在肿瘤细胞上优先出现的过度拥挤或截短形式。
武装抗体以杀死肿瘤细胞
识别肿瘤特异性标记本身就很有价值,但研究者更进一步,将A10制成抗体-药物偶联体(ADC)。他们通过一个可在细胞内被切断的连接子,将一种强效细胞毒物单甲基奥立司他辛E(MMAE)化学连接到A10上。该A10-MMAE ADC对癌细胞的结合与未偶联的抗体一样好。在多种细胞系的实验室测试中,ADC对那些EGFR水平极高或携带EGFRvIII的肿瘤最为有效——在这些细胞中,A10有大量结合位点,极低剂量的偶联体即可触发细胞死亡。具有较少A10靶点或对MMAE天生耐受的肿瘤系受影响较小,而携带野生型EGFR的正常成纤维细胞尽管对游离MMAE敏感,却未受到伤害。结果显示,选择性结合与内部药物释放的组合可以将毒性明显集中到癌细胞上。
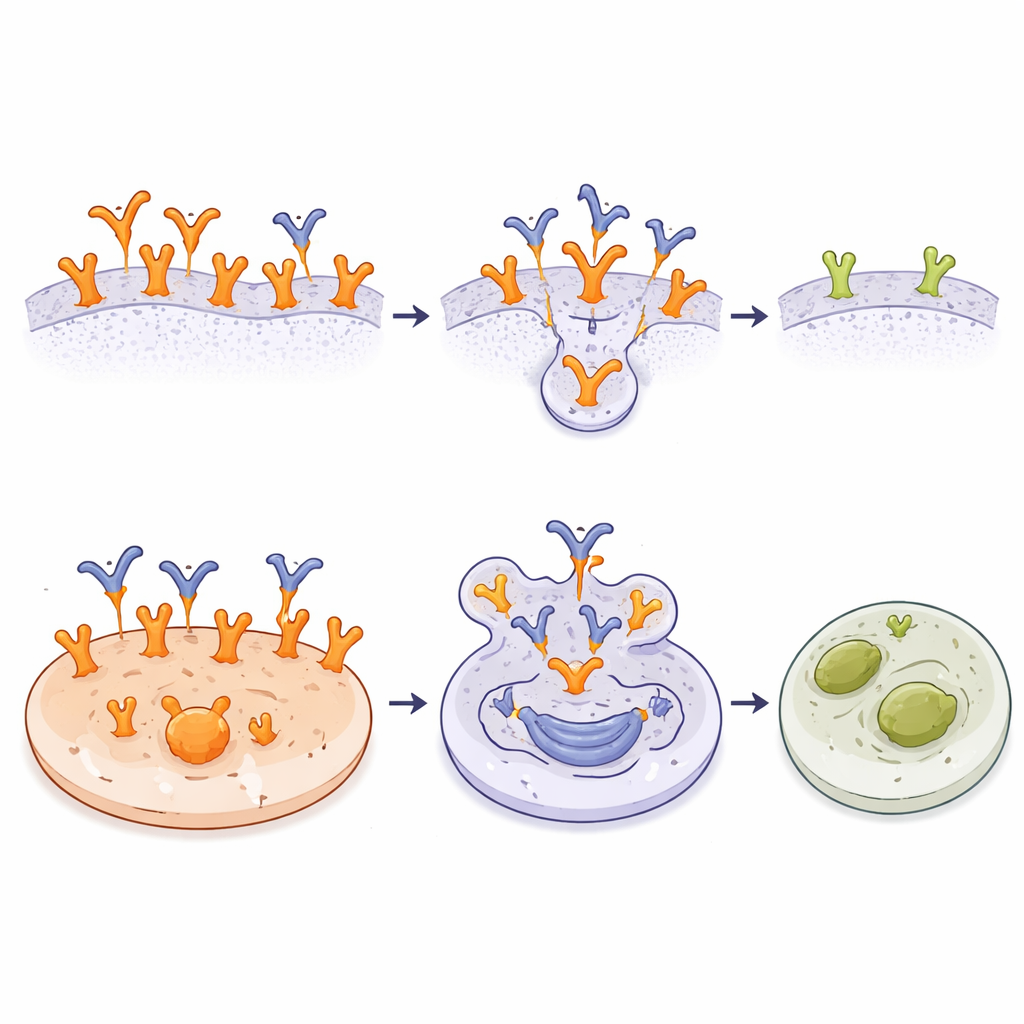
这对未来癌症治疗可能意味着什么
简言之,这项工作表明可以构建出仅在EGFR以类似致癌形式出现时“看见”它的抗体,同时在很大程度上忽略其在健康组织中的日常形态。通过精确描绘A10如何抓握EGFR上的隐蔽环,并证明基于A10的药物偶联体能有效杀死受体丰富的肿瘤细胞而保护正常细胞,该研究为开发更安全、高度靶向的疗法提供了坚实基础。如果这些发现能转化到临床,基于A10的未来治疗可能将强效药物直接送达依赖EGFR的癌症,同时在很大程度上不影响机体其他部位。
引用: Costa, T.G.F., Sarnovsky, R., Zhan, J. et al. Targeting cancer expressed EGFR with a humanized monoclonal antibody. Sci Rep 16, 10814 (2026). https://doi.org/10.1038/s41598-026-46245-y
关键词: EGFR, 抗体药物偶联体, 靶向癌症治疗, 胶质母细胞瘤, EGFRvIII