Clear Sky Science · zh
来自肺癌细胞的生物工程化细胞外囊泡对α2β1和α5β1整合素靶向的结构与机制洞见
癌症的隐秘信使
肺癌常在晚期被发现,此时可供的治疗选择有限。一种有前景的抗癌策略是将药物精确输送到癌细胞,从而保护健康组织。该研究考察了一种微小的天然递送系统——细胞外囊泡(EVs),这是癌细胞用来传递信息的途径。通过用一个短小的靶向标签重新工程化这些囊泡,研究者展示了它们如何附着在肿瘤细胞上的特定对接位点,为更精确、毒性更低的癌症疗法奠定了基础。
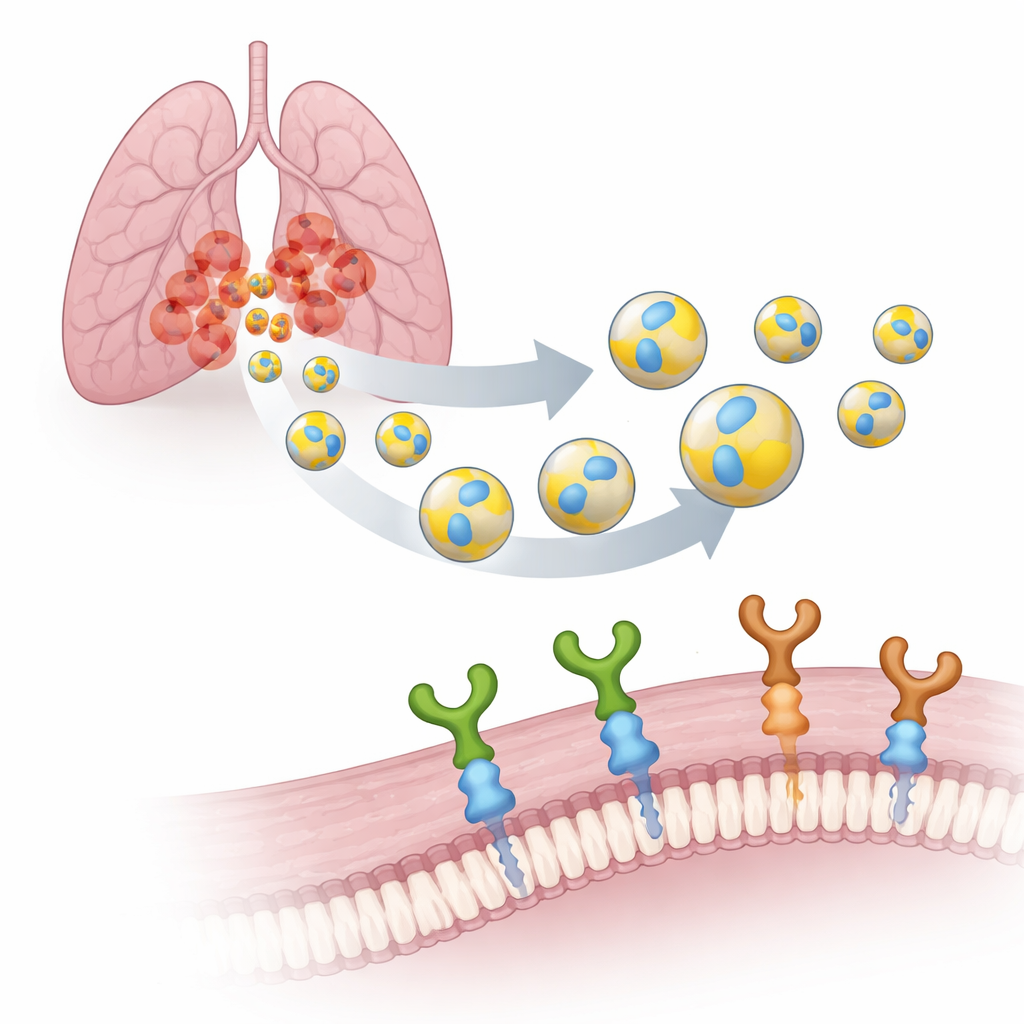
把天然包裹体变成智能快递员
人体内每个细胞都会释放EV:纳米级的囊泡,被膜包围,有点像显微镜下的肥皂泡。因为它们由自身细胞产生,EV可生物降解、易穿透生物屏障,并且比合成载体更不易引起不良反应。团队聚焦于人肺癌(A549)细胞产生的EV,并在其表面修饰了一种由七个残基组成的小标签PTHTRWA。早期实验表明,该标签能驱动EV在小鼠体内定向到肺癌细胞,与肿瘤细胞的结合明显强于正常肺细胞,同时毒性较弱。
在肿瘤细胞上找到合适的对接口
为了将这些带标签的囊泡转化为真正的靶向工具,研究者需要识别癌细胞上它们识别的“端口”。他们考察了两种相关的表面受体:α2β1和α5β1整合素。这些分子如同抓钩,帮助细胞粘附到周围环境并向内传递信号。在肺肿瘤中,α5β1与侵袭性行为、转移和不良生存率密切相关,而α2β1则与化疗耐药性有关。研究团队使用一种灵敏的技术——表面等离子体共振,比较了PTHTRWA修饰的EV与两种整合素的结合强度。结果显示,未带标签的囊泡几乎没有相互作用,而带标签的EV在近生理条件下能与两种受体形成紧密、稳定的复合体。
放大分子层面的拥抱
为了理解标签与整合素相遇时逐原子发生了什么,研究者求助于计算机模拟。他们构建了标签与整合素关键区域结合的三维模型,并在虚拟水环境中让这些体系演化数百纳秒。计算表明,PTHTRWA可紧密契合在α2β1受体的一个浅槽中,形成一系列氢键和疏水相互作用以稳定复合体。关键是,结合更倾向于将受体推向一种“开放”的构象——即高亲和力、易于传递信号的状态——而非“闭合”的静息态。当他们测试对标签稍作化学修饰的变体时,发现末端的微小化学调整能够细微改变肽在槽内的取向,从而影响其对不同整合素的偏好强度。
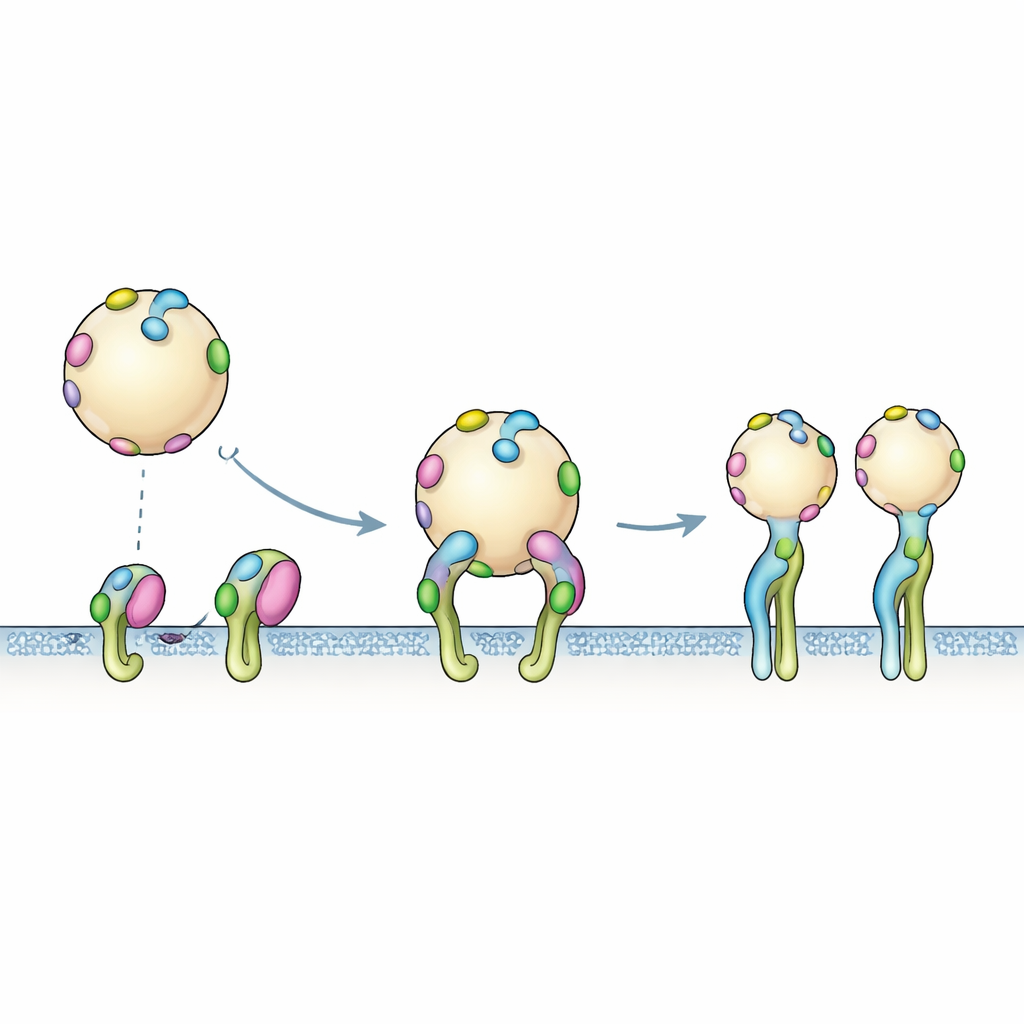
从单一标签到多价握持
计算模型通常描绘单个标签与单个受体的相互作用,但真实的EV表面布满了大量PTHTRWA拷贝。结合实验反映了这种多价现实:当带标签的囊泡接近一片整合素区域时,多个标签可以同时参与结合。传感器数据最适合描述为一个两步过程。首先,囊泡通过快速、可逆的接触短暂对接;随后发生较慢的重排,整合素转变为开放构象,整体结合强度增强。这种协同的、多手抓取解释了整囊泡的表观结合强度为何高于单个标签所能预测的值。
这对未来治疗意味着什么
简而言之,这项研究表明,携带PTHTRWA标签的EV能够选择性识别在肺癌中过度活化的整合素,并通过促使这些受体进入开放且紧密结合的构象来实现识别。通过详尽绘制这些相互作用,研究者为下一代基于囊泡的载体设计提供了规则,能够将药物、成像探针或其他负载直接送达恶性细胞,同时在很大程度上忽略健康组织。尽管仍需更多的动物和临床研究,但这种整合素靶向策略使个性化EV为基础的癌症治疗愿景更进一步。
引用: Nowicka, A.M., Żołek, T., Kowalczyk, A. et al. Structural and mechanistic insights into α2β1 and α5β1 integrin targeting by bioengineered extracellular vesicles originating from lung cancer cells. Sci Rep 16, 10833 (2026). https://doi.org/10.1038/s41598-026-46071-2
关键词: 肺癌, 细胞外囊泡, 整合素, 靶向药物递送, 分子模拟