Clear Sky Science · zh
同位素富集的64Zn-天冬氨酸盐在LPS诱导的大鼠帕金森模型中减轻全身性炎症和肠道失调
这项研究为何关系到日常健康
帕金森病最为人所知的表现是震颤和僵硬,但在这些症状背后存在着全身性的炎症风暴和紊乱的肠道菌群。本研究在大鼠身上探索了一种实验性的锌基治疗,旨在平息这种风暴。通过降低血液中的炎症并恢复更健康的肠道微生物组合,这一方法提示未来可能出现的疗法不仅能掩盖症状,还可能减缓帕金森病进展。
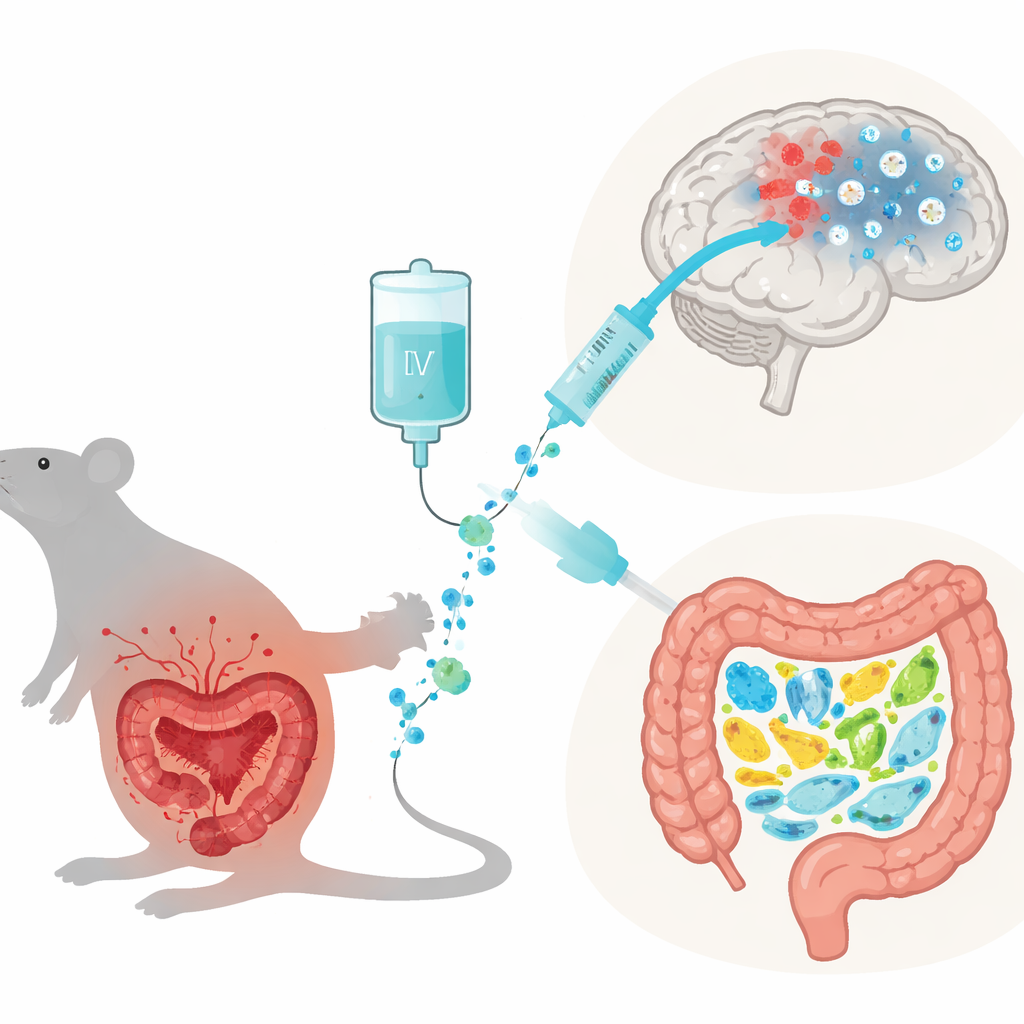
对帕金森病的新角度
多年来,帕金森病主要被视为多巴胺生成神经元的问题,而多巴胺是维持平稳运动所必需的化学物质。研究现在表明,免疫系统和肠道也深度参与其中。脑内的炎症可以渗入血液循环,而体内慢性、低度炎症又可反过来加剧脑内损伤。同时,帕金森病患者常表现出肠道菌群失衡,常见的非运动症状包括便秘和其他消化问题。脑、免疫系统与肠道之间的这种双向交流——有时称为肠-免疫-脑轴——已成为新疗法研究的主要方向。
一种特殊形式的锌进入视野
锌是一种对免疫力、抗氧化防御和大脑功能至关重要的微量矿物质。帕金森病患者往往血锌水平较低,动物研究表明补充锌可能对神经具有保护作用。本研究所测试的化合物是一种实验室制备的形式,称为64Zn-天冬氨酸盐,其中锌与氨基酸天冬氨酸结合,并富集了天然的轻同位素64Zn。该团队早期研究显示,这种形式的锌在类阿尔茨海默病的大鼠模型中可减少炎症和记忆问题,并在帕金森模型中缓解脑部炎症。在本研究中,研究者探究64Zn-天冬氨酸盐是否也能平抑全身炎症并保护炎症驱动型帕金森大鼠的肠道生态。
在大鼠中检验该治疗
为模拟帕金森病的关键特征,研究者将一种名为LPS的细菌片段直接注入控制运动的脑区。这触发了持续性的多巴胺产生细胞丧失、运动障碍和动物的焦虑增加,并伴随显著的全身性炎症标志。一部分帕金森样大鼠随后连续十天接受静脉注射64Zn-天冬氨酸盐。与未治疗的动物相比,接受治疗的大鼠在行为测试中活动更自如,焦虑行为较少,且在使用可揭示多巴胺损伤的药物诱发的异常转向运动减少。这些改变表明运动回路在一定程度上得到保护。
平息免疫风暴
研究团队随后检查了大鼠的血液和免疫细胞。在帕金森样动物中,经典的炎症标志升高:血液中的C反应蛋白增高,粒细胞和血小板过多,淋巴细胞减少,以及一组临床上日益用于评估炎症负担的复合血细胞比率。单核细胞和中性粒细胞等免疫细胞处于高度反应性的促氧化状态,产生大量有害的活性氧。在接受64Zn-天冬氨酸盐治疗后,这些指标大多恢复到健康或假手术对照大鼠的水平。胸腺——免疫细胞成熟的关键器官——也恢复了更正常的大小和细胞构成。总体而言,该药将免疫细胞从破坏性、过度激活的状态推动到更平和、更平衡的表型。
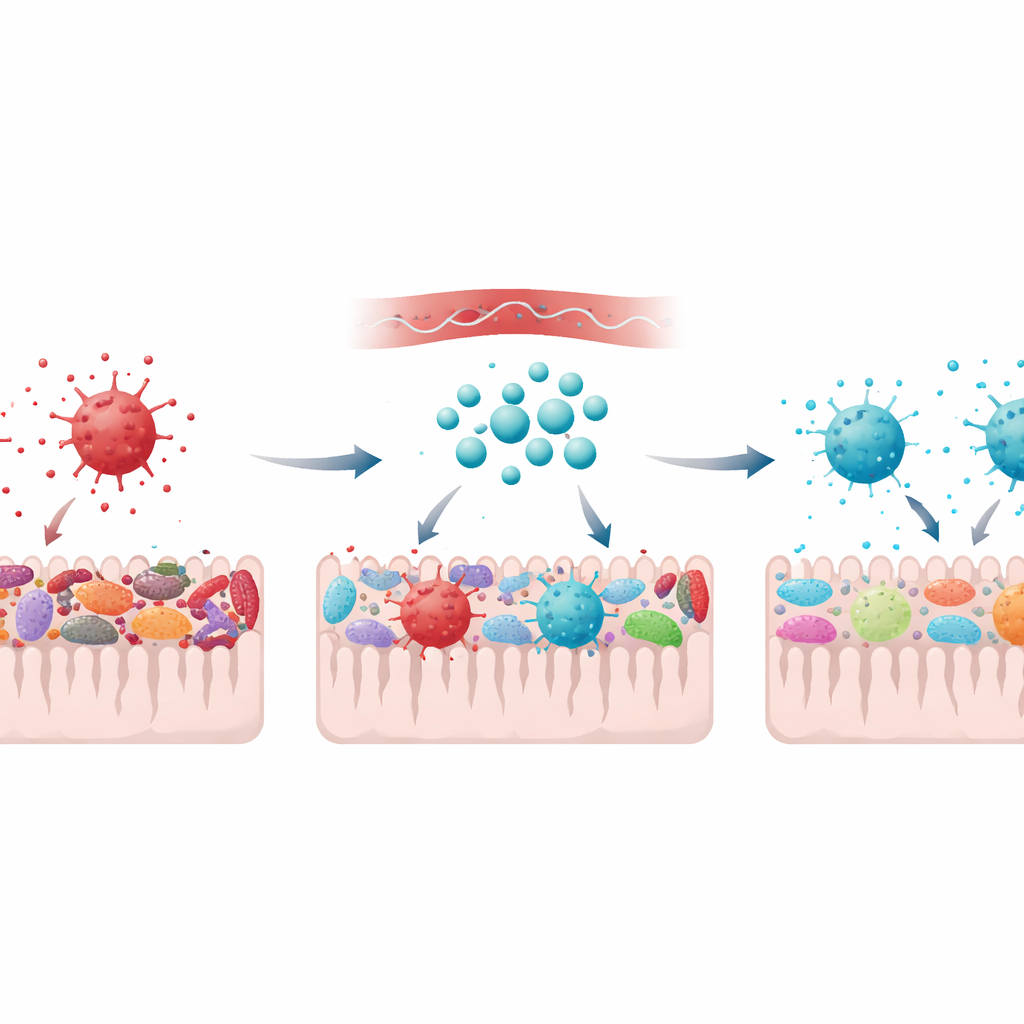
帮助肠道重获平衡
肠道的变化呈现出类似的故事。在帕金森样大鼠中,有益细菌如双歧杆菌和乳酸杆菌——这些菌群帮助分解食物并产生可与神经系统对话的分子——数量减少。与此同时,肠壁黏附的肠杆菌科和葡萄球菌等潜在问题菌群扩大。这一变化暗示肠道环境更富氧并伴有炎症,类似于帕金森患者中观察到的模式。使用64Zn-天冬氨酸盐治疗在很大程度上保留了有益菌,抑制了机会性物种在肠道黏膜和粪便中的扩张。尽管治疗组大鼠的排便量仍略高于对照组,但微生物群落明显更健康。
这对人类可能意味着什么
该研究在大鼠中完成,并不能证明64Zn-天冬氨酸盐在人类帕金森病患者中同样有效。但它提供了有力的概念验证:通过靶向全身性炎症并稳定肠道微生物群,或许可以保护脆弱的脑细胞,并改善运动与情绪。这项研究将这种特殊的锌化合物定位为一类新型疗法的有前景候选者,作用于肠-免疫-脑轴,目标不仅是缓解症状,而是减缓疾病进程本身。
引用: Temnik, M., Rudyk, M., Balakin, A. et al. Isotopically enriched 64ZN-aspartate attenuates systemic inflammation and gut dysbiosis in an LPS-induced rat model of Parkinson’s disease. Sci Rep 16, 10907 (2026). https://doi.org/10.1038/s41598-026-45640-9
关键词: 帕金森病, 全身性炎症, 肠道微生物群, 锌治疗, 神经免疫-肠轴