Clear Sky Science · zh
氟喹啉类化合物通过双靶向GLUT1和PI3K/AKT信号通路发挥抗红细胞白血病作用
从新角度看一种危险的血液癌症
红细胞白血病是一种罕见但高度侵袭性的血液癌症,除干细胞移植外可用的治疗选项有限。对许多主要为老年患者的人群而言,这意味着治疗强度大、费用高且预后不佳。本研究探索了一种实验室设计的化合物FKL-137,它以一种意想不到的方式针对红细胞白血病细胞:切断它们最喜爱的燃料——糖,并诱导其自我毁灭。该工作提示了一类可能的新型靶向药物,利用癌细胞对异常能量使用的依赖性,同时相对保留更多健康组织。
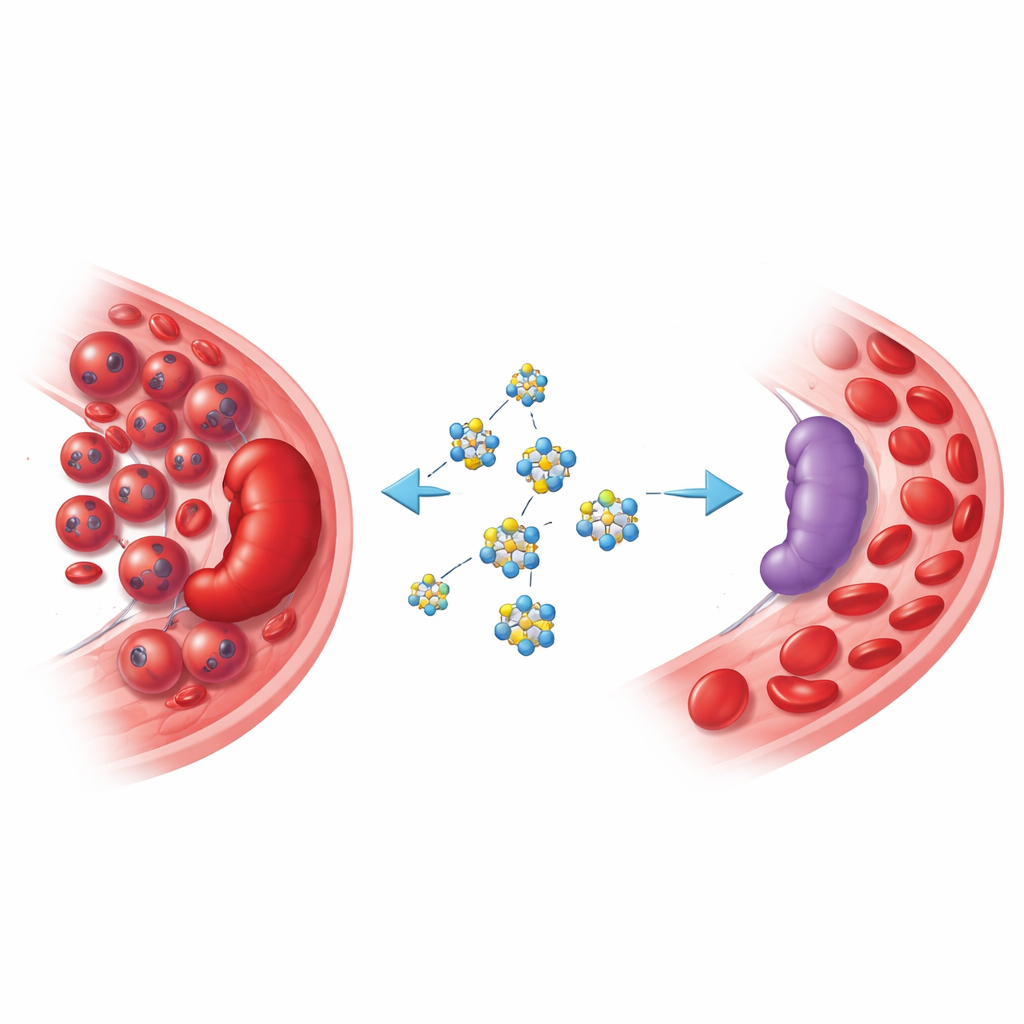
当血细胞失控时
在红细胞白血病中,尚未成熟的红细胞前体在骨髓和脾脏中异常增殖。患者可能出现严重贫血、脾脏肿大并有破裂风险,以及健康状况迅速恶化。目前的疗法有限,许多人因体弱无法承受积极治疗。与此同时,研究人员已发现许多血液肿瘤依赖于重新编程的糖代谢:它们以高速摄取葡萄糖并迅速将其转化为能量和合成所需的构件,帮助肿瘤细胞增殖并逃避免疫系统。针对这种代谢“成瘾”已成为新药开发的一个有吸引力的策略。
让癌细胞“饿死”于糖分
研究者聚焦于一种小分子合成物FKL-137,源自一个已知具有抗癌活性的化学家族。在体外实验中,他们用递增剂量的FKL-137作用于两种人源红细胞白血病细胞系。该化合物随时间显著抑制细胞增殖并促使细胞进入程序性死亡,伴随经典的形态学变化和内在死亡机制的激活。重要的是,FKL-137对白血病细胞的毒性远高于对正常肝细胞的影响,且药物安全性评估显示在有效剂量下毒性相对较低。
打击癌细胞的糖运输通道
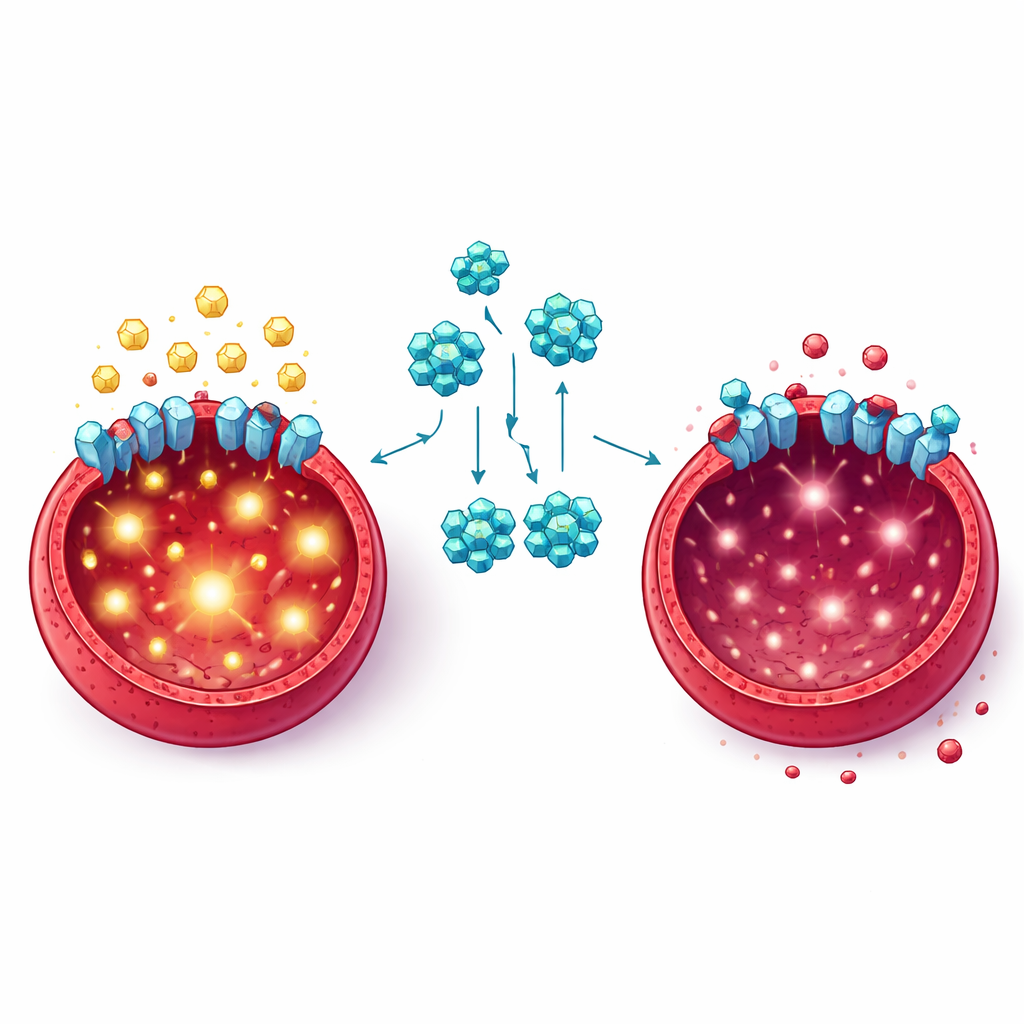
进一步研究中,团队探究了FKL-137如何干扰癌细胞代谢。他们发现被处理的白血病细胞葡萄糖摄取减少,乳酸(一种剧烈糖代谢的代谢产物)释放也减少。通常帮助将葡萄糖转化为能量和合成原料的关键蛋白表达下调。通过计算建模、热稳定性测试和成像,研究者证明FKL-137与GLUT1结合,GLUT1是细胞表面负责摄取葡萄糖的主要“闸门”。当通过基因手段降低GLUT1水平时,白血病细胞增殖变慢、糖代谢降低,并对FKL-137更为敏感。这证实了GLUT1既推动红细胞白血病细胞生长,又是该药物的重要靶点。
破坏生长信号的反馈回路
研究还发现了超出糖运输本身的效应。红细胞白血病细胞通常利用被称为PI3K/AKT的信号途径来促进生存、增长和高糖代谢,部分机制是通过支持GLUT1。FKL-137处理降低了该通路中关键蛋白的活性形式,打破了糖运输与生长信号之间的相互强化回路。在使用一种可靠诱发红细胞白血病的病毒感染的小鼠模型中,FKL-137治疗改善了红细胞水平、缩小了肿大的脾脏、减少了癌细胞向器官的侵袭,并纠正了脾组织中的异常糖代谢——且未见心脏、肝脏、肺或肾脏的明显损伤。
前景、局限与下一步
综上所述,该工作将FKL-137呈现为一种双重作用的候选药物,既阻断了红细胞白血病细胞的主要糖通道,又抑制了依赖该燃料的强力生长通路。通过先让癌细胞“挨饿”再将其推向死亡,该化合物提供了一种概念上优雅的方法,以利用正常细胞没有同等程度共享的弱点。然而,作者也提醒,FKL-137仍需改进:其安全有效窗相对较窄,癌细胞可能通过旁路重编程代谢来补偿,且细胞系与小鼠模型的发现必须在人体组织中得到证实。即便如此,该研究强化了这样一种理念:精确靶向癌细胞的“吃与长”方式,可能为治疗这一难以控制的血液癌症开辟新战线。
引用: Cheng, S., Zhao, W., Yu, J. et al. The fluoroquinoline compound exerts anti-erythroleukemic effects by dual-targeting GLUT1 and the PI3K/AKT signaling pathway. Sci Rep 16, 10916 (2026). https://doi.org/10.1038/s41598-026-45597-9
关键词: 红细胞白血病, 癌症代谢, GLUT1抑制剂, PI3K AKT通路, 靶向治疗