Clear Sky Science · zh
使用弱监督学习对原发性皮肤黑色素瘤的转移风险进行早期检测
这对患者和医生为何重要
皮肤黑色素瘤之所以致命,往往不是因为皮肤上的病灶本身,而是某些肿瘤会悄然扩散到其他器官。如今,医生主要依靠肿瘤的厚度和表面是否破溃来判断哪些患者风险最高。本研究探讨现代人工智能(AI)能否从常规显微镜图像中读出更多信息,更早识别危险肿瘤,特别是在那些表面上看起来仍属较小肿瘤的患者中。
在组织图像中寻找无声的预警信号
研究人员收集了426例原发性皮肤黑色素瘤的标准玻片数字化图像,并附带肿瘤厚度、溃疡、细胞分裂率和肿瘤大小等基本临床资料。大约三成肿瘤后来发生了淋巴结或远处转移,而其余病例在至少三年的随访中未出现转移。研究团队没有请病理学家手工标注特定区域,而是让计算机检查每张切片的所有部分,把每幅大图切成许多小补丁。问题很直接:计算机仅以患者最终是否发生转移为训练标签,能否学会辨认出将高风险肿瘤与低风险肿瘤区分开的视觉模式?
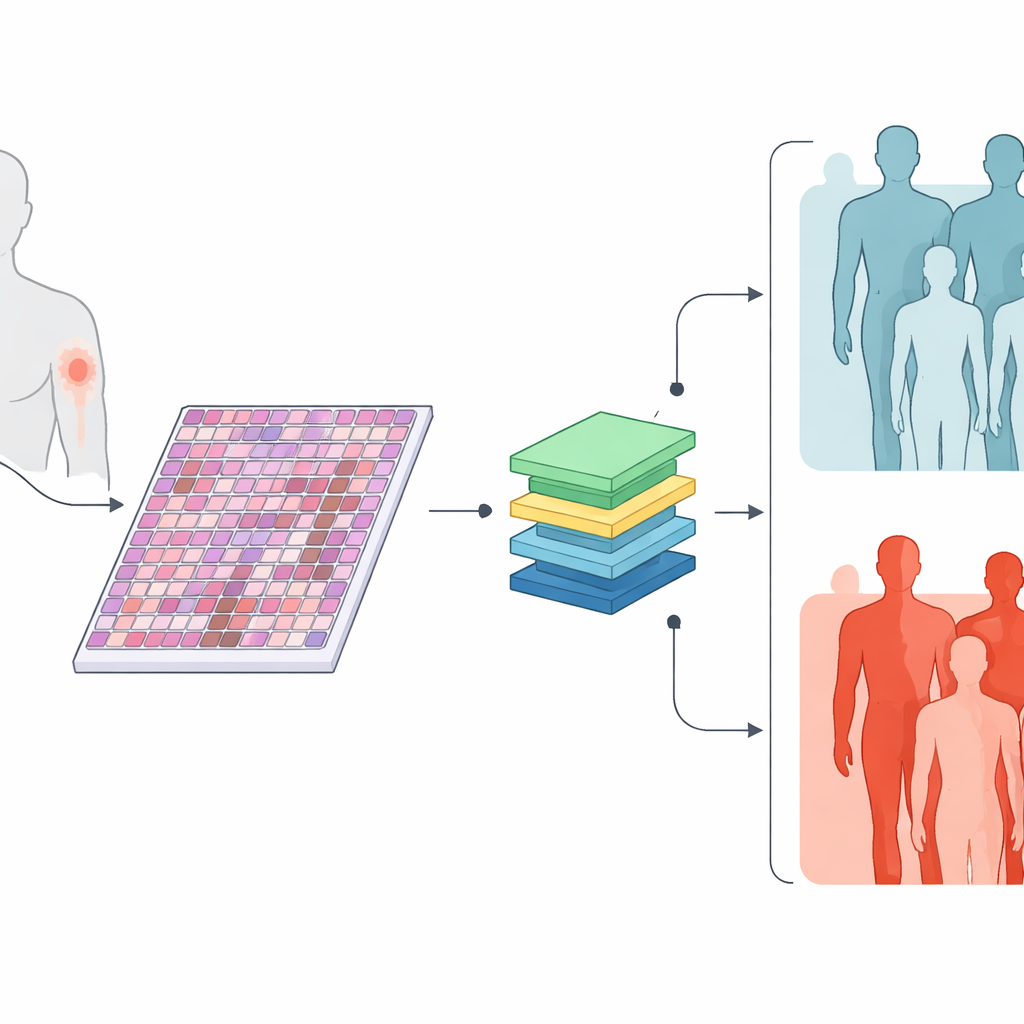
教机器像读地图一样解读组织
团队使用了先在大规模医学图像与文本集合上预训练、然后再针对黑色素瘤微调的最新AI方法。一个模型TransMIL只读取组织图像。另一个模型MultiTrans将图像信息与对肿瘤临床特征的简要文本描述结合起来。第三个较简单的模型BertMLP仅使用这些临床特征,忽略图像。在对一组未见过的切片进行测试时,两个基于图像的模型能在约85%的情况下正确区分转移性与非转移性肿瘤,并在整体准确性上优于仅使用临床数据的模型。这表明显微镜图像中包含着当前常规测量未能完全捕捉的、关于未来行为的丰富线索。
在决策最困难时提供更强的帮助
基于图像的AI优势在中等厚度肿瘤中最为明显——这是医生最难判断谁需要积极治疗的群体。在这些T2级黑色素瘤中,图像模型明显优于仅依赖临床数据的模型,后者倾向于将过多肿瘤判为低风险。图像系统在更厚的肿瘤中也表现良好,但这些病例按现有标准已被认为危险。在若干最初被归类为非转移但随后发生转移的患者中,AI模型数年前就已正确标记原发肿瘤为高风险,暗示此类工具未来可能支持更早、更有针对性的治疗决策。
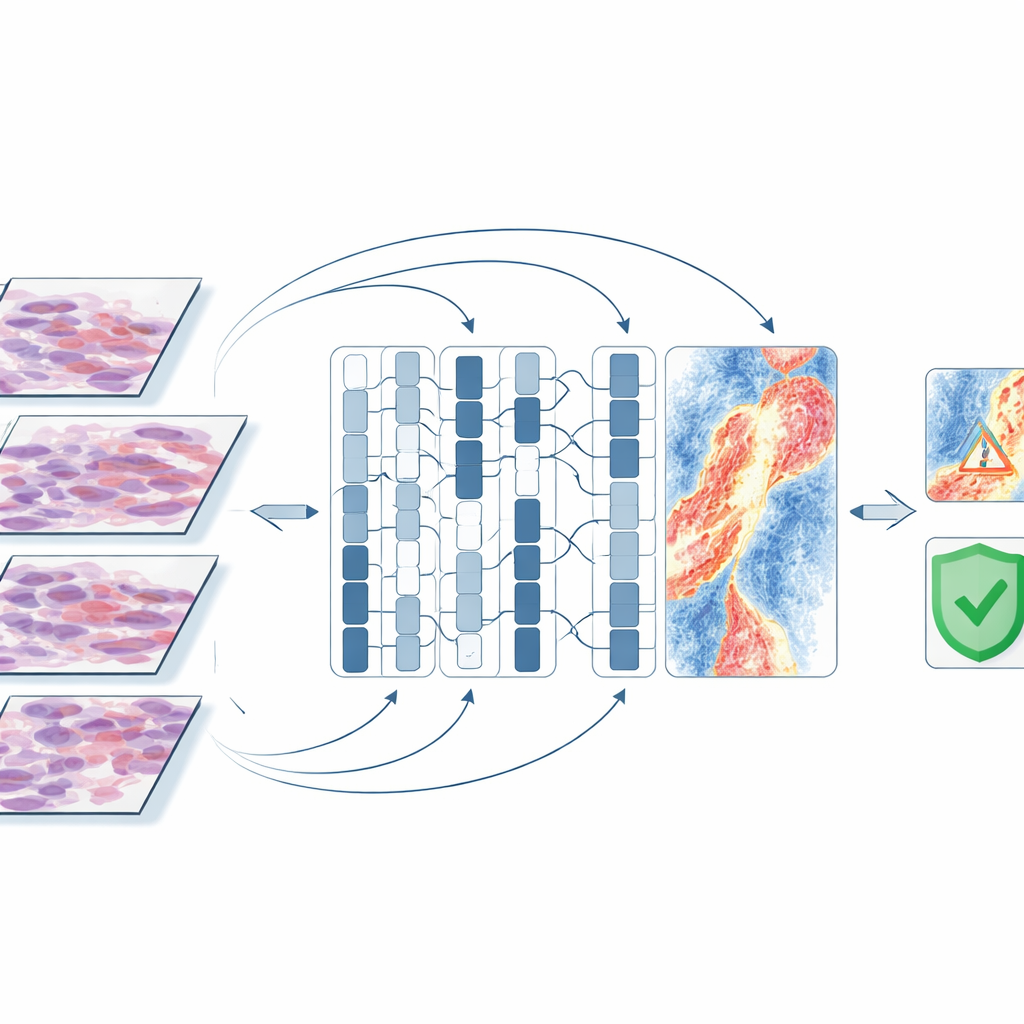
AI在肿瘤内部“关注”的是什么
为理解计算机所依据的线索,研究人员生成了注意力图,高亮出对某一预测最有影响的切片区域。在最终发生转移的肿瘤中,模型经常关注的并非密集的肿瘤细胞团块,而是周围环境:血管、皮肤表面破溃区域以及皮下更深处成带状分布的炎性细胞。在未发生转移的肿瘤中,被高亮的区域往往是完整的表层,几乎没有损伤迹象。被误分类的病例常包含平淡的结缔组织、脂肪或制片时的伪影,提示当清晰的组织信号较弱时,计算机会遇到困难。这些模式与目前对黑色素瘤细胞如何进入淋巴管和血流的理解一致,为AI的判断提供了生物学上的可信性。
局限、下一步以及可能的意义
该工作仅在一家医院、数百例肿瘤上完成,模型尚未在不同中心进行外部验证,也未用于预测生存时间。该方法也不能取代病理学家;相反,它是从常规切片中自动提取的一层新的风险信息。不过,研究结果表明弱监督AI可以直接从原发黑色素瘤组织中发现有意义的转移预警信号,而不需费时的人工标注。如果在更大规模、多中心的研究中得到验证,并与皮肤照片、基因表达检测等其他数据结合,此类工具可帮助医生更好识别那些表面看似早期但实际上隐含高转移风险的患者,并为他们提供更密切的随访或更早的预防性治疗。
引用: Dahlén, F., Shujski, I., Yacob, F. et al. Early detection of metastatic risk in primary cutaneous melanoma using weakly supervised learning. Sci Rep 16, 11234 (2026). https://doi.org/10.1038/s41598-026-45588-w
关键词: 黑色素瘤, 转移风险, 数字病理学, 人工智能, 弱监督学习