Clear Sky Science · zh
基于水相两相体系从血浆中提取非细胞游离DNA用于液体活检的概念验证
为什么血液检测对癌症和其他疾病很重要
许多现代医学检测会寻找在血液中自由漂浮的微小DNA片段。这些称为游离DNA的片段可以揭示肿瘤是否在脱落遗传物质、移植器官是否被排斥或妊娠进展情况。但由于这些DNA片段稀少、片段短并且与大量蛋白质及其他分子混杂在一起,想要快速且纯净地分离它们并不容易。本研究介绍了一种新的、更简便的方法,使用温和的水基分离策略从血浆中提取这些片段,有望使先进的“液体活检”检测更易获得且更经济。
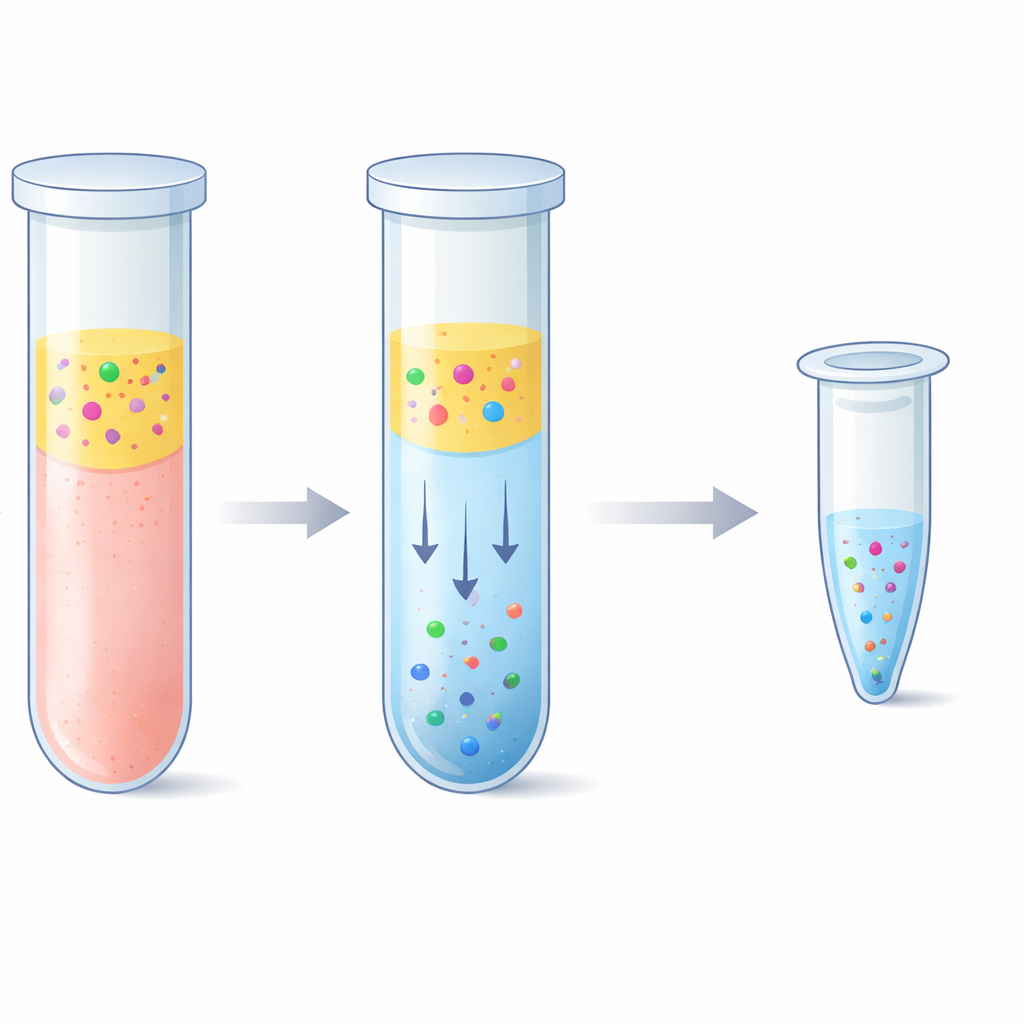
钓出微小DNA片段的挑战
医生和研究人员使用液体活检通过一次简单抽血读取遗传线索,而不是切取组织。但问题在于,血浆中的游离DNA通常仅有每毫升几十纳克,并且被切割成很短的片段。这些材料中只有一小部分可能来自肿瘤或移植器官,因此每一个片段都很重要。标准提取试剂盒通过在强盐存在下使DNA吸附到二氧化硅表面,然后进行多次洗涤和离心步骤来捕获DNA。这些试剂盒能有效工作,但耗时、需要专门设备且成本较高。它们在回收最短片段方面也可能吃力,并且有时会带入不需要的长条常规基因组DNA,从而掩盖罕见的疾病相关信号。
一种利用两层水相捕获DNA的小技巧
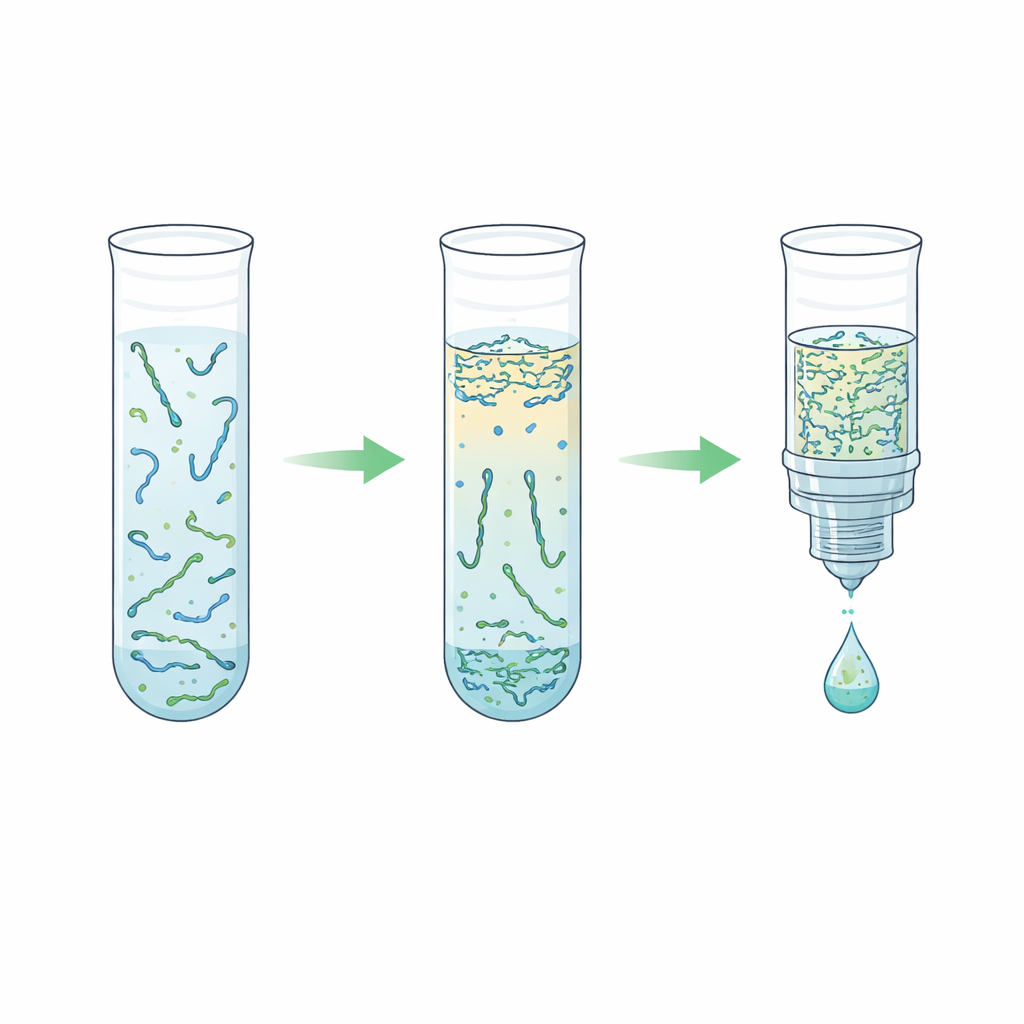
研究小组探索了一种基于“水相两相体系”的替代方法——通俗地说,就是两种都以水为主但不完全混溶的液体,类似油和醋但两者都以水为主。通过将血浆与聚乙二醇这种聚合物和简单的磷酸盐混合,混合物自然分离为上层和下层。令人惊讶的是,短片段DNA明显更倾向于富含盐的下层,而大多数血液蛋白和长DNA则停留在上层或界面处。研究人员精心调整配方,使下层足够小以浓缩DNA,同时又温和到不会损伤DNA。随后他们将此步骤与“反向洗脱”纯化结合,利用将含盐下层推动通过多孔基质来去除盐并缩小最终体积,最终得到更洁净且更浓缩的DNA溶液。
为实际应用改进流程
通过多轮测试,作者调整了聚合物与盐的比例、离心速度、体积以及可选的裂解步骤以打断蛋白–DNA复合体。他们发现沿着某些组成线增加聚合物含量可以在不损害回收率的情况下将DNA浓度提高一倍,并且在反向洗脱步骤中加强处理大约将浓缩倍数较早期工作提高了四倍。出人意料的是,他们发现常规在两相分离前施加的强烈裂解往往并非最佳;裂解会扰动相分离并降低产率。一个精简的、在很大程度上无需裂解的工作流程能去除约99.7%的血浆蛋白,同时在四倍更小的体积中回收大约多达三分之二的短片段DNA,整个过程总耗时约十分钟,实际操作时间只需几分钟。
新方法的比较表现
研究人员将他们的方法与一种广泛使用的商业硅胶试剂盒进行了比较。标准试剂盒在总体DNA产量和更强的浓缩能力上略胜一筹,因为它可以用非常小的洗脱体积。然而,两相法在不同DNA输入量下始终保持高于60%的回收率,即使起始量非常小,而且所需的人工步骤和设备都明显更少。重要的是,该新流程像一个内建的片段长度过滤器:富集了短的、类似游离DNA的片段,同时大体上排除了可能来自破裂血细胞的长片段。定量PCR测试表明,净化后的提取物不会抑制后续扩增。当团队使用含有已知癌症相关突变的商业参考样品时,利用该方法回收的DNA可以构建测序文库,在高通量测序仪上运行,并用于以正确频率检测到所有预期变体。
这对未来血液检测意味着什么
简而言之,这项工作表明,相对简单的水基分离可以替代用于从血浆制备游离DNA的更复杂固相化学方法。尽管该新方法目前的总DNA产量略低于顶级商业试剂盒,但它提供了快速处理、对不需要的蛋白和长DNA的强效去除,并且与PCR和下一代测序兼容。如果在真实患者样本上进一步验证并为自动化做出改进,这种方法有可能降低成本、简化实验室工作流程,从而帮助将基于基因组的癌症、移植和其他疾病的精确血液检测更广泛地推向日常应用。
引用: Meutelet, R., Buerfent, B.C., Hess, T. et al. Proof of concept for aqueous two-phase system-based extraction of cell-free DNA from plasma for liquid biopsy applications. Sci Rep 16, 11232 (2026). https://doi.org/10.1038/s41598-026-45585-z
关键词: 液体活检, 游离DNA, 癌症血液检测, DNA提取, 下一代测序