Clear Sky Science · zh
干扰素-β 和 FTY720 通过与 SOCS1 相关的星形胶质细胞信号传导缓解进展性中枢神经系统炎症
这项研究对多发性硬化患者的重要性
对于许多多发性硬化(MS)患者而言,最大的担忧并非早期的复发性发作,而是随后可能出现的缓慢且持续的功能丧失。在这个后期进展阶段,即使那些作用于血液中免疫系统的常规药物发挥作用,脑和脊髓内部的损伤仍会继续。本研究探讨了一种方法,通过将现有的口服 MS 药物与一种以直接方式送达大脑的长期使用药物形式相结合,以触及这种“隐藏”的炎症。
一种长期性脑疾病且可选方案有限
MS 是一种自身免疫性疾病,机体自身的免疫细胞攻击神经纤维的髓鞘,导致视力问题、无力及其他神经系统症状。早期症状往往断断续续。随着时间推移,许多患者进入以逐渐、常常不可逆残疾为特征的进展期。在这一阶段,血脑屏障变得更难以穿透,驻留于大脑的胶质细胞——尤其是星形胶质细胞和小胶质细胞——的有害活动起到越来越重要的作用。现有治疗主要通过阻断血液中的免疫细胞发挥作用,一旦进入这一阶段,疗效通常有限。
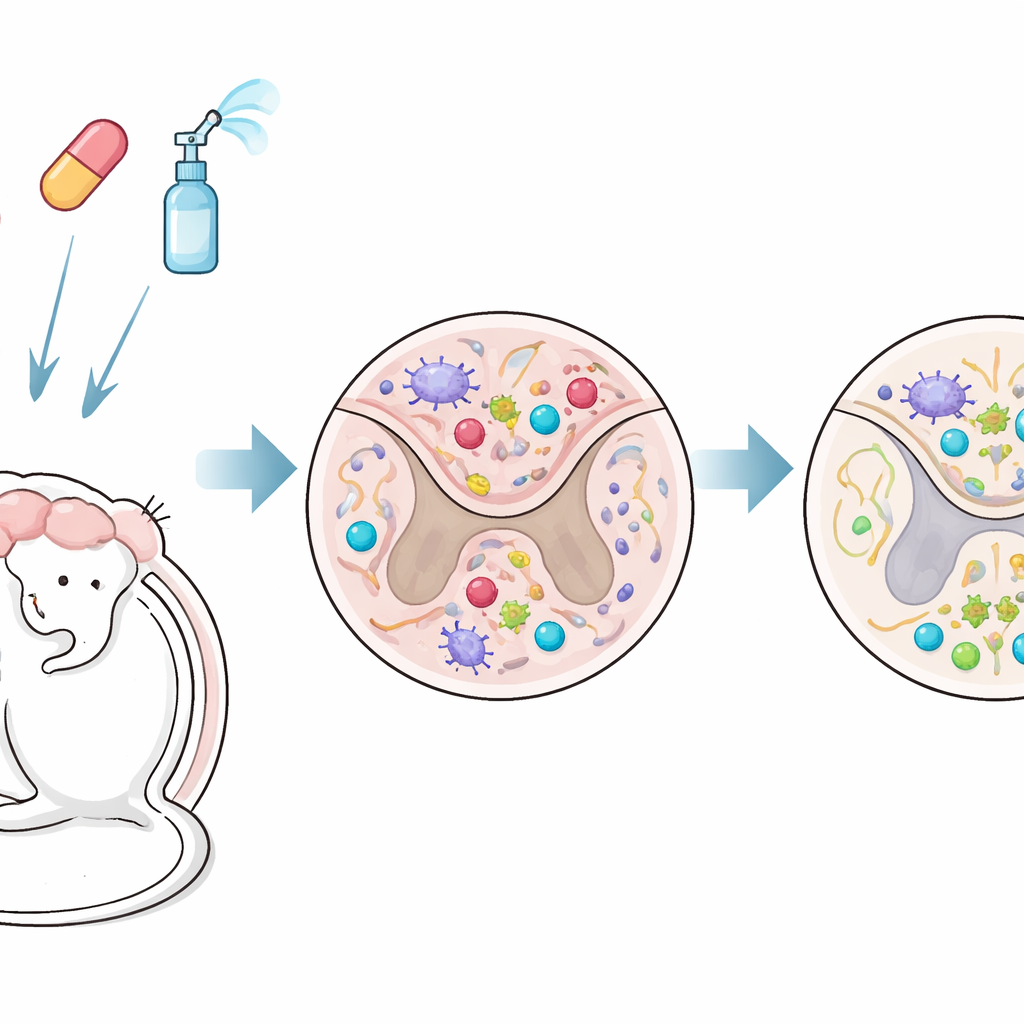
将两种药物配对以同时作用于血液和大脑
研究人员在一个与进展期 MS 高度相似的小鼠模型中测试了联合治疗。其一是芬戈莫德(FTY720),一种能将免疫细胞滞留在淋巴结内的口服药,并且可进入大脑;另一种是干扰素‑β,这是一种长期用于 MS 的疗法,通常由于难以穿过血脑屏障而在脑外发挥作用。在本研究中,干扰素‑β 通过鼻腔给药,从而绕过血脑屏障,更直接地到达中枢神经系统。治疗在小鼠已出现慢性神经学问题之后才开始,反映出一种通常更难逆转的损伤阶段。
损伤减轻与免疫活动平息
接受芬戈莫德加鼻用干扰素‑β 联合治疗的小鼠表现优于仅用芬戈莫德者。疾病评分改善更多,部分既有的神经功能缺损有所减轻。检查脊髓时,研究人员发现更多的髓鞘保存、更少的轴突损伤迹象以及更少的浸润性免疫细胞。促炎性的 T 细胞和单核细胞减少,残留的 T 细胞产生损伤性信使分子干扰素‑γ 和 IL‑17 的量也下降。更重要的是,联合疗法还抑制了来自星形胶质细胞和小胶质细胞的有害信号,这些胶质细胞参与塑造脑和脊髓内的局部环境。
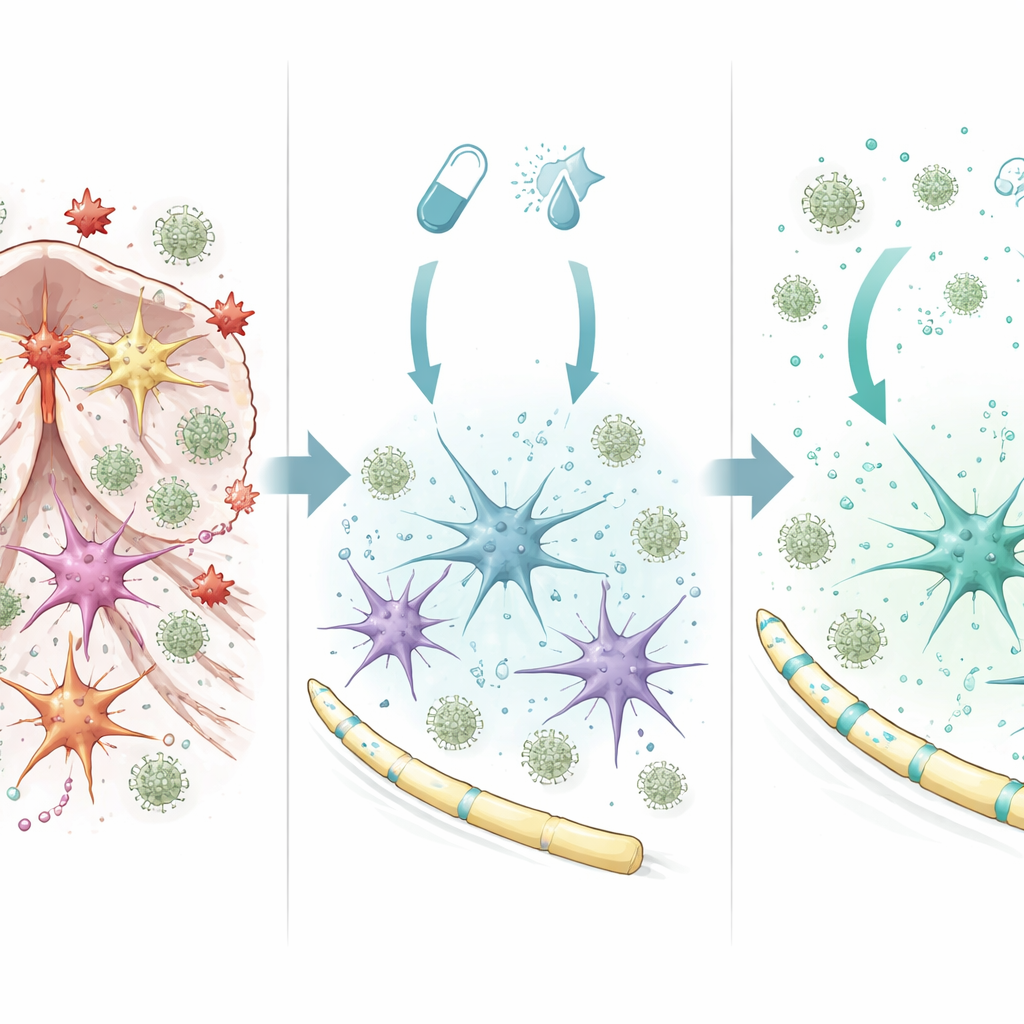
星形胶质细胞由有害行为转向保护性行为
为了解联合治疗在脑内的作用机制,研究团队在培养物中研究了纯化的星形胶质细胞。暴露于芬戈莫德与干扰素‑β 的组合时,星形胶质细胞启动了一组与细胞存活、炎症减少和更健康的神经髓鞘相关的广泛基因表达模式。一个关键因子是名为 SOCS1 的调节子,它对炎症信号起制动作用。在星形胶质细胞中阻断 SOCS1 会抹去大部分保护性基因表达模式,并导致这些细胞释放更多招募免疫细胞的炎性因子。相反,当 SOCS1 活性存在时,星形胶质细胞产生更多促进生长与修复的信号,并释放一类能减少炎性单核细胞迁移的分子混合物。在用该药物组合处理的人类星形胶质细胞和小胶质细胞系中也观察到类似的保护性转变,表明该机制可能超越小鼠具有相关性。
这对未来 MS 治疗的可能意义
本研究表明,将芬戈莫德与经鼻给药的干扰素‑β 配对,能够不仅仅通过阻断血液中的免疫细胞发挥作用,还能将中枢神经系统内的星形胶质细胞重编程为更平静、更具保护性的状态,其中 SOCS1 起到关键控制结点的作用。虽然这些工作主要在小鼠和细胞培养中完成,且在所有实验中并未始终并列测试单独的干扰素‑β,但结果指向一种有前景的策略:同时靶向外周免疫系统与大脑自身的支持细胞。如果在人体中能够实现并证实类似效果且安全性得到保证,这类兼顾外周与脑内的联合策略或许有助于减缓甚至部分逆转推动进展性 MS 的“沉默”性损伤。
引用: Tsaktanis, T., Beyer, T., Nirschl, L. et al. Interferon-β and FTY720 ameliorate progressive CNS inflammation via SOCS1-associated astrocyte signaling. Sci Rep 16, 9851 (2026). https://doi.org/10.1038/s41598-026-45303-9
关键词: 进展性多发性硬化, 芬戈莫德, 干扰素β, 星形胶质细胞, 神经炎症