Clear Sky Science · zh
研究大肠杆菌Colicin E9免疫蛋白与铜绿假单胞菌DNA旋转酶的相互作用:用于开发新型抗菌策略的先进计算方法
将细菌武器转化为新药物
随着抗生素耐药性的蔓延,临床可用来抵御危险感染的手段正在减少。一些最顽固的病原体,如铜绿假单胞菌,能抵御多种药物。该研究从细菌自身寻找新思路,探索一种微生物的内在保护蛋白是否可以改造为使另一种微生物的重要酶失活的工具。通过先进的计算模拟,研究人员展示了一种小型“免疫”蛋白如何紧密结合到关键细菌酶上,提示出一种未来抗菌剂的新途径。
对致命毒素的一道微小护盾
某些毒株的大肠杆菌能产生被称为colicin的强效蛋白毒素,能够杀死邻近细菌。为了避免自毒,这些细菌也产生配套的免疫蛋白。其中一种被称为Colicin E9免疫蛋白(通常称为Im9)的护盾,能绑定毒素的切割结构域,防止其破坏宿主的DNA。由于这种配对极其特异且结合力强,科学家长期认为对其进行细致研究可能揭示控制有害细菌的新方法。在本研究中,作者探讨Im9是否也可能附着于铜绿假单胞菌的DNA旋转酶——一种管理其DNA盘绕与复制的必需酶。
瞄准难治病原体的脆弱酶
铜绿假单胞菌是重要的医院病原体,能在恶劣环境中生存并对多种药物具有耐受性。DNA旋转酶是其最重要的酶之一,负责维持细菌长链DNA的正确扭转,以便复制。因为阻断该酶可以阻止细菌生长,它已经是若干抗生素的既定靶点。作者使用深度学习工具扫描铜绿假单胞菌DNA旋转酶的三维结构,标出可能的“热点”——酶表面对结合伙伴最重要的氨基酸簇。这些区域构成酶的活性位点,正是正常DNA加工发生的地方,也是潜在抑制剂理想的结合位置。
模拟分子间的握手
为评估Im9是否能抓住这些热点,研究人员使用分子对接程序,虚拟地将蛋白质像三维拼图一样“配合”在一起。他们首先对Im9和DNA旋转酶的可用结构进行了清理与修补,修复了酶中缺失的一段回旋并进行了短时模拟以松弛任何应力区域。随后采用两种互补的对接工具ClusPro和LightDock生成大量候选复合体。从中筛选出最有希望的构象,进一步进行了长时间的分子动力学模拟,持续数百纳秒。这些时间分辨的“电影”让他们得以观察两蛋白如何调整、弯曲并在结合时趋于更稳定的构象。
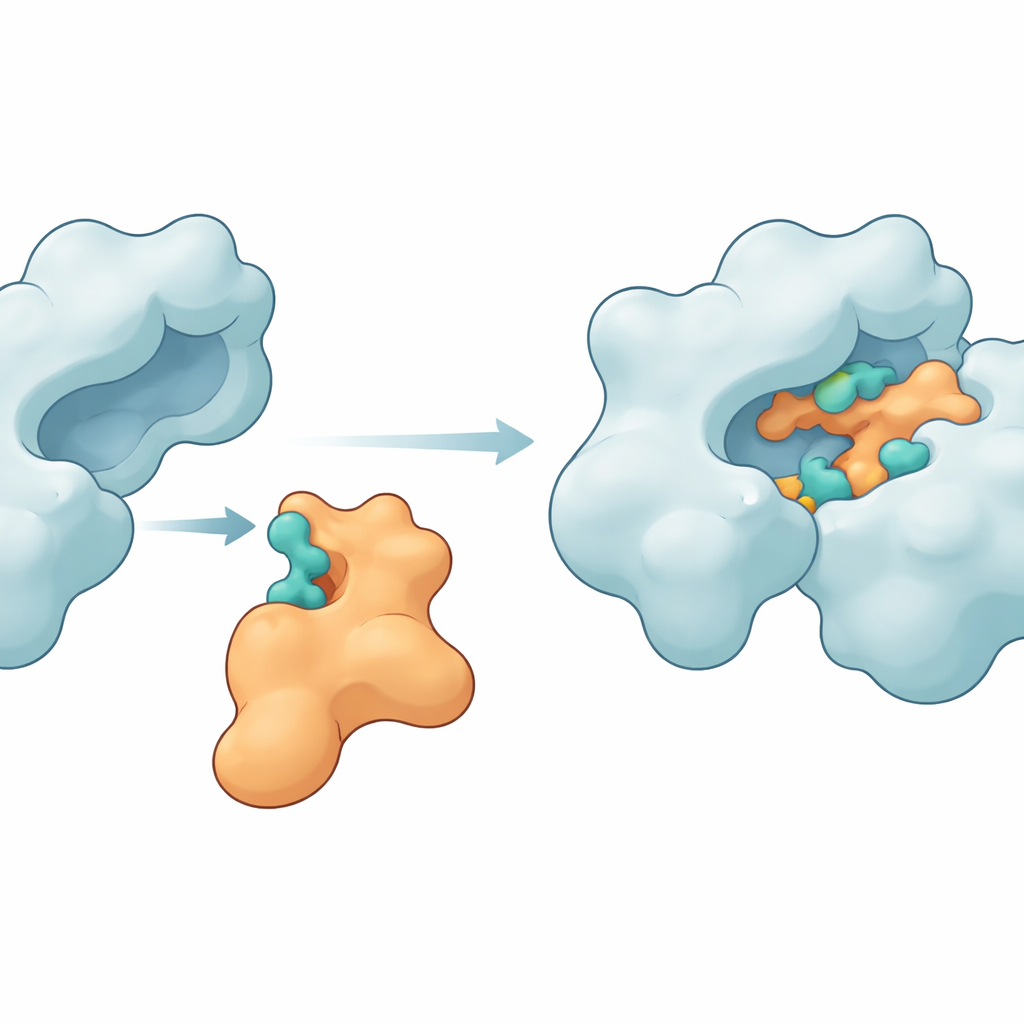
将蛋白黏合在一起的关键接触点
模拟显示Im9确实可以与DNA旋转酶形成紧密且持久的复合体。酶上的若干氨基酸——诸如MET27、ASP47、LYS105、LEU198、ASN199、ARG191和GLU194——反复与Im9上的对应位点形成氢键及其他吸引力。在一个领先模型中,两者在大部分模拟过程中维持了六到十个氢键,表明界面强健且组织良好。其它结构指标——包括蛋白的紧凑程度和构象波动量——显示酶保持完整,而免疫蛋白仅适度弯曲以环绕旋转酶表面。使用MM-GBSA方法的能量计算进一步支持这些接触产生了有利的(尽管适中)结合自由能,电荷相互作用和范德华力为主导贡献。
从计算模型走向未来抗菌剂
综合来看,结果表明Colicin E9免疫蛋白可以稳定地结合到铜绿假单胞菌DNA旋转酶的活性区域,形成一个寿命较长的复合体,理论上可能阻断酶在DNA处理中的正常功能。尽管这些发现完全基于计算模型,仍需实验验证,它们为蛋白抑制剂可能附着的部位和方式提供了详细蓝图。对非专业读者来说,关键的信息是:来自自然的细菌武器与护盾可以激发对抗难治感染的新策略。通过以原子级细节理解这场微观握手,科学家离设计出能关闭关键细菌酶而不伤害人类细胞的新型抗菌剂又近了一步。
引用: Alfaraj, R., Alkathiri, F. & Chikhale, R. Investigating Escherichia coli Colicin E9 immunity protein interactions with DNA gyrase of Pseudomonas aeruginosa: advanced computational approach for developing novel antimicrobial strategies. Sci Rep 16, 10786 (2026). https://doi.org/10.1038/s41598-026-44427-2
关键词: 抗生素耐药性, DNA旋转酶, 蛋白质–蛋白质相互作用, 计算药物设计, 铜绿假单胞菌