Clear Sky Science · zh
热嗜微生物Dolichylphosphate甘露糖合成酶的晶体学数据表明该酶可能会翻转其糖脂产物
耐高温微生物如何维持其细胞包膜的形态
许多在沸腾高温环境中生存的微生物依赖于覆盖在细胞表面的保护性糖衣。构建这种糖衣需要特殊的脂–糖分子,这些分子必须在细胞膜的一侧合成,然后被转移到另一侧。本研究解析了一种来自耐高温微生物的此类分子合成酶,并提出一个引人注目的观点:同一蛋白可能还帮助将其产物翻转穿过膜——实现两项功能。
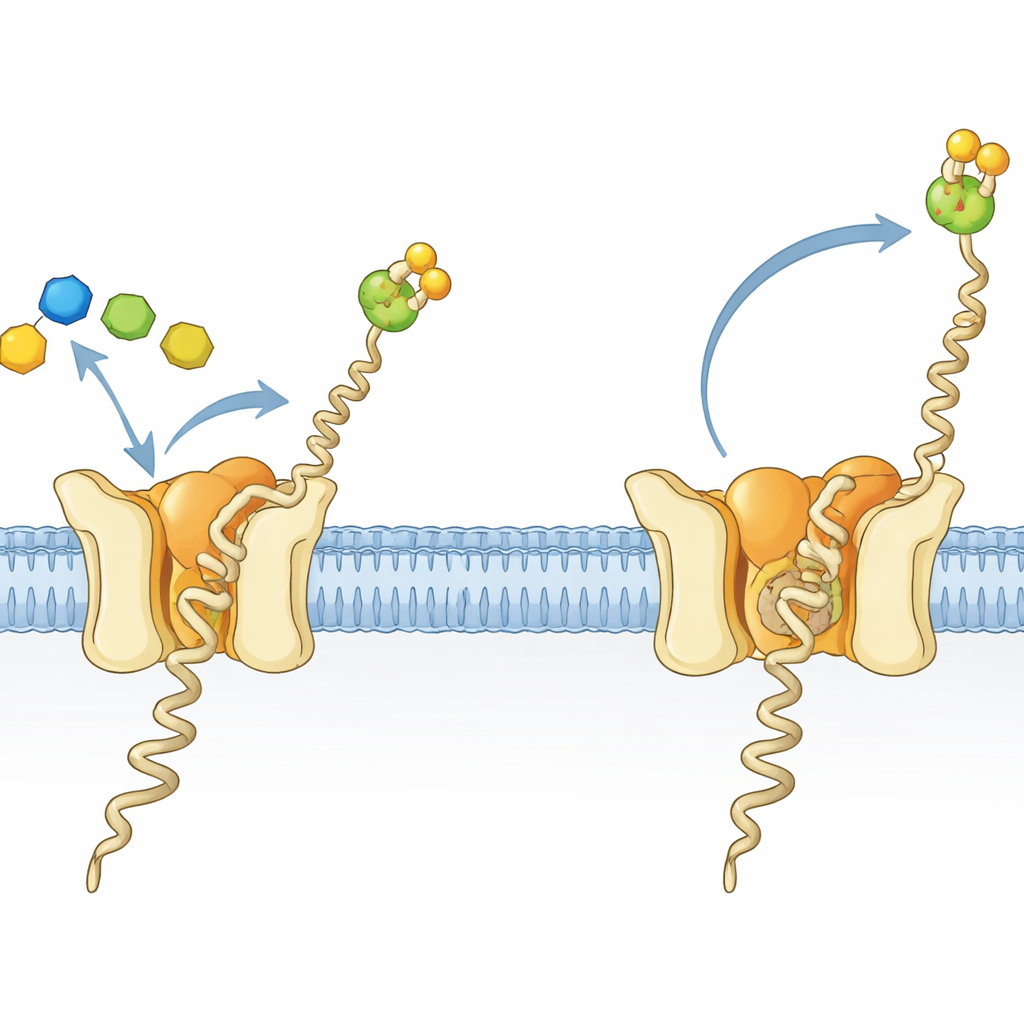
为关键脂–糖分子打造的小型工厂
所有生命域的细胞都会在许多蛋白质上修饰糖链,这一过程对于蛋白正确折叠、稳定性和细胞间通讯至关重要。在古菌和真核生物中,这类修饰的重要构件之一是称为dolichylphosphate mannose(Dol‑P‑Man)的脂–糖分子。它由锚定于膜中的长疏水尾部和伸向水相的糖‑磷酸头部组成。Dol‑P‑Man由酶dolichylphosphate mannose synthase(DPMS)合成,DPMS将可溶性供体上的甘露糖转移到膜结合的脂质上。在嗜高温古菌Pyrococcus furiosus中,DPMS为单链蛋白,被称为III型DPMS,具有一个可溶的催化区域,连接着一个由四个螺旋组成的跨膜部分,其功能此前尚不清楚。
捕捉酶在作用中的瞬间
研究者将P. furiosus的DPMS与底物共同结晶,并通过X射线晶体学追踪反应过程。他们的新结构结合此前的三种结构,捕捉到糖转移发生前后的一系列快照。在一种状态中,供体分子(GDP‑mannose)和类似Dol‑P的受体以精确的构象结合,使甘露糖的反应性碳原子正对着Dol‑P的磷酸基——一个理想的“转移前”排列。酶上的环状结构像前后门一样工作:它们闭合以固定供体和金属离子,然后重排以为Dol‑P进入并在糖被转移后让被消耗的GDP离开打开通道。这些细节阐明了酶如何在膜表面确保高效且精确的糖转移。
隐藏在膜内的颠倒产物
更令人惊讶的是,在相同晶体中观察到的第二种不同构象。在这里,完成的Dol‑P‑Man并不位于活性位点,而是卡在蛋白跨膜部分更深处,以“颠倒”的朝向存在。其糖‑磷酸头部位于两对螺旋(TMD1和TMD2)之间的极性口袋中,而疏水尾部沿着由螺旋形成的槽延伸。一个关键氨基酸——苯丙氨酸,似乎充当门闩,可以阻挡或打开通向该口袋的通道。电子密度的质量及蛋白在晶体中的堆积方式表明,这个翻转的Dol‑P‑Man并非晶体接触的人工产物,而是酶可以采用的真实且被充分占据的构象状态。
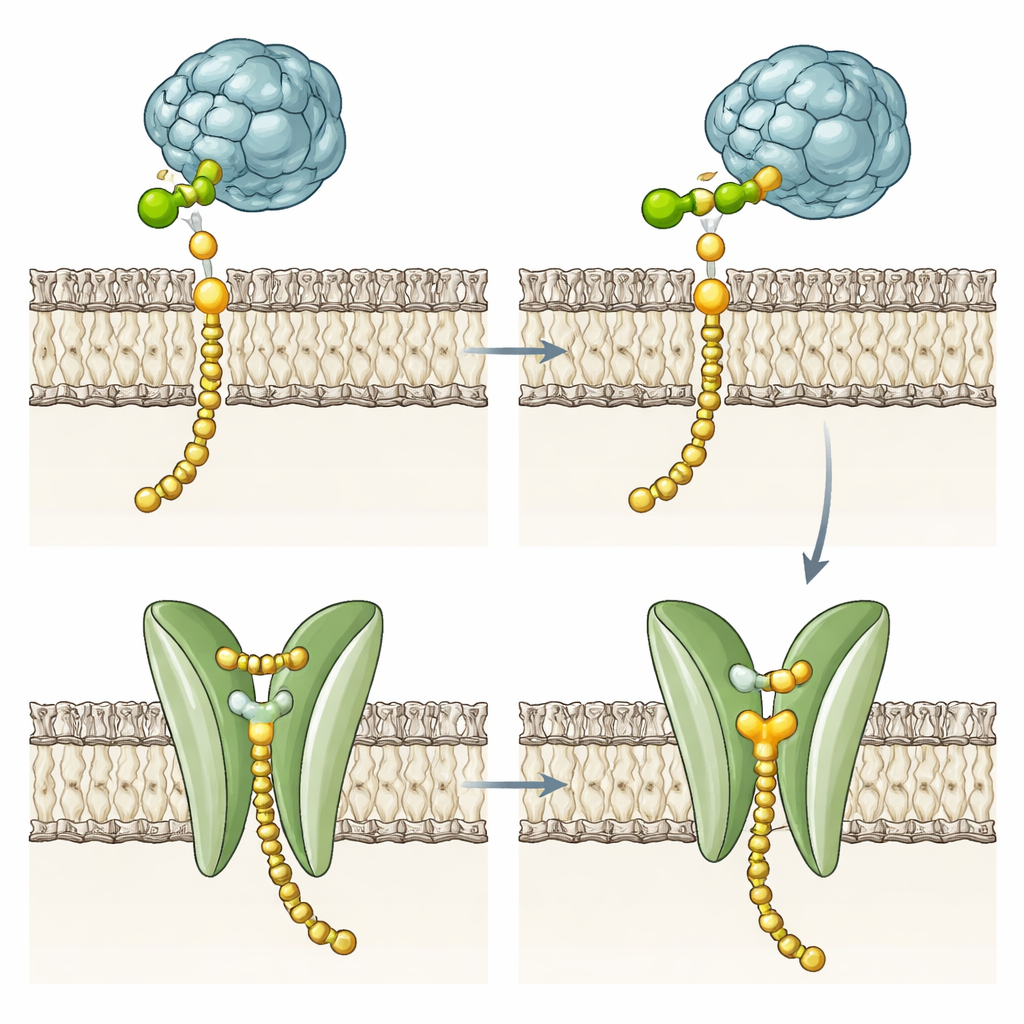
突变酶提示的第二项职责
为了测试跨膜域是否对糖转移化学反应必需,团队构建了多种变体。他们删除了大部分或全部螺旋,将其替换为来自酵母DPMS的不同膜片段,或改变口袋中的关键残基和苯丙氨酸门闩。值得注意的是,这些突变体仍以与完整酶相似的速率生成Dol‑P‑Man,尽管有些在膜中稍微不太稳定。这表明核心化学反应位于可溶的催化区,四螺旋束并非将甘露糖接到Dol‑P所必需。相反,其保守的极性口袋、槽和门控残基提示其在处理生成产物方面具有特殊作用,尤其是在那些膜较为僵硬、自发脂质翻转在能量上代价高的嗜高温古菌中。
为什么一种双重功能的酶很重要
将结构学与突变学证据结合起来,作者提出III型DPMS是一种“多面手”蛋白。它首先在古菌质膜的内侧合成Dol‑P‑Man;然后其跨膜域可能帮助翻转该脂–糖分子,使头部出现在细胞外,供其他构建细胞糖衣的酶使用。进化似乎主要在极端耐热的古菌中偏好这种嵌合设计,在那里将合成位点靠近专门的翻转槽可将浪费和热损伤降到最低。尽管这项工作尚未直接证明翻转活性,但它为酶如何在严苛的膜屏障上既制造又重新定位重要脂质中间体提供了一个具体的结构模型。
引用: Gandini, R., Keskitalo, M.M., Reichenbach, T. et al. Crystallographic data for Pyrococcus furiosus dolichylphosphate mannose synthase suggest that the enzyme could flip its glycolipid product. Sci Rep 16, 9076 (2026). https://doi.org/10.1038/s41598-026-44343-5
关键词: dolichylphosphate 甘露糖, 脂质翻转酶, 古菌, 蛋白质糖基化, 膜酶