Clear Sky Science · zh
在免疫功能完整的肠道芯片平台中模拟艰难梭菌毒素发病机制与抗血清保护
为什么这个肠道感染模型很重要
抗生素能挽救生命,但也可能使肠道易受危险感染的侵袭。其中最令人头疼的是Clostridioides difficile(艰难梭菌),这种细菌可引起严重腹泻并导致结肠危及生命的炎症,尤其在住院患者中更为常见。本研究引入了一个微型“肠道芯片”,重建了人体肠道的关键特征,包括血管和免疫细胞,从而能实时观察C. difficile毒素如何损伤肠道,以及抗体治疗如何阻止这种损害。
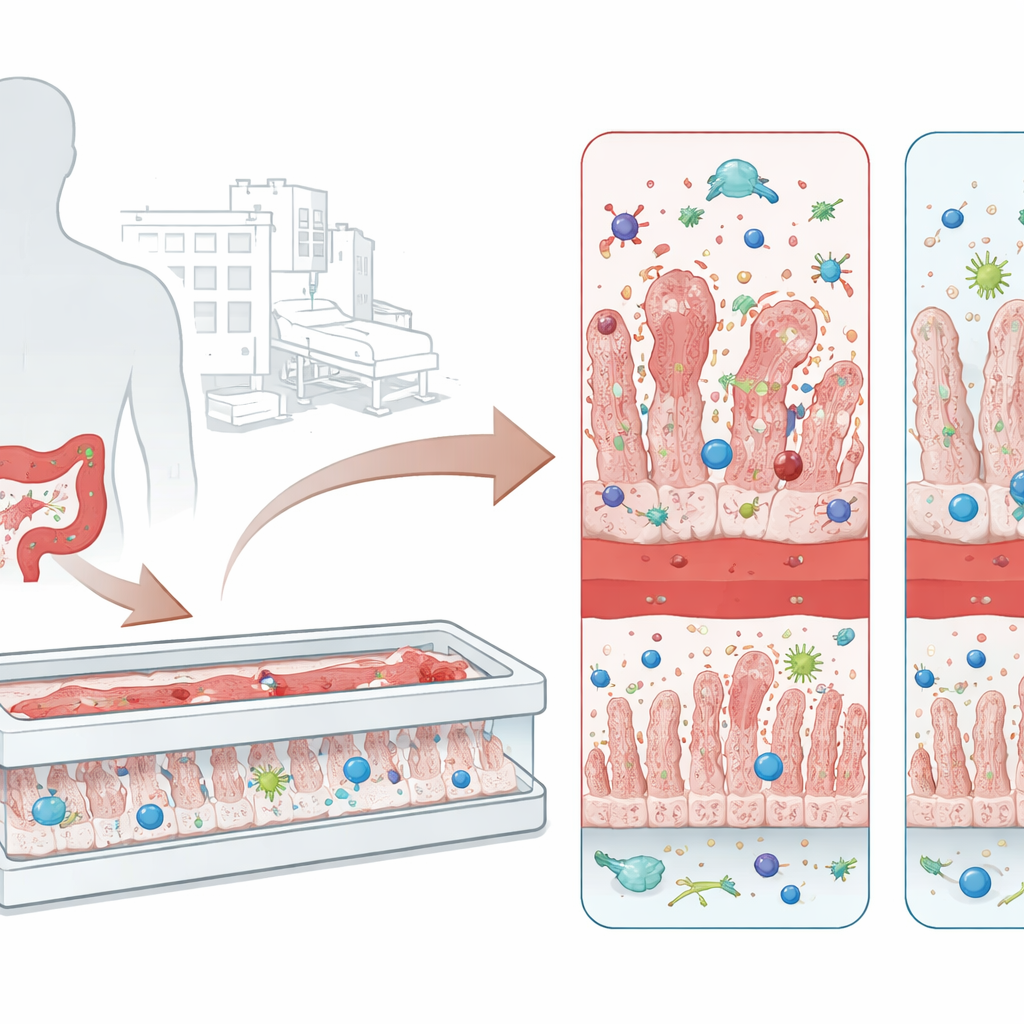
从顽固的医院病原体到肠道损伤
C. difficile会在正常肠道菌群被扰乱的人体内繁殖,常见于接受了广谱抗生素治疗之后。该微生物以耐久的孢子形式存活于严苛环境中,一旦在结肠定殖,会释放两种主要毒素,称为TcdA和TcdB。这些毒素攻击肠上皮细胞,破坏细胞间的紧密连接,并引发大范围炎症。病情可从轻微顽固的腹泻发展到伪膜性结肠炎,其特征是肠壁被死组织和免疫细胞覆盖。当前治疗主要依赖更多抗生素,有时采用粪便移植,但许多患者仍反复感染,凸显出需要更好方法来研究该疾病并测试阻断毒素的治疗手段。
在芯片上构建微型活体肠道
传统实验模型在培养皿中生长平面的肠上皮细胞层。尽管有用,这些二维培养缺乏血管、免疫细胞以及塑造真实肠道的温和流体动力。研究者因此使用了一个微工程的“肠道芯片”装置,包含由多孔膜分隔的两条平行通道。一侧铺有肠上皮细胞,细胞生长成类似绒毛的指状结构并形成紧密屏障。另一侧则为人体血管内皮细胞。研究团队向这段微型组织中加入了单核细胞来源的巨噬细胞,使其驻留在肠壁,以及可通过血管通道循环并浸润组织的中性粒细胞,从而创建出一个更接近生理、具备免疫功能的肠道芯片(i‑IoC)。
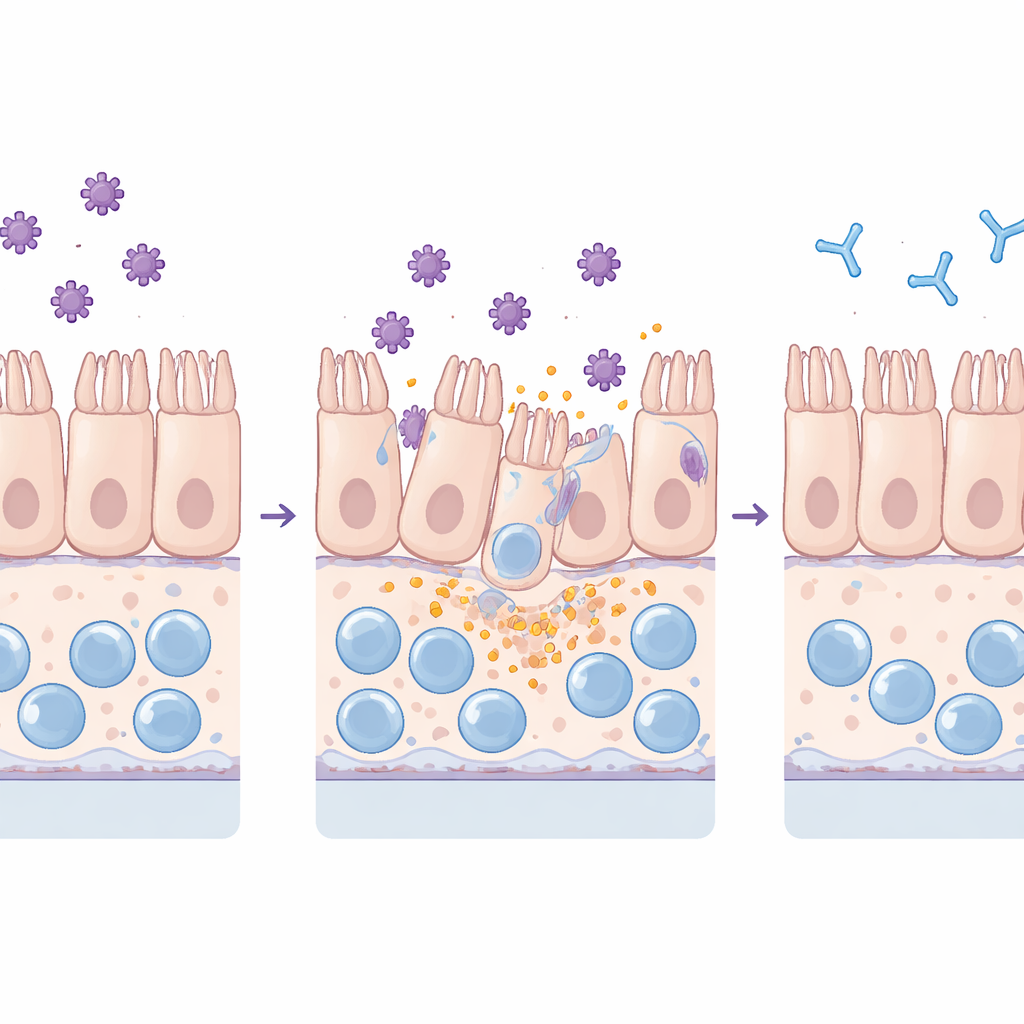
观察毒素如何损伤屏障
团队将纯化的TcdA和TcdB分别作用于传统平面培养和更复杂的芯片模型。他们监测肠道屏障阻止荧光染料渗透的能力、检查维系相邻细胞的连接蛋白,并测量周围液体中的炎性分子与细胞损伤标志物。两种毒素都对组织造成损害,但方式有别:TcdA主要破坏紧密连接并使细胞圆缩,而TcdB则导致大量细胞从上皮层脱落。关键是,芯片在远低于平面培养可检测到的毒素浓度下就能发现这些效应,反映出它在持续流动条件下的更高灵敏度和更接近活体的行为。
免疫细胞加剧反应——但也能被保护
向芯片中加入巨噬细胞和中性粒细胞放大了对毒素的反应。巨噬细胞促使关键炎性介质如IL‑6和IL‑8的释放增加,但自身数量减少,这与一种炎性细胞死亡形式相符。中性粒细胞粘附在血管壁并迁移入肠组织,重现了病人中观察到的免疫细胞涌入。更长时间的毒素暴露不仅损伤肠上皮,也最终损及血管层。然而,当研究者将毒素与中和毒素的抗体血清预先混合时,结构性损伤、屏障泄漏、细胞因子激增、巨噬细胞丢失和中性粒细胞浸润均显著减少。在延长的实验中,TcdB所致的损伤在移除毒素后可部分恢复,而TcdA则留下更持久的损害,这提示两种毒素在修复能力上存在差异。
这对患者和治疗意味着什么
对普通读者来说,关键结论是这个微型活体肠道模型可以真实模拟C. difficile毒素如何损伤肠道并激发免疫反应,同时评估抗毒素抗体对组织的保护效果。与简单的细胞层相比,肠道芯片更为敏感,包含血管和免疫细胞,并且可以持续运行数日以捕捉早期损伤与随后的修复尝试。这使其成为测试下一代中和毒素的治疗和疫苗的有前景的平台,能够在不进一步扰乱肠道微生物的前提下中和毒素,并有潜力在未来使用患者来源的细胞进行个体化疗法筛选。
引用: Wegner, V.D., Warschinke, M., Brahim, I.B. et al. Modeling Clostridioides difficile toxin pathogenesis and antiserum protection in an immunocompetent intestine-on-chip platform. Sci Rep 16, 9233 (2026). https://doi.org/10.1038/s41598-026-44170-8
关键词: 艰难梭菌, 肠道芯片, 肠道感染, 中和抗体, 器官芯片模型