Clear Sky Science · zh
无标记多光子显微成像与机器学习用于识别肝细胞癌
这对肝癌患者为何重要
肝癌,尤其是肝细胞癌,既常见又致命,手术往往是唯一治愈的机会。手术中,外科医生必须在尽可能保留健康肝脏的同时切除整个肿瘤;当患病肝组织本身已经外观异常时,这是一项极具挑战的平衡。本研究探索了一种在手术中实时“看见”癌变的新方法,无需染色剂或耗时的实验室流程,通过将先进的激光显微成像与人工智能结合,目的在于帮助外科医生更快、更准确地找到肿瘤真实边界,可能改善患者的手术结局。
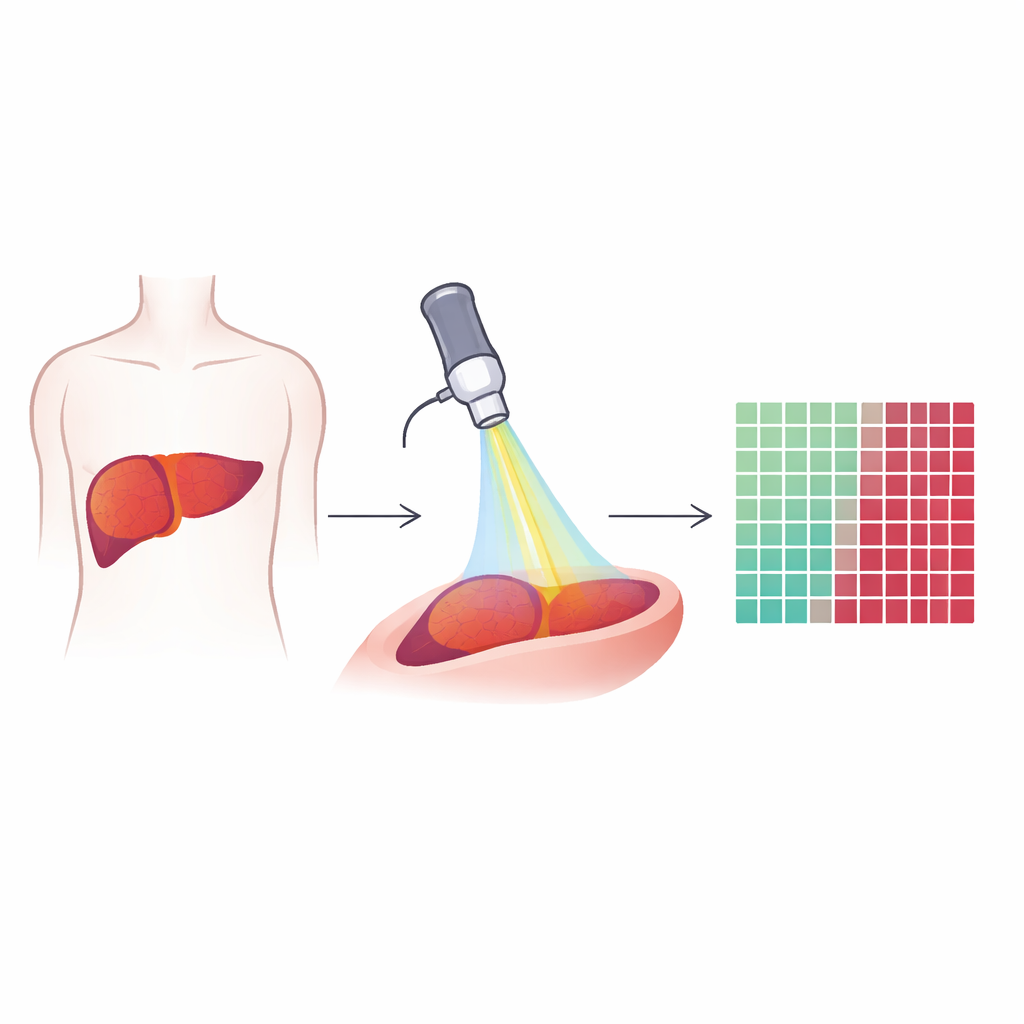
用特殊光线观察组织内部
研究人员使用了一种称为多光子显微镜的技术,该技术依赖极短的激光脉冲使组织中天然分子发光或产生信号。该方法不添加染色剂或对比剂,而是读取已有的信息:脂质、胶原纤维以及细胞内天然荧光物质。每个微小视野从肝组织样本中记录了三类信号:一种突出脂质,一种显示如NADH和维生素A等分子的自发荧光,另一种揭示刚性胶原纤维。综合这些信号可生成色彩丰富、高分辨率的图像,既能显示单个细胞又能呈现肝组织与肿瘤的整体结构。
捕捉肝癌的多种面貌
团队检查了76位接受肝癌手术患者的组织,既看肿瘤也看周围肝组织。他们证明这种无标记成像能够呈现肝细胞癌的典型生长模式,例如薄板或厚板状的肿瘤细胞排列、实性片以及腺样结构。它还显示了周围肝组织的改变,包括脂肪堆积和瘢痕形成,这些在慢性肝病患者中很常见。重要的是,这些模式即使在相对较低分辨率下也可见,这类似于未来可置入体内的内窥设备可能提供的成像质量。这表明该方法在手术室中具有实际可行性,而不仅限于实验室环境。
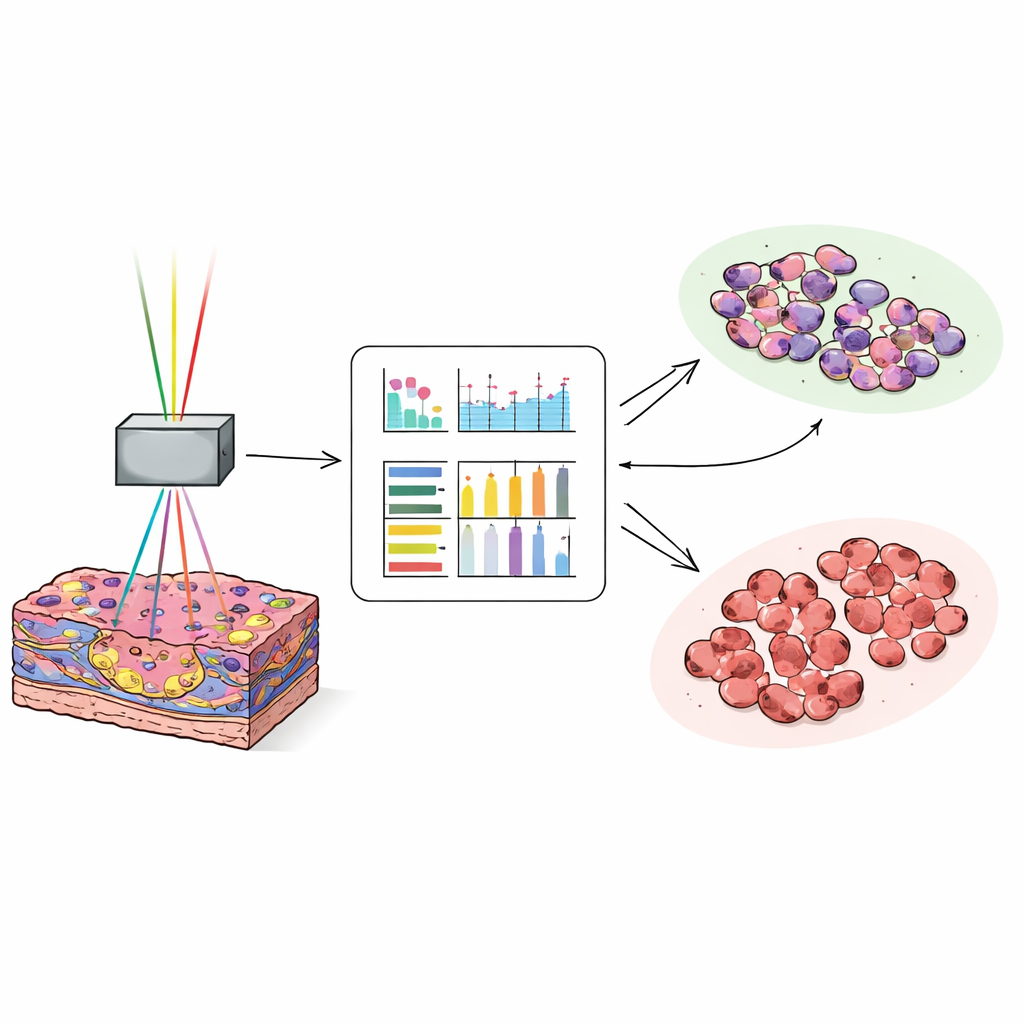
教计算机识别肿瘤边界
为将丰富但复杂的图像转化为快速决策,科学家们把每幅图像转换为描述纹理的数值,例如像素模式的光滑度、粗糙度或多样性。对于每个图像通道,他们计算了17项此类测量,并用来自35位患者约25,000张图像训练了一个神经网络,以区分肿瘤组织与非癌性肝组织。随后他们在另外38位患者的约27,000张新图像上测试该模型。当计算机使用自发荧光与胶原敏感信号的组合时,大约能在100例中正确标记97例图像为肿瘤或正常。即便是那些分化良好、病理学家在快速冷冻切片上也难以识别的微妙肿瘤,分类准确度仍然很高。
光学模式对癌症的揭示
通过比较不同信号组合,研究发现自发荧光携带了区分癌与非癌的最多有用信息。这种荧光来自细胞内的多种天然分子以及弹性蛋白和胶原等结构,因此它编码了细胞密度、核的大小与形状(表现为较暗区域)、脂滴以及周围组织的成分。加入胶原特异性信号进一步增强了肿瘤与背景肝组织之间的对比,反映了纤维和血管排列差异。出人意料的是,聚焦脂质的信号对自动分类的贡献较小;这一实用见解可能允许更简单的设备设计,依赖单束激光而非更复杂的双束系统。
从实验室台面走向手术室
为了模拟真实手术使用,团队还将最优模型应用于包含肿瘤与肝脏实际交界处的组织样本,生成概率图以突出癌组织终止与正常组织开始的位置。这些概率图总体上与常规组织学结果高度一致,尽管高度脂肪化或富含胶原的区域有时会混淆分类器。作者指出在将该技术用于实时手术前仍有若干障碍,包括光学成像的有限深度、需制造稳健且无菌的内窥镜、手术视野中的运动与出血问题,以及在大型真实世界数据集上验证人工智能的挑战。尽管如此,这项工作表明无标记多光子成像结合机器学习,可作为一种快速的数字显微镜,有朝一日可能帮助外科医生更精确、更安全地切除病灶,从而在尽可能保留健康肝组织的同时提高切除全部癌变的几率。
引用: Galli, R., Korn, S., Aust, D. et al. Label-free multiphoton microscopy and machine learning for recognition of hepatocellular carcinoma. Sci Rep 16, 8734 (2026). https://doi.org/10.1038/s41598-026-43831-y
关键词: 肝癌成像, 多光子显微镜, 自发荧光, 手术切缘, 机器学习