Clear Sky Science · zh
阐明亲和力与效力在治疗性IgE性能中的关系
将过敏抗体转用于对抗癌症
过敏患者都知道IgE抗体的威力——这些分子会触发眼睛瘙痒和突然打喷嚏。本研究提出了一个令人意外的问题:是否可以将这种强大的生物学机制重新定向用于抗癌?如果可以,应当如何精确调节这些抗体以获得最佳效果?研究者将目标对准产生HER2蛋白的乳腺癌,包括那些HER2表达极低、当前药物常常失效的病例。
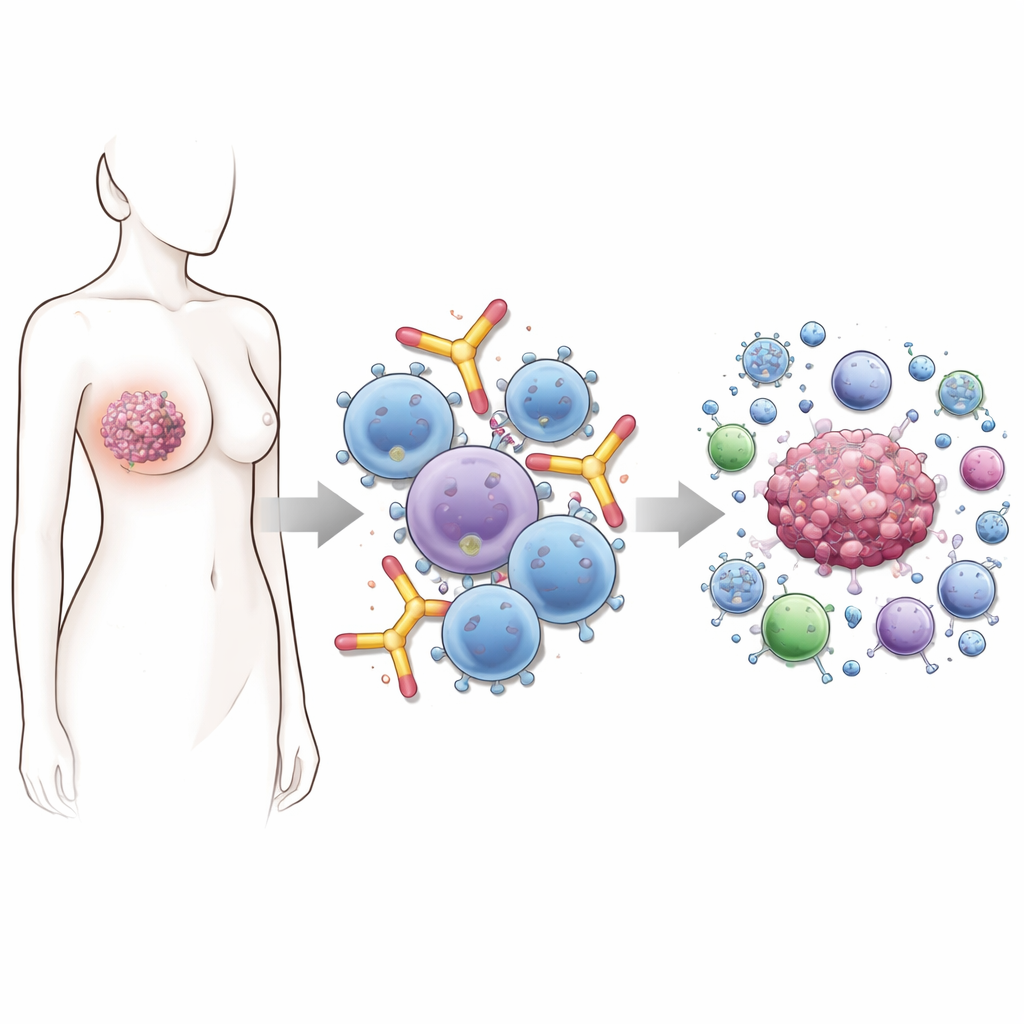
这种抗体类别为何如此特殊
目前上市的大多数抗体药物属于IgG类。它们是现代癌症治疗的主力,但也有局限——尤其当肿瘤通过降低表面靶蛋白数量来逃避免疫时。IgE抗体则不同。它们天然能够非常紧密地与肥大细胞、嗜碱性粒细胞、单核细胞和巨噬细胞等免疫细胞结合,使这些细胞处于快速反应的准备状态。在过敏反应中,这意味着对花粉或食物的剧烈反应;在癌症中,相同的机制可能意味着一旦IgE在肿瘤表面遇到靶点,就能发起快速、聚焦的攻击。
设计更锋利的癌症定位IgE
该团队此前已经构建了一种识别乳腺癌HER2的IgE抗体,称为EPS 226,在实验模型中可减缓肿瘤生长。在这项新工作中,他们着手回答一个细微但关键的设计问题:使抗体对HER2的抓握更紧,是否真能提升其召集免疫系统的能力,还是IgE天然的“多点”结合(称为亲合力)已经能完成大部分工作?为此,他们采用靶向诱变和细菌筛选的方法,生成了数百万种HER2结合区的小变体,最终筛选出12种比原始抗体对HER2结合更强的新IgE变体。
在细胞与动物中的功效测试
这些改良后的抗体随后在一系列细胞实验中接受考验。当这些抗体装载于肥大细胞并暴露于HER2阳性癌细胞时,大多数高亲和力的IgE引发了更强的脱颗粒反应——一种释放强效免疫化学物质的激活反应。其中一个变体,被命名为EPS 232,在激活细胞的能力同时仍能有效结合人源和鼠源肿瘤细胞方面表现突出。进一步测试显示,EPS 232更能武装免疫细胞以杀伤癌细胞:它增强了嗜碱性粒细胞的细胞毒性,并促进工程化免疫细胞和原代人巨噬细胞更有效地吞噬HER2阳性肿瘤细胞。有趣的是,增强结合强度的收益仅在一定范围内成立;亲和力极高的变体并未优于EPS 232,这表明存在一个“最佳点”:抓握足够强以发挥作用,但又不至于强到妨碍每个肿瘤细胞上多只抗体和免疫细胞的协同接触。
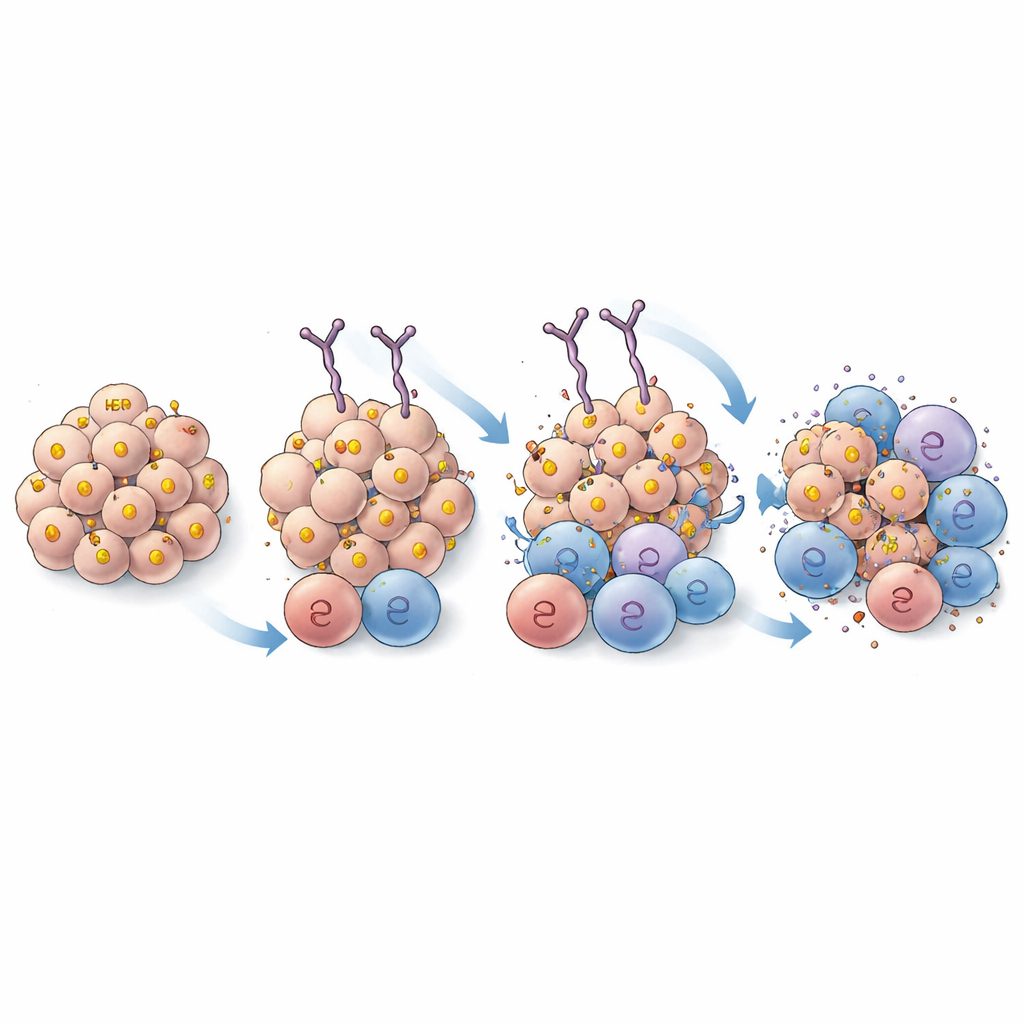
放大观察抗体如何结合
为确保性能提升来自于亲和力增强而非识别了HER2的新位点,科学家们使用高分辨率冷冻电子显微镜可视化EPS 232和原始EPS 226与HER2蛋白的结合方式。结构显示,两种抗体都停靠在HER2的相同区域并使用非常相似的接触点,仅有细微差别,预计不会改变整体结合位点。这支持了EPS 232性能提升来源于亲和力改进而非靶点改变的观点。
从试验台到肿瘤控制
真正的考验在动物模型中进行。在携带人类乳腺肿瘤并供有人人体免疫细胞的小鼠中,EPS 232以比EPS 226更低的剂量更有效地抑制了肿瘤生长。在携带一种产生超低水平HER2的侵袭性乳腺癌大鼠模型中——类似某些三阴性乳腺癌——经适配的大鼠版EPS 232不仅比其前体更能减缓肿瘤生长,还延长了动物的存活期。受治疗动物的肿瘤显示出更多的T细胞和巨噬细胞浸润,表明改良后的抗体更善于将肿瘤微环境重塑为有利于免疫攻击的状态。
这对未来癌症疗法意味着什么
对普通读者来说,主要信息是:微调IgE抗体与癌症靶点的结合强度,确实可以显著影响其疗效,尽管IgE自身已通过多点接触建立了强有力的机制。研究将EPS 232确定为针对HER2阳性及HER2低表达乳腺癌的领先IgE药物候选者,包括目前缺乏有效治疗方案的亚型。更广泛地说,这表明“过敏式”抗体可以通过合适的结合强度平衡被工程化,让通常引起打喷嚏的高敏感系统,转而帮助免疫系统识别并清除肿瘤。
引用: Marano, F., McKenzie, C., Birtley, J.R. et al. Elucidating the relationship between affinity and potency in the performance of therapeutic IgE. Sci Rep 16, 10555 (2026). https://doi.org/10.1038/s41598-026-43772-6
关键词: 治疗性IgE, HER2乳腺癌, 抗体亲和力, 癌症免疫疗法, 三阴性乳腺癌