Clear Sky Science · zh
天然遗传变异影响亚洲巴伐利亚伯氏疏螺旋体PFam54同源蛋白的补体抑制活性
这对莱姆病为何重要
莱姆病已是北半球最常见的蜱媒疾病,但并非所有致病的伯氏疏螺旋体在机体内的表现都相同。这项研究聚焦于与主要莱姆病病原关系密切的巴伐利亚伯氏疏螺旋体,提出一个简单却意义重大的问题:亚洲与欧洲菌株的天然遗传差异,是否会改变这些细菌躲避血液中首批防线之一——补体系统的能力?答案有助于解释这些微生物如何传播、如何致病,以及未来可针对的治疗或疫苗靶点。
两大洲的故事
巴伐利亚伯氏疏螺旋体在欧亚大陆的小型动物与蜱之间循环,并能导致人类的莱姆病。欧洲菌株常表现出对神经系统的强烈偏好,常见于神经梅毒样的神经性莱姆病例,而亚洲菌株似乎较少与脑神经感染相关。遗传学研究提示,欧洲菌株可能起源于种群多样性更高的亚洲祖先,并在适应欧洲不同蜱种时经历了瓶颈。这个进化事件可能重塑了细菌基因组的部分区域,包括位于称为 lp54 质粒上的一组名为 PFam54 的基因簇。许多 PFam54 基因编码的表面蛋白能通过干扰补体,帮助细菌在血液中存活。
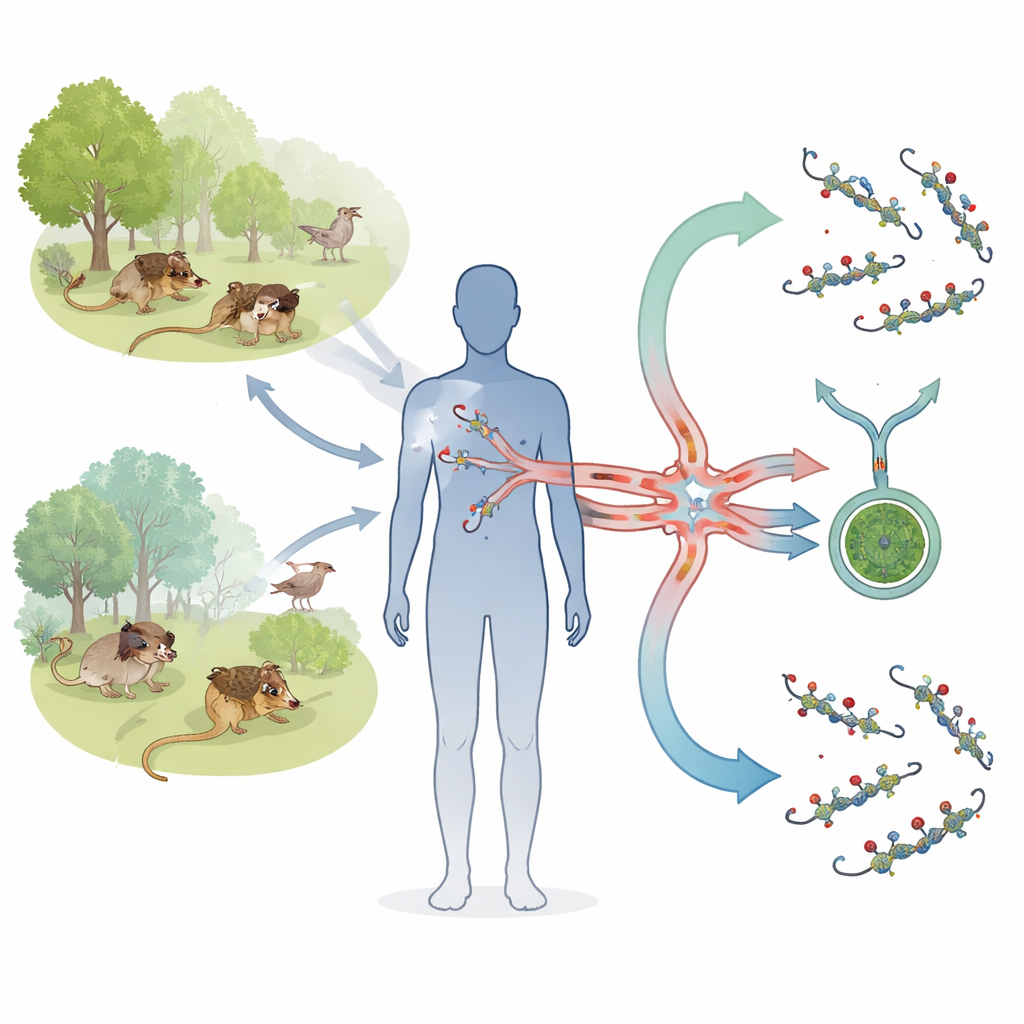
细菌如何躲过血液攻击
可以把补体系统想象成一种分子级的警报,一旦被触发,最终会形成“膜攻击复合体”,在细菌膜上钻孔。先前对欧洲参考菌株的研究表明,两个 PFam54 蛋白 BGA66 和 BGA71 位于细菌表面,能结合补体的末端成分(C7、C8、C9),阻止这一终端孔结构的组装。然而,亚洲的 B. bavariensis 菌株通常携带不同组合的 PFam54 基因,有些甚至不含欧洲株中存在的确切 BGA66 与 BGA71 基因。研究者因此探究这些亚洲变体是否仍能作为补体防护屏障,以及是否存在亚洲特有的 PFam54 家族成员提供替代性保护。
用遗传学与结构学探查多样性
研究团队首先比对了数十株亚洲与欧洲 B. bavariensis 基因组中的 PFam54 基因。如预期,亚洲菌株在该家族中显示出更高的序列多样性,但总体模式表明这些蛋白仍然承受保持基本功能的选择压力。利用 AlphaFold 预测三维结构,他们发现亚洲版本的 BGA66 与 BGA71 以及若干相关蛋白尽管存在大量氨基酸改变,仍折叠成非常相似的全螺旋形状。这些突变倾向于聚集在暴露于表面的区域——正是与补体相互作用之处——暗示进化可能偏向于细化结合特性,而不是完全丧失功能。
将蛋白进行功能检验
为了解这些差异在实际中的影响,研究者将亚洲 PFam54 蛋白在细菌中表达并在人体血清中测试。两株日本 B. bavariensis 分离株 NT24 与 JHM1114 对活性人补体介导的杀伤表现出高度抗性,类似于欧洲型参考株。从这些菌株分离并纯化的蛋白随后在受控试验中与人补体成分混合测试。亚洲的 BGA66 仍能阻断膜攻击复合体的形成,但效率低于欧洲对应物。一个亚洲的 BGA71 变体在通路后期部分受损步骤上有抑制作用,但需要更高剂量才能显现效果。引人注目的是,一个仅见于亚洲的新蛋白 BGA67b 强烈抑制末端通路,但并不直接阻断 C9 的聚合,提示其通过不同机制阻止孔的组装。当这些 PFam54 蛋白在原本对补体敏感的替代菌株表面表达时,使该替代菌株获得血清抗性,证实了它们的保护作用。
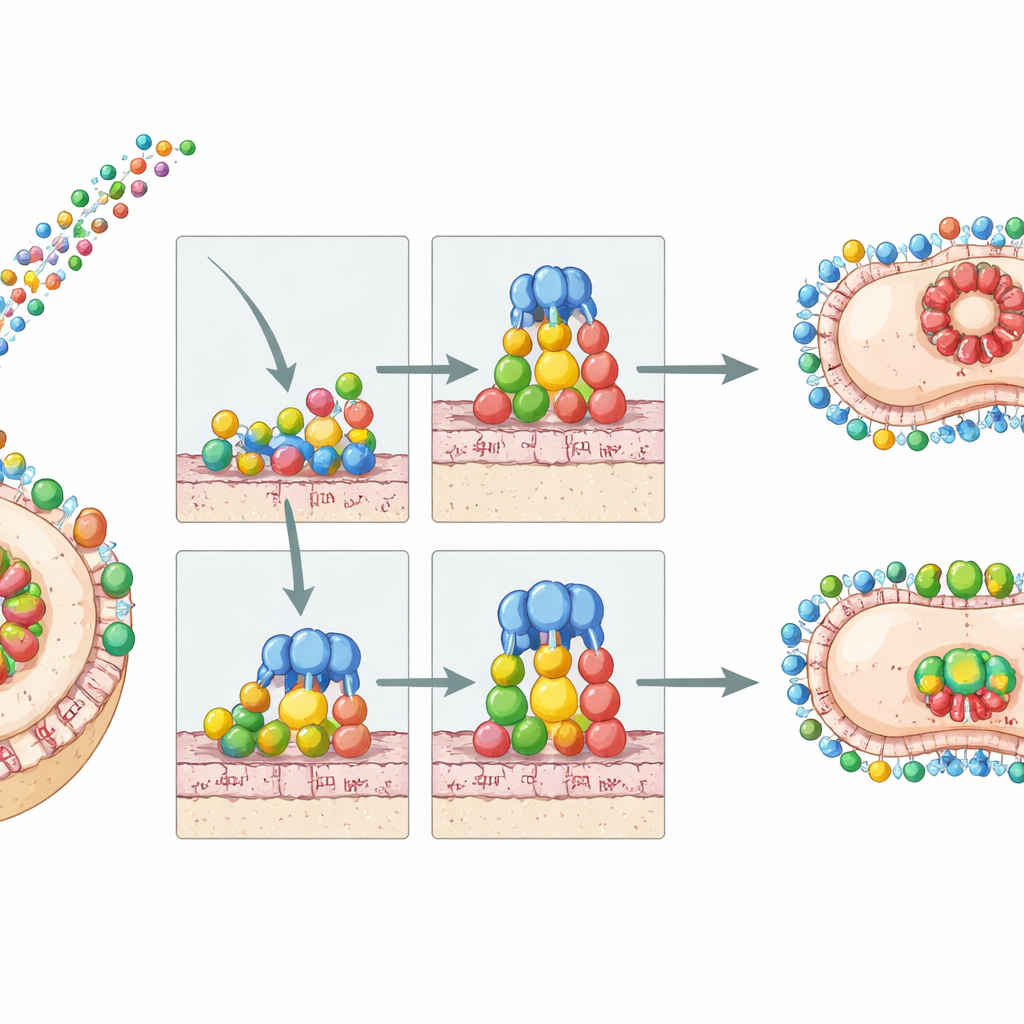
对患者与未来研究的意义
通俗地说,这项工作表明无论亚洲还是欧洲的 B. bavariensis 菌株,都配备了能在分子水平上保护它们免受血液补体分解的“盾牌”。具体的盾牌蛋白及其效率各有差异,但总体策略——在攻击序列的后期干扰以防止孔形成——在各洲间得以保留。这意味着单靠 PFam54 蛋白的补体逃逸不能解释为何欧洲菌株更常与神经系统疾病相关。其他因素,如额外的表面蛋白、组织定位机制或宿主与蜱的生态差异,必然也参与其中。同时,该研究强调了一小组保守的蛋白形状和相互作用表面,它们对细菌在血液中的生存至关重要,因而是作为使细菌暴露于先天免疫防御下的药物或疫苗潜在靶点的有希望候选。
引用: Langhoff, L., Kapfer, P., Röttgerding, F. et al. Natural genetic variation impacts complement inhibitory activity of PFam54 orthologs of Asian Borrelia bavariensis. Sci Rep 16, 9080 (2026). https://doi.org/10.1038/s41598-026-43598-2
关键词: 莱姆病, 巴伐利亚伯氏疏螺旋体, 补体系统, 免疫逃逸, PFam54 蛋白