Clear Sky Science · zh
按处方剂量分层可改善基于深度学习的局部进展期NSCLC VMAT剂量预测
为何更聪明的放疗计划很重要
医生在用放疗处理进展期肺癌时处于一条紧绷的钢丝上:既要输送足够能量以控制肿瘤,又要保护周围脆弱的器官。设计这些计划既缓慢又复杂,很大程度上依赖于策划者的经验。本研究探索了人工智能如何预测胸部的放射剂量分布,并关键地展示了按处方剂量对训练数据进行分组能使其预测更准确、更具临床价值。
如何用聚焦光束治疗肺癌
多数局部进展期非小细胞肺癌患者无法通过手术切除肿瘤。相反,他们通常接受化疗并配合在胸部绕行旋转发射的高度整形化放射束,这种技术称为VMAT。目标是使肿瘤接受高且均匀的剂量,同时限制对肺、心脏、食管和脊髓的照射。实现这种平衡通常需要多轮试错式调整,耗时且可能延误治疗决策。如果医生能快速估计对某位患者现实可及的剂量分布,就能更早选择最佳治疗策略。
教算法识别剂量模式
研究者转向深度学习——一种能直接从影像中学习模式的人工智能方法。他们收集了72例接受VMAT治疗的肺癌患者的CT扫描和完成的治疗计划。对每位患者,他们重新计算了相同束列下三种不同的总剂量:50、54 和 60 灰(Gy,放射剂量的标准单位)。每个病例被转换为一个三维网格,标注肿瘤、关键器官以及基础CT影像。这九个通道的信息被输入到一个3D U-Net中,这是一种常见的神经网络结构,可基于解剖学学习剂量在体内的流动规律。
为何按处方剂量分组很重要
一个核心问题是如何处理患者被处方不同总剂量的事实。团队建立了四个在其他方面相同的AI模型。三个为“单一处方”模型,各自仅在一种剂量水平(50、54 或 60 Gy)的计划上训练。第四个模型则将50 Gy 与 60 Gy 的病例混合训练,但未告知网络当前样本的处方。当在新患者上测试时,按处方分开的模型在匹配肿瘤真实剂量方面表现更佳,既能保持覆盖度又能控制高剂量热点,与临床计划通常相差仅几 Gy。相比之下,混合模型在肿瘤高剂量区域及脊髓周围出现了明显更大的误差,而脊髓剂量必须保持在严格的安全限值以下。
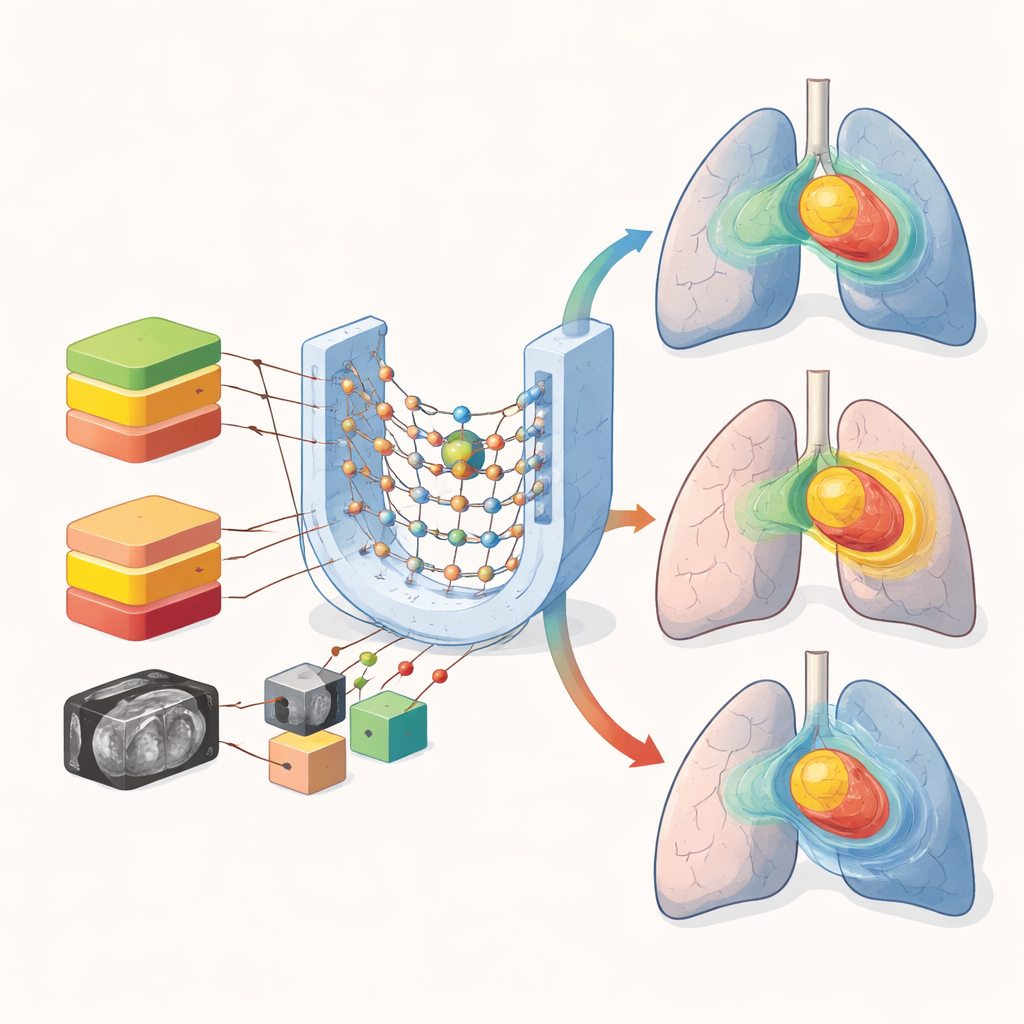
在加速计划的同时保护重要器官
有趣的是,对于肺、心脏和食管等许多器官,混合模型与分层模型的表现相近。这些较大结构的平均剂量误差在各方法间都保持适中。混合处方的主要弱点出现在像脊髓这样的小而敏感的结构上,在这些部位需要陡峭的剂量下降。对预测剂量图的目视检查显示,所有模型都能捕捉肿瘤内高剂量区的总体形状,但混合处方会在陡变梯度处和肺部低剂量区导致更多模糊。这些在数值上虽细微的差异,在医生判断更高处方是否安全时可能具有重要意义。
对患者和临床的意义
对患者而言,这项工作并不能取代临床系统中已有的精确剂量计算,但它能帮助把时间和精力集中在那些真正可行且安全的计划上。研究表明,按处方剂量对训练数据分组能显著提升AI预测的精确性——尤其是在肿瘤覆盖和脊髓保护方面——这突出了一个实用的设计选择,可让计算机辅助更值得信赖。经过在更大且更多样化患者群体中的进一步测试,此类模型有望成为日常工具,为医生提供基于解剖的快速预览,帮助权衡放射治疗的利与弊,从而支持更好、更一致的治疗计划制定。
引用: Chaipanya, T., Nimjaroen, K., Chamchod, S. et al. Prescription‑dose stratification improves deep learning‑based VMAT dose prediction in locally advanced NSCLC. Sci Rep 16, 8707 (2026). https://doi.org/10.1038/s41598-026-43192-6
关键词: 肺癌放疗, 深度学习剂量预测, VMAT 计划, 治疗计划优化, 危及器官