Clear Sky Science · zh
膳食模式影响双歧杆菌Bifidobacterium adolescentis HD17T2H及其他人类肠道细菌的体外(in silico)GABA产能
为何你的晚餐可能影响你的情绪
很多人听说过肠道像“第二大脑”,但我们仍不清楚饮食如何塑造那片隐藏的微生物世界,进而影响我们的心理与消化健康。本研究聚焦一种关键信使——γ-氨基丁酸(GABA),这是一种可抑制神经活动的化学物质,不仅在大脑中合成,肠道细菌也能产生。研究者提出了一个看似简单的问题:如果你改变饮食,肠道微生物产生GABA的能力会如何变化?
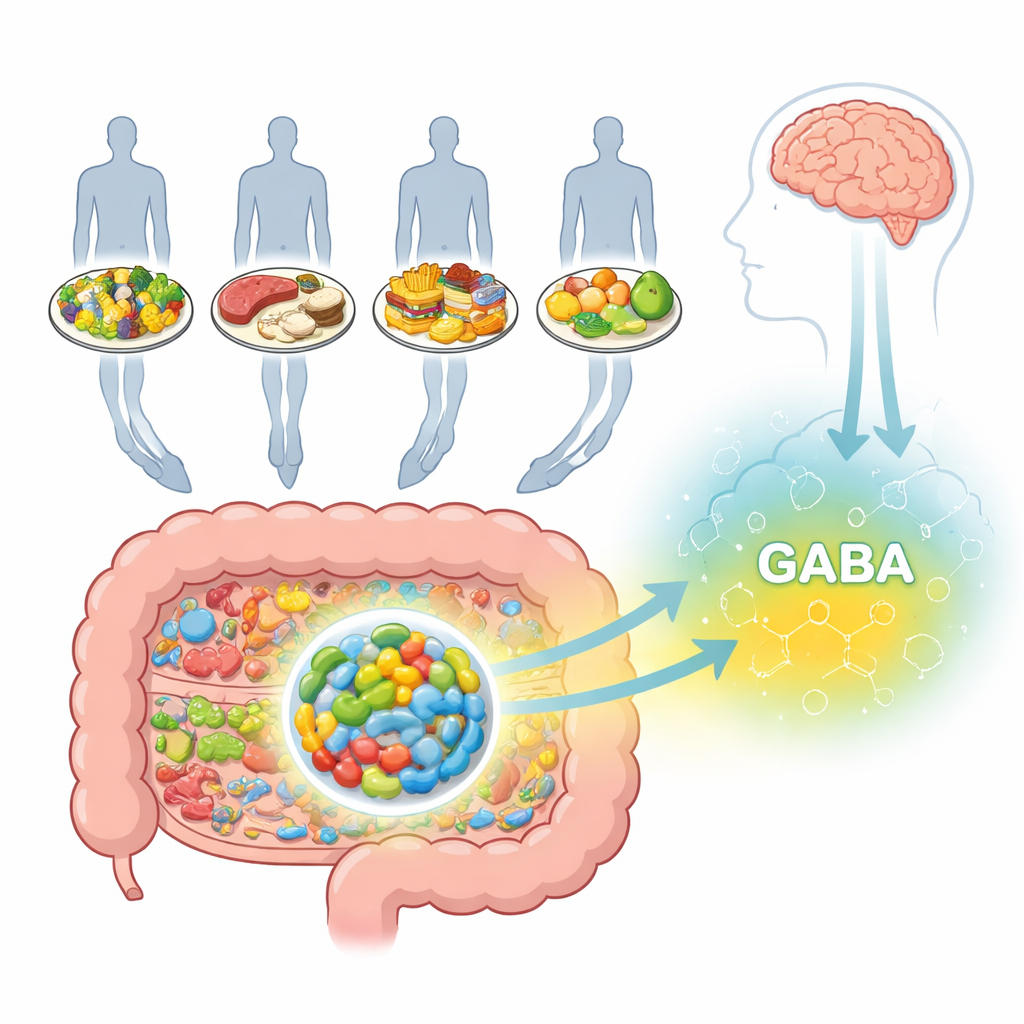
肠道中产生的镇静化学物质
GABA在大脑中最为人所知,作为一种抑制性信号,它有助于防止神经元过度兴奋,并与焦虑和抑郁有关。但GABA在肠道内也具有活性,会影响肠道运动、液体分泌和激素释放。一些肠道细菌可以通过已知的生化途径将常见营养物转化为GABA。其中一种微生物,Bifidobacterium adolescentis HD17T2H,是突出的GABA产生者,属于常见于益生菌产品的一类细菌。然而直到现在,科学家尚未系统地了解不同饮食模式如何改变该细菌合成GABA的能力。
用计算模型作为虚拟肠道
研究团队没有进行大量耗时的实验室实验,而是基于B. adolescentis的基因组建立了详细的计算模型。随后他们用十一种来自营养数据库的现实全日饮食“喂养”这个虚拟微生物,包括素食、纯素、高蛋白、欧洲平均、地中海、低碳和生酮等模式。借助估算营养物在代谢中流动的数学工具,研究者计算了在每种饮食下该细菌原则上可以分泌多少GABA,同时仍能维持生长。他们还进行了数千次虚拟“补充”测试,在计算环境中额外添加单一营养物,以观察哪些物质最能提高GABA产出。
不同饮食如何塑造GABA潜力
模拟结果显示,不同饮食模式之间存在显著差异。在基线条件下,素食饮食赋予该细菌最高的GABA产生潜力,其次是高蛋白饮食和为2型糖尿病设计的饮食。相反,生酮(极低碳水)饮食产生的基线GABA输出最低,纯素饮食也处于较低水平。当团队人为增加单一化合物的供应时,两类营养物始终能将GABA产量推高:碳水化合物和富含氮的分子,尤其是氨基酸。在低碳饮食中,添加类糖化合物的影响最大,表明碳能量是限制因素。相反,在碳水丰富的饮食(如素食和纯素)中,额外的氨基酸及相关氮源影响最大,表明此时氮成为瓶颈。
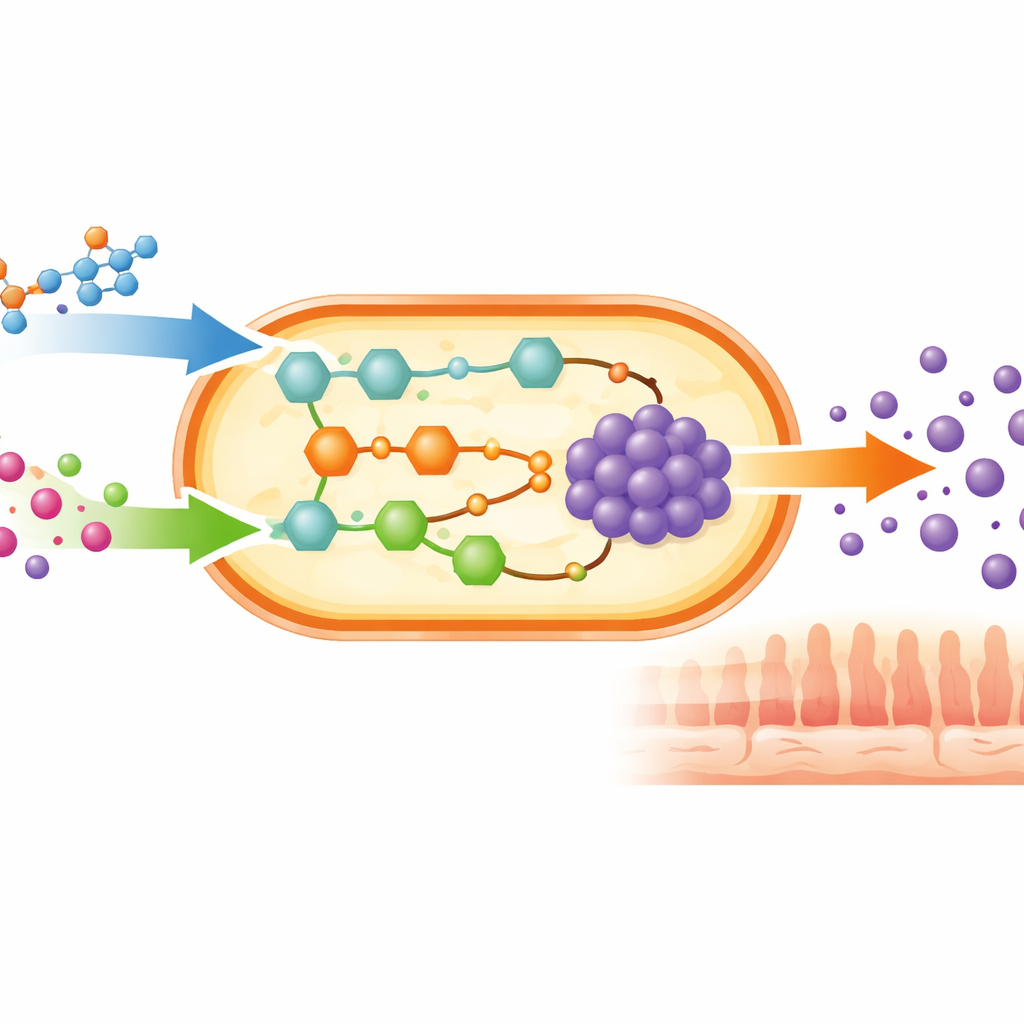
超越单一细菌的视角
为考察这些发现在人群中的潜在表现,研究者使用了来自基尔(Kiel)队列中一千多名成人的详细饮食记录。对每个人,他们计算了其体内B. adolescentis群落根据报告的营养摄入理论上可以产生多少GABA。机器学习方法确认,氨基酸远为最重要的饮食驱动因子,其次是其他含氮化合物、某些糖类、脂肪酸以及帮助酶发挥作用的B族维生素。团队随后将建模扩展到同一队列的整个微生物群,使用了大型肠道微生物模型库。他们发现有87种细菌菌株、分布于47个属,具备生产GABA的能力,既包括有益定居民也包括潜在病原体,强调GABA产生是肠道生态系统中一种广泛的生存策略,而非少数“好”微生物的专属特征。
这对健康与未来研究意味着什么
总体而言,研究表明肠道细菌产生GABA的能力对饮食高度敏感,且关键受限营养物取决于整体饮食模式:在低碳环境中以富含碳的糖类为限制因子,在高碳环境中以富含氮的构建模块为限制因子。这并不意味着人们应当通过大量摄入糖或蛋白质来追求更高的GABA水平——例如高糖饮食与健康风险相关,可能尽管影响微生物也会加重情绪障碍。相反,这项工作提供了一张关于哪些营养物对微生物GABA生成最重要的机制图谱,并强调许多肠道物种,而非仅经典益生菌,可能对这一镇静化学物质有所贡献。未来的实验室与临床研究需要检验这些体外(in silico)见解如何转化为真实世界的肠脑功能变化,以及是否可以通过精心设计的饮食或补充剂安全地利用微生物GABA产生来支持心理与消化健康。
引用: Homscheid, A., Moors, K.A., Nap, B. et al. Dietary patterns influence the in silico GABA production capacity of Bifidobacterium adolescentis HD17T2H and other human gut bacteria. Sci Rep 16, 8961 (2026). https://doi.org/10.1038/s41598-026-43006-9
关键词: 肠道微生物组, GABA, 膳食模式, 青年双歧杆菌, 肠脑轴