Clear Sky Science · zh
PGE2通过NOS2调节MC3T3-E1细胞的铁死亡和成骨
为什么矫正牙齿会影响你的骨骼
托槽和透明矫治器不仅仅移动牙齿——它们促使每颗牙齿周围的骨组织发生重塑。这种缓慢的生物学构建工作正是正畸治疗常常需要数年时间的原因之一。本研究深入成骨细胞,探讨一种常见的炎性信号前列腺素E2如何既可能加速牙齿移动,又可能在不显山露水间削弱新生骨质,为未来使正畸疗程更快且更稳定的策略提供线索。
推牙时释放的信号
当正畸医师对牙齿施加力时,牙根周围的韧带和骨组织会经历一种可控的损伤。该区域的细胞会释放化学信使,包括前列腺素E2,帮助协调牙齿一侧的骨吸收与另一侧的骨重建。作者聚焦于被称为成骨细胞的成骨细胞群,使用标准的小鼠细胞系作为模型,研究前列腺素E2如何影响细胞内两项关键结果:它们构建矿化骨的能力,以及它们发生一种新近发现的、依赖铁的细胞死亡形式——铁死亡的倾向。
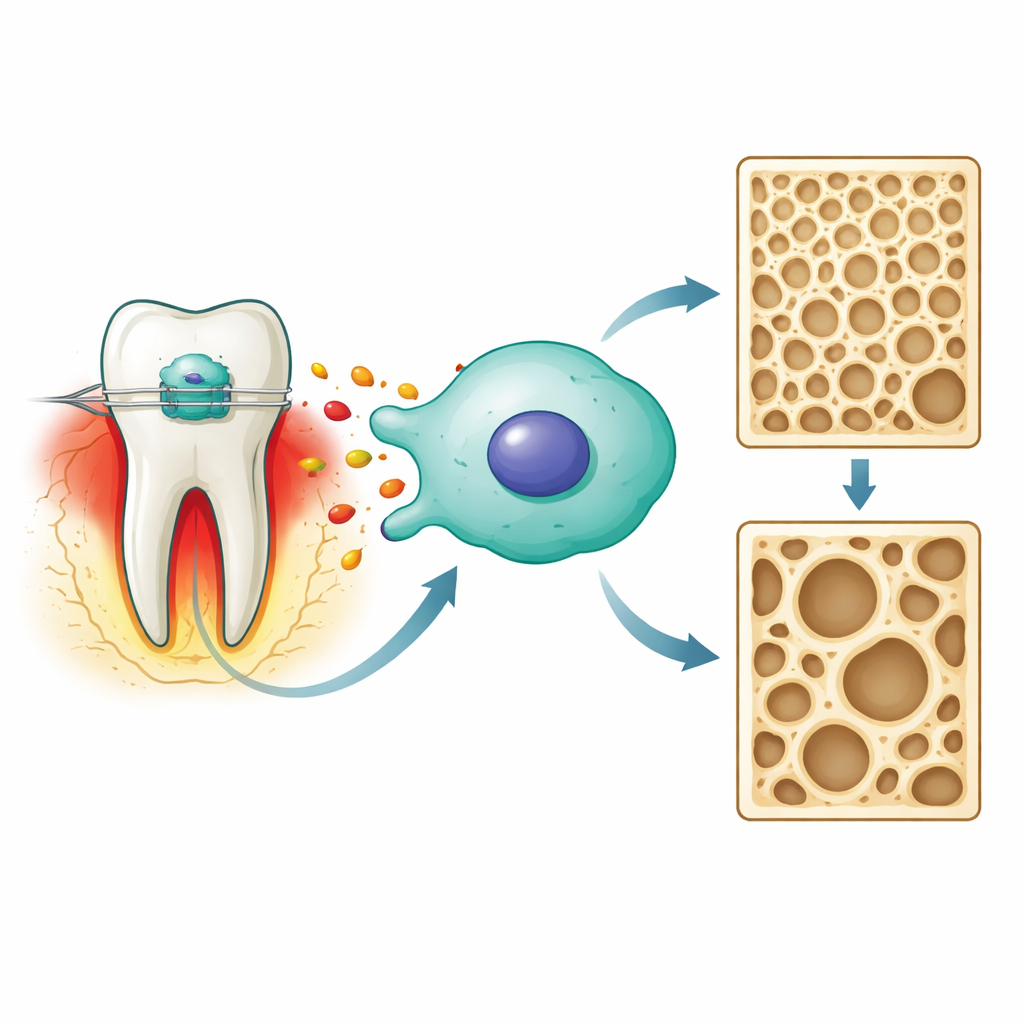
以单一酶为中心的应激通路
研究团队先利用正在发生牙齿移动的大鼠的基因数据,寻找同时与正畸力和铁死亡相关的分子。一个候选者——称为诱导型一氧化氮合酶2(NOS2)的酶——突出了其中心枢纽的地位。在体外实验中,用临床相关剂量的前列腺素E2处理类成骨细胞,产生了一种“无菌性”炎症状态——没有病原体,只有机械应激。在这一信号下,NOS2水平上升,其他应激标志物和有害的活性氧分子增加,而保护性的抗氧化与铁处理蛋白下降。总体来看,这些变化是细胞内铁死亡启动的特征性表现。
当造骨者关闭开关
相同的前列腺素E2处理还降低了细胞的成骨表现。经典的成骨标志物下降,可视化早期骨样矿化和关键酶碱性磷酸酶的检测显示染色变弱、矿沉积减少。当研究者加入已知可阻断铁死亡的药物ferrostatin-1时,这些损害大多被逆转:氧化应激减轻,铁死亡信号被抑制,成骨活性恢复。这提示,在该模型中,炎性信号通过驱动细胞走向铁死亡,部分阻碍了骨形成。
像开关一样上下调NOS2
为了判断NOS2是旁观者还是主动驱动因子,研究组在基因水平上上调和下调其表达。降低前列腺素处理细胞中的NOS2会减弱铁死亡标志、降低氧化损伤并将成骨行为恢复到接近正常水平。过表达NOS2则产生相反效果:加剧应激并进一步抑制成骨特征。值得注意的是,单纯增强NOS2——无需加入前列腺素E2——就足以触发类似铁死亡的变化并抑制成骨。这表明NOS2不仅是对炎症的响应者;它本身就能推动成骨细胞远离形成坚固矿化骨的路径。
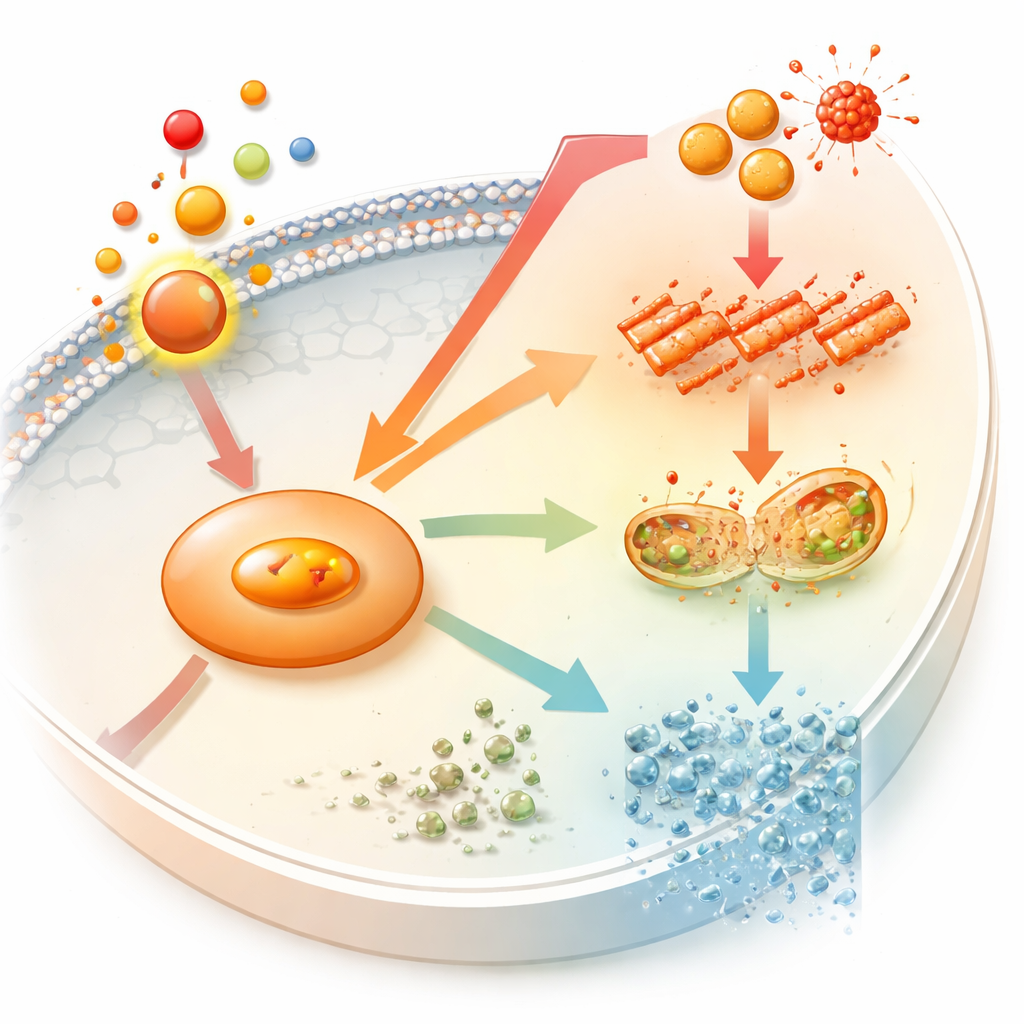
这对未来正畸意味着什么
这些实验合在一起勾勒出牙齿移动期间骨生物学中的一条新轴线:前列腺素E2上调NOS2,NOS2助长氧化损伤与铁死亡,导致成骨能力下降。对于患者而言,这并不意味着戴牙套不安全,但可以解释为何治疗需要在快速移动牙齿与保护周围强健骨质之间取得微妙平衡。长期来看,能够微调NOS2活性或保护成骨细胞免受铁死亡的药物或材料,可能帮助正畸医生在缩短治疗时间的同时维持甚至改善支撑骨的质量和稳定性。
引用: Sun, M., Yang, Y., Pang, L. et al. PGE2 regulates ferroptosis and osteogenesis of MC3T3-E1 cells via NOS2. Sci Rep 16, 8893 (2026). https://doi.org/10.1038/s41598-026-43001-0
关键词: 正畸牙齿移动, 骨重塑, 铁死亡, 一氧化氮合酶, 成骨细胞功能