Clear Sky Science · zh
探讨细胞外囊泡在胶质母细胞瘤凝血与免疫调节中的双重作用
为何血栓在脑癌中重要
被诊断为胶质母细胞瘤——最具侵袭性的脑癌形式——的患者常面临一个意外危险:腿部或脑内的危险血栓。这些血栓可缩短生存期并使原本就严峻的治疗变得更复杂。本研究提出了一个简单但关键的问题:胶质母细胞瘤细胞为何使其周围的血液更易凝固?它们释放到血液中的微小颗粒如何重塑全身的免疫防御?
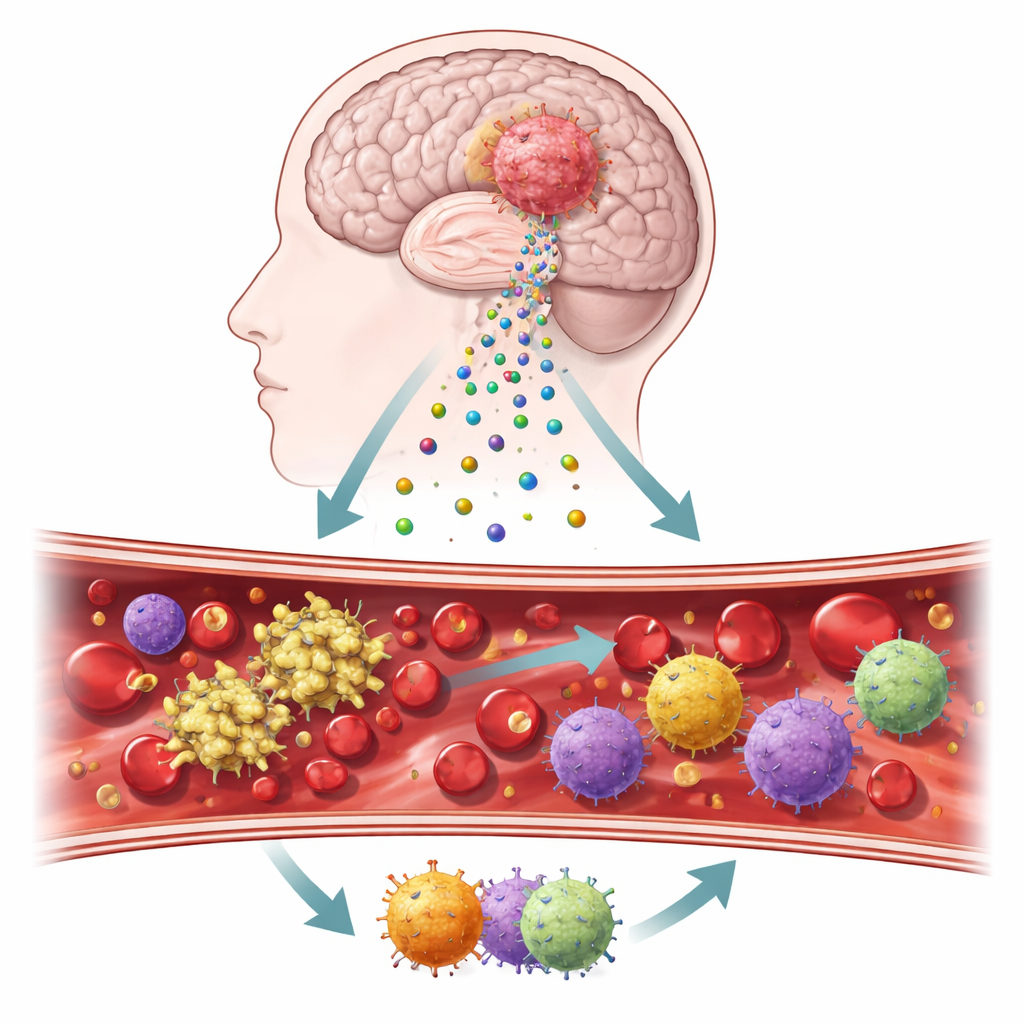
从脑肿瘤脱落的微小信使
研究人员将注意力集中在被称为细胞外囊泡的微观小泡上,这些小泡从肿瘤细胞出芽,漂浮在血液和脑组织中。这些囊泡表面携带两种关键蛋白——组织因子和podoplanin(血小板聚集相关蛋白)——已知可触发凝血并影响炎症。研究团队使用手术时采集的肿瘤样本、血液和从患者肿瘤培养的细胞系,建立了分步工作流程,以追踪这些分子在真实患者和受控实验室条件下的行为。他们还将肿瘤组织与正常脑组织进行比较,以评估这些与凝血相关信号的激活强度。
血流总体平静但肿瘤区已被激活
常规医院检测显示,术前许多患者的血液在表面上意外地接近正常:常见的凝血时间和血块强度值大多处于参考范围内。然而,当科学家检查肿瘤本身时,却呈现出不同的图景。胶质母细胞瘤组织持续显示出高水平的组织因子和podoplanin,同时天然抑制因子——组织因子途径抑制物水平很低。来自患者的肿瘤细胞系在培养皿中大体保留了这一特征,证实了这种“利凝血”特征是癌细胞的内在属性。当这些细胞或其释放的囊泡在实验室中与血浆混合时,凝块形成更快,尤其通过依赖组织因子的所谓外源性凝血途径。
不同肿瘤细胞,不同凝血策略
并非所有胶质母细胞瘤表现相同。一些来自患者的细胞系具有很高的组织因子,另一些则更多表达podoplanin,还有些两者都很少。富含组织因子的细胞在缩短凝血时间方面最为有效,而富含podoplanin的细胞则主要通过对血小板的影响发挥温和作用。当将某一细胞系分选为仅表达组织因子、仅表达podoplanin、两者兼具或两者皆无的亚群时,这些细胞并不会长时间保持该状态。在三周内,它们逐渐回归到混合表达谱,表明存在高度的可塑性。这种动态重塑伴随细胞内氧化应激的变化,提示肿瘤中的化学压力可能推动细胞朝向更促凝的状态。
囊泡如何塑造脑内与血液中的免疫
研究组进一步聚焦肿瘤来源囊泡对脑内免疫细胞(称为小胶质细胞)以及循环中的白细胞和中性粒细胞的影响。来自高度促凝肿瘤细胞系的囊泡易被小胶质细胞摄取,并减缓其迁移,同时促使其呈现更具炎性、类似“M1”表型及细胞衰老的特征。在血液中,富含组织因子的囊泡活化白细胞、增加活性氧(ROS)产生,并促进中性粒细胞释放被称为细胞外陷阱的粘性网状结构。携带podoplanin的囊泡在激发这些爆发式免疫反应方面作用较弱,但强烈促进一种类似衰老的程序,使免疫细胞停止分裂并改变行为。即便是不含这两种关键蛋白的囊泡仍能诱发一定程度的衰老,表明其他货物分子也起作用。
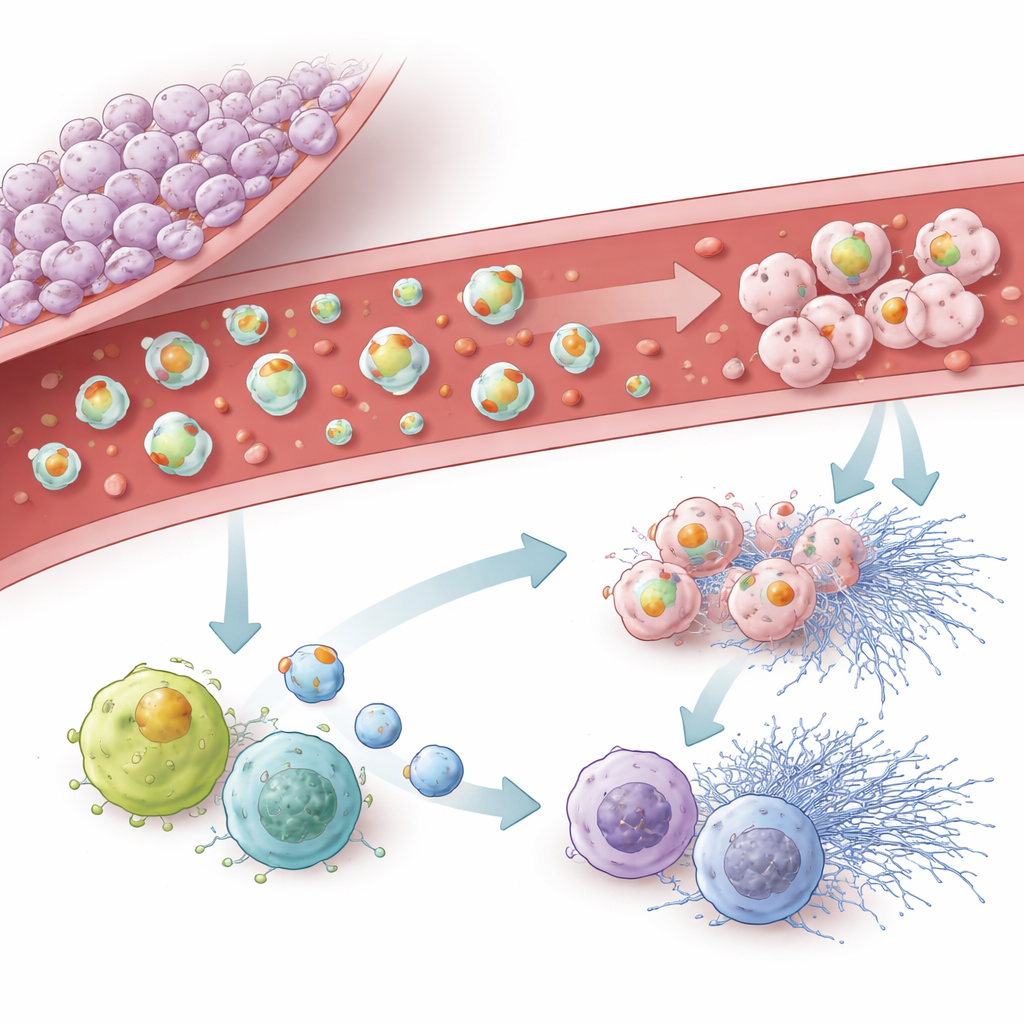
对患者和未来治疗的意义
综合来看,研究结果表明胶质母细胞瘤并非在全身范围内简单地使血液变稠。相反,肿瘤及其释放的囊泡在局部形成了一个高度复杂的区域,凝血和炎症互为推动力。组织因子是凝血形成和炎性激活的主要驱动因子,而podoplanin则通过影响血小板、免疫衰老和小胶质细胞行为发挥自身作用。由于这些囊泡在循环中存在并反映肿瘤状态,它们可能成为未来基于血液的标志,用以识别出特别易患血栓的患者。它们也可能指引更有针对性的预防策略,旨在抑制肿瘤的促凝机制,而不需广泛地稀释血液。
引用: Wolff, A., Waitz, G., Kaps, P. et al. Exploring the dual role of extracellular vesicles in coagulation and immune modulation in glioblastoma. Sci Rep 16, 9534 (2026). https://doi.org/10.1038/s41598-026-42867-4
关键词: 胶质母细胞瘤, 血栓, 细胞外囊泡, 肿瘤微环境, 免疫反应