Clear Sky Science · zh
评估结核分枝杆菌 dodecin 骨架作为 HPV L2 抗原多聚化平台对免疫原性的影响
这项研究对未来疫苗的重要性
人乳头瘤病毒(HPV)几乎导致所有宫颈癌,并在其他癌症中的占比日益增加,但现有疫苗制造复杂且并未覆盖所有危险病毒型。本研究探索了一种新的构建方式,旨在开发更简单、覆盖更广的 HPV 疫苗,期望能更便宜、更稳定并更易于在全球范围内使用,尤其是在中低收入国家。研究者通过重新安排关键病毒蛋白片段向免疫系统的呈现方式,试图诱导机体产生针对多种 HPV 型的强效抗体。
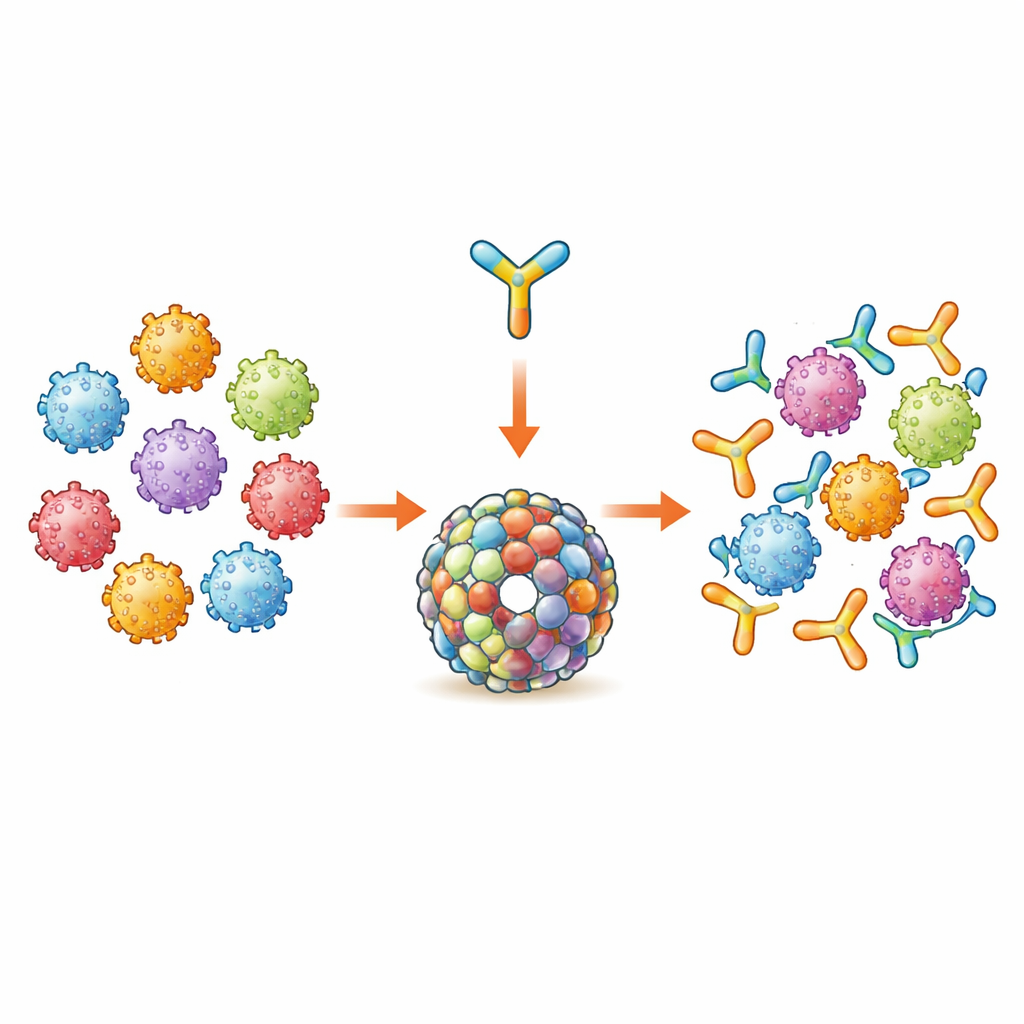
用于 HPV 保护的新构件
现有的 HPV 疫苗依赖一种称为 L1 的壳体蛋白,组装成类病毒颗粒,能强烈刺激针对疫苗中所含少数 HPV 型的抗体反应。研究团队则把注意力转向第二种病毒蛋白 L2,L2 含有在多种 HPV 型间高度保守的短片段,因此可以触发更广泛的保护。他们采用了先前设计的抗原 Trx-8mer,其中来自八种 HPV 型的小保守 L2 片段被拼接并展示在一个稳定的载体蛋白上。早期工作已显示,将七个 Trx-8mer 单元捆绑成环状复合体(名为 PANHPVAX 的疫苗)能产生强烈的交叉保护性抗体反应,目前正处于早期人体试验阶段。
把细菌蛋白变成疫苗平台
在本研究中,研究者试图超越七份拷贝的限制,将更多 L2 抗原装入每个颗粒,基于高度重复的展示模式对活化产生抗体的 B 细胞尤其有效的理论。他们选择了一种来自结核分枝杆菌的小型耐热蛋白 dodecin,该蛋白天然组装成由十二个相同亚基构成的空心球体。通过将 Trx-8mer 在基因上融合到 dodecin 上,他们制作了若干新的疫苗候选物,设计为自组装成多聚纳米颗粒,展示大量 L2 拷贝。这些颗粒可在细菌中表达,由于其稳健性可通过高温纯化,并通过多种生物物理方法验证形成了预期的纳米结构。
直接融合并非万无一失
出人意料的是,简单地将 L2 货载直接连接到 dodecin 骨架,并未在小鼠中优于现有的七聚体参照疫苗 PANHPVAX。尽管多聚颗粒按预期形成并且能诱导针对疫苗内与疫苗外 HPV 型的中和抗体,但滴度通常低于 PANHPVAX。在疫苗中加入内建的辅助 T 细胞表位(有时可增强抗体反应)也未能改善性能。结构建模和功能数据提示,体积较大的直接融合 Trx-8mer 单元可能相互挤压,掩蔽了对 B 细胞受体重要的 L2 区域,从而削弱了免疫反应,即便理论上抗原拷贝数更多。
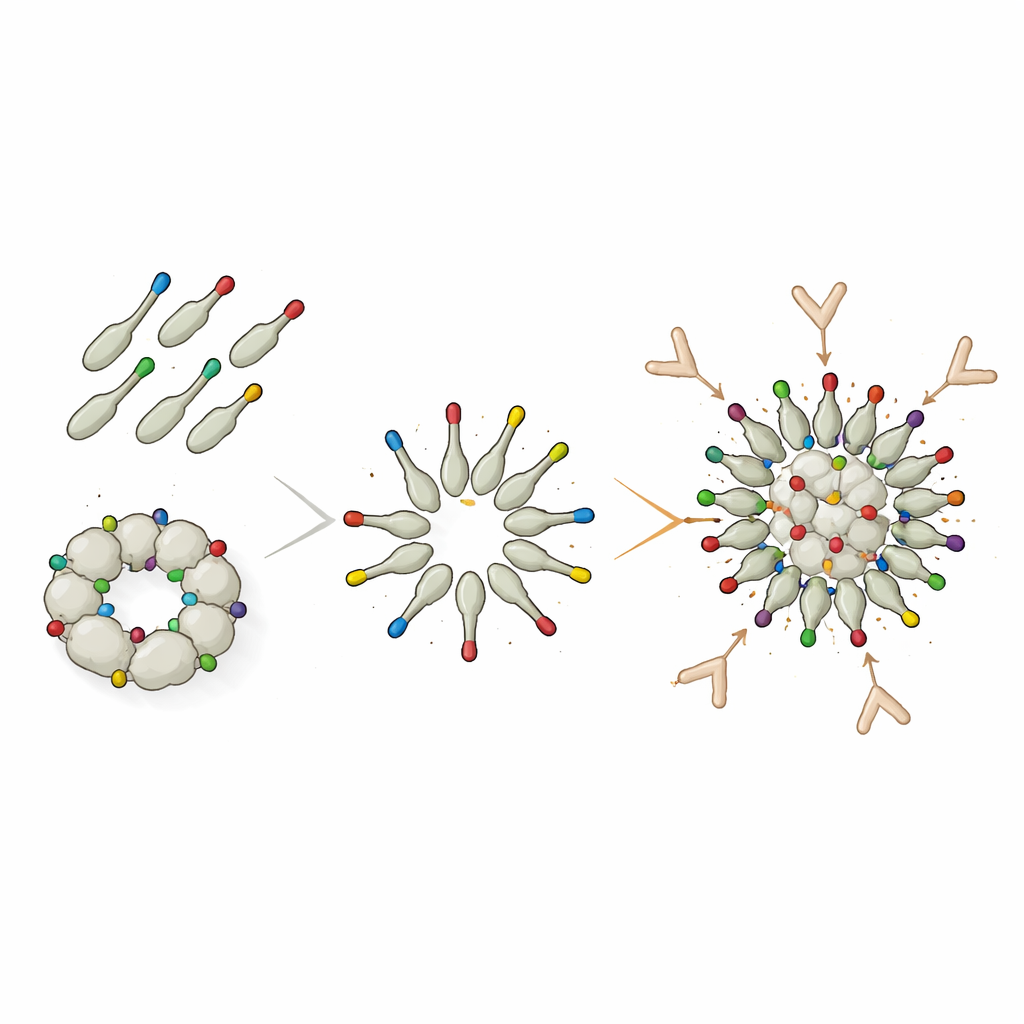
“点击式”修饰显著增强免疫反应
为克服这些结构限制,团队转而采用一种模块化的“蛋白胶”体系,称为 DogTag/DogCatcher。在该设计中,先制备仅在表面带有微小 DogTag 肽的 dodecin,使其能自由组装成整洁的纳米颗粒。Trx-8mer 抗原则另行与匹配的 DogCatcher 伴侣融合。当混合时,Tag 与 Catcher 通过自发共价键锁合,将携带 L2 的 Trx-8mer 单元“扣”到预先形成的 dodecin 颗粒上。尽管只有约一半的 Trx-8mer 最终附着在颗粒上,其余仍以游离形式存在,接种这种修饰构建体的小鼠仍然对多种高危 HPV 型产生了远高于直接融合颗粒的中和抗体滴度。对于某些类型,如 HPV16,修饰颗粒甚至优于 PANHPVAX。
对廉价且广谱 HPV 疫苗的启示
总体而言,该研究表明抗原的空间排列可能比理论上的拷贝数更为关键。先组装稳固的纳米颗粒骨架,然后将抗原“扣”上去,能够为 L2 片段提供更有利的间距和朝向,从而在小鼠中诱导更强且更广的抗体反应。由于基于 dodecin 的颗粒体积小、热稳定性高且可在细菌中生产,它们是下一代 HPV 疫苗的有前景候选者,可能降低制造成本并减少对低温保存的依赖。通过进一步优化和测试,这一模块化平台可用于开发在单次可及接种中保护多种 HPV 型的疫苗,甚至可能改造为在同一纳米颗粒中组合预防性和治疗性成分。
引用: Kaplan, E., Mariz, F.C., Zhao, X. et al. Assessment of Mycobacterium tuberculosis dodecin scaffold as a multimerization platform on the immunogenicity of HPV L2 antigens. Sci Rep 16, 9086 (2026). https://doi.org/10.1038/s41598-026-42678-7
关键词: HPV 疫苗, 纳米颗粒免疫原, L2 抗原, dodecin 骨架, 蛋白质偶联