Clear Sky Science · zh
使用量化病理学对齿源性黏液瘤谱系病变进行多中心临床病理学研究
这对患者和牙医的重要性
在颌骨深处,罕见的肿瘤可能在数月或数年内悄然生长才被发现。这些被称为齿源性黏液瘤和黏液纤维瘤的病变不是癌症,但它们可以扩展、削弱骨质并增加手术难度。数十年来,病理学家主要凭肉眼判断这些病变,导致不同医院在描述和分类相同类型病灶时存在差异。本研究将强大的图像分析工具引入玻片检查,展示了人工智能(AI)如何帮助医生更清晰、一致地识别这些肿瘤。
外观极为相似的罕见颌骨肿瘤
齿源性黏液瘤和齿源性黏液纤维瘤起源于参与牙齿形成的组织。两者都是柔软、胶状的肿瘤,位于颌骨内部。在显微镜下,它们包含松散的粘液样区域与较致密的纤维带的混合体。传统上,病理学家试图通过估计肿瘤中纤维组织与黏液样成分的比例来加以区分。但这些肿瘤十分罕见,且尚无普遍认同的规则来界定多少纤维组织比例足以改变诊断标签。因此,即便患者症状和影像检查相似,不同医院也可能对非常相近的病变给予不同的名称。
将显微镜玻片转化为数字
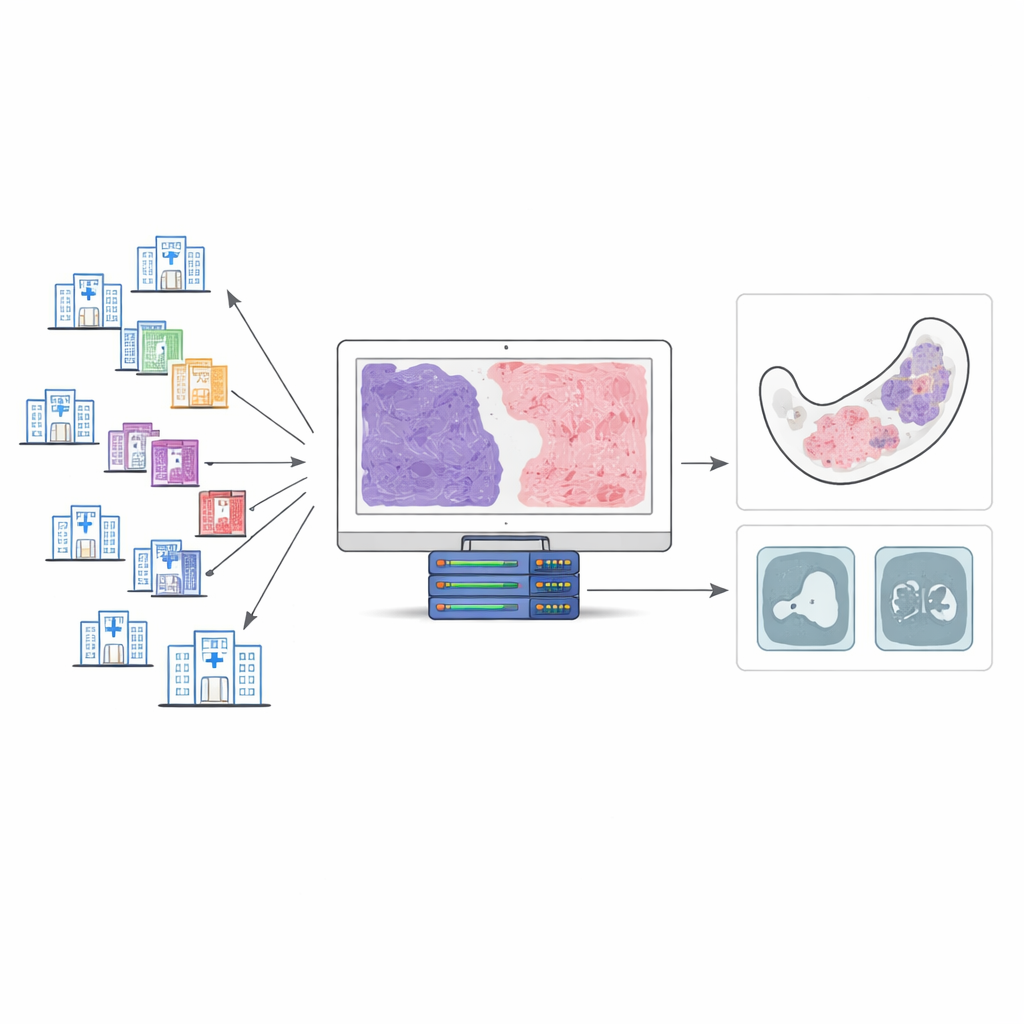
研究团队收集了来自34家医院、跨越二十年的143份组织样本,最终筛选出100例符合严格质量标准的病例。所有样本均采用一种特殊染色(Masson三色染色),该染色能将纤维组织与周围肿瘤区分开来。两位口腔病理学专家对每例进行了仔细审阅,并以10%为步长估计纤维组织的百分比。这些专家估计作为参考,用于训练一个AI系统以完全量化的方式自动执行同样的任务。
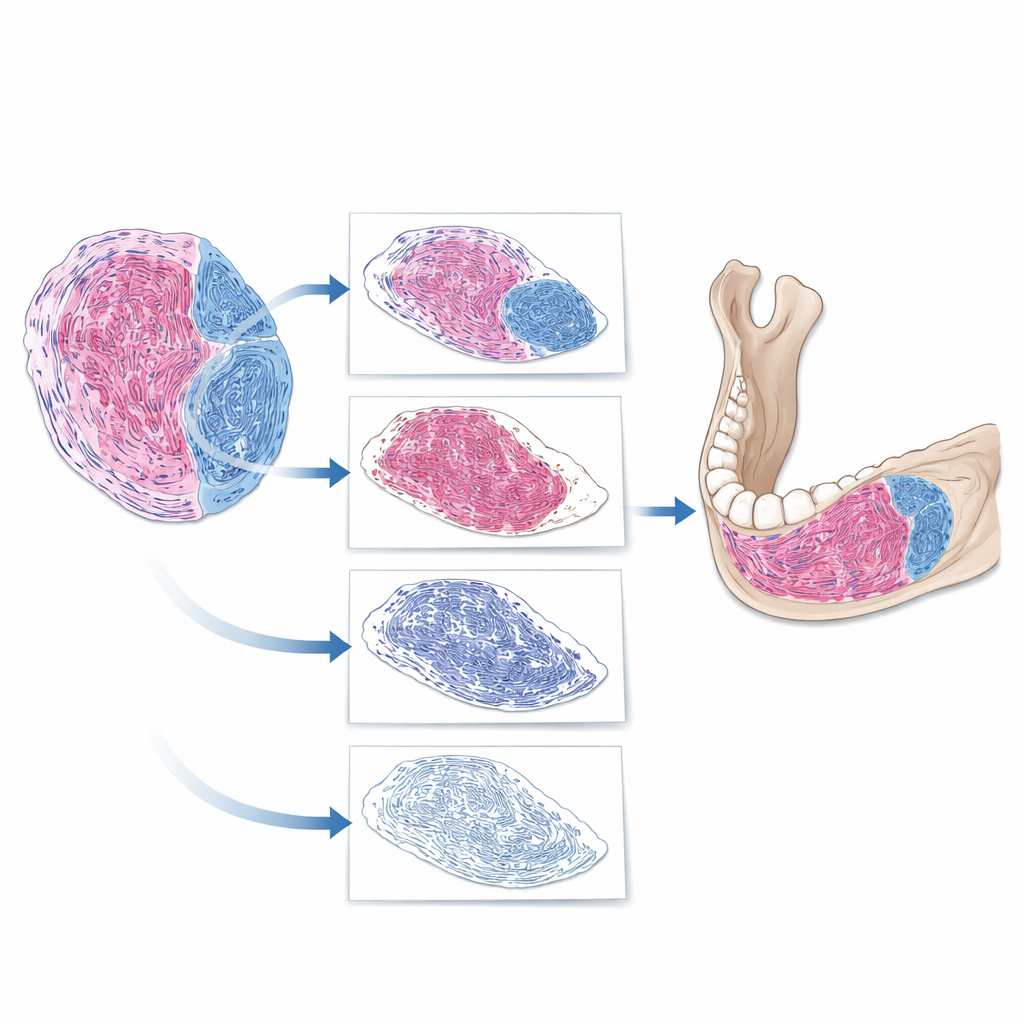
AI如何“解读”肿瘤切片
团队构建了一个逐步的数字化流程来分析整张玻片图像。首先,软件将真实组织与空白背景分离。接着,分离出肿瘤与邻近结构(如骨骼和牙齿)。最后,在肿瘤内部去除细胞核并聚焦剩余基质,识别出吸收纤维染色的区域。由此,AI 计算出纤维组织比例:纤维组织面积除以肿瘤总面积。当研究人员将AI生成的数值与专家评估进行比较时,两者一致性良好,大多数个例的差异约为10个百分点左右。这表明AI能够可靠地反映专家判断,同时以精确测量值替代粗略的印象。
纤维成分揭示肿瘤外观的含义
有了这些测量数据,研究者考察了纤维含量与临床及影像学特征的关系。他们发现纤维组织的比例在不同机构间差异很大,反映了病理学家最初命名肿瘤时的差异性。在观察影像特征时,出现了一个显著规律:在扫描中显示为单一腔室的病灶(单房性病变)通常比具有多个小腔室的病灶(多房性病变)具有更高的纤维组织比例。这与这样一种观念相符:更致密的纤维组织可能形成更为实质、单腔的肿块,而较松散、富含液体的组织则更容易分隔成多个空腔。
这对未来诊断和护理的意义
该研究并不旨在重新命名疾病或用机器取代病理学家。相反,它显示了基于AI的量化病理学能够为不同医院之间的罕见颌骨肿瘤提供一个共同的度量标准。通过将肿瘤组织的细微纹理转化为可重复的数字,这种方法揭示了日常诊断在多大程度上依赖主观判断,并提供了一种降低这种差异性的途径。对于患者来说,更一致的病变解读有助于支持更明确的治疗决定,并改善不同中心之间疗效比较。随着类似方法推广到其他罕见肿瘤,AI 辅助的显微镜检查可能在不知不觉中重塑病理学家的疾病视角——使其评估更具可比性,并最终在患者接受治疗的任何地点都更有用。
引用: Harazono, Y., Fukawa, Y., Iwasaki, T. et al. Multicenter clinicopathological study of odontogenic myxoma spectrum lesions using quantitative pathology. Sci Rep 16, 11221 (2026). https://doi.org/10.1038/s41598-026-42019-8
关键词: 齿源性黏液瘤, 颌骨肿瘤, 数字病理, 人工智能, 纤维组织比例