Clear Sky Science · zh
可视化恶性进展:基于原位 CD109 的空间免疫荧光检测在肿瘤微环境内描绘乳头状向未分化甲状腺癌的转化
这项甲状腺癌研究为何重要
未分化甲状腺癌是人类最致命的癌症之一,经常将通常可治愈的甲状腺肿瘤迅速演变为致命疾病。然而,临床上仍未完全弄清楚一种常见且生长缓慢的乳头状甲状腺癌如何会突变为这种侵袭性类型。本研究直接在患者肿瘤内追踪了这一转化,采用一种新的成像技术观察癌细胞及其周围“邻里”如何逐步变化。该研究提供了更细致的图景,说明肿瘤局部环境如何可能推动细胞走向更致命的状态,并提示了延缓或阻止这种转化的新思路。
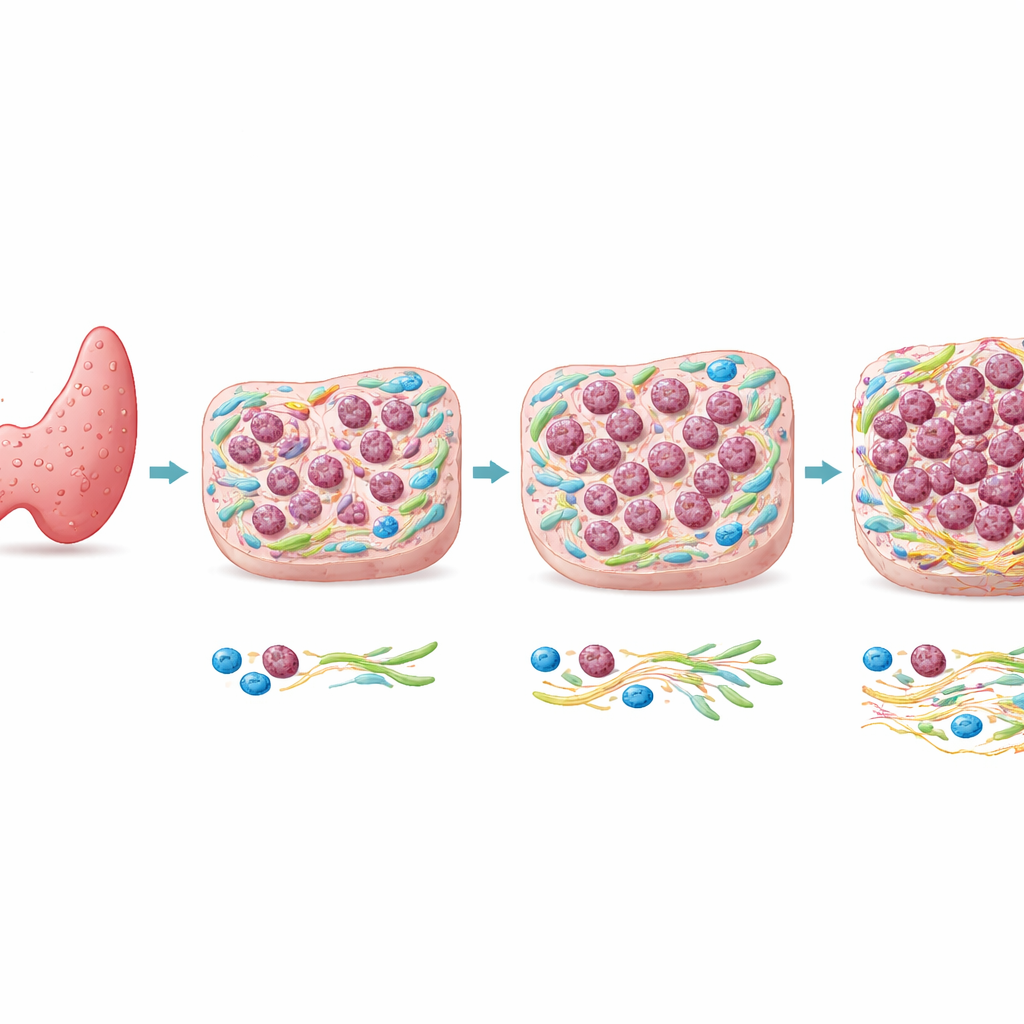
从常见肿瘤到罕见杀手
大多数甲状腺癌为乳头状甲状腺癌(PTC),通常生长缓慢且预后良好。相比之下,未分化甲状腺癌(ATC)罕见但常在数月内致死。遗传学研究显示,同一患者中相邻的 ATC 与 PTC 常常共享许多相同的 DNA 突变,包括已知的癌基因变化。这一相似性表明,仅靠基因变化可能无法解释为何肿瘤的某些区域会变为未分化。因此,作者将注意力集中在细胞周围的组织景观——肿瘤微环境上,探讨局部条件是否促成了这一危险的转变。
一种原位绘制肿瘤的新方法
研究团队开发了空间免疫荧光(SPI)检测,这是一种多色显微成像方法,可在组织切片的微小划分区域内测量特定蛋白的荧光强度。他们将该方法以 CD109 为核心——一种他们在甲状腺组织中识别出的与恶性行为相关的表面蛋白——以及 CK8/18,一种表征普通乳头状肿瘤细胞的蛋白。通过计算数百个小区域中 CD109 与 CK8/18 的比值,他们生成了色码化的地图,将典型的 PTC 区域与典型的 ATC 区域区分开来,并关键性地揭示了两者重叠的中间带。转变并非呈现锋利边界,而是以渐进且斑驳的连续体形式出现。
沿着变化路径的五个区域
为更好地理解这一连续体,研究者将组织划分为五个区域,从纯 PTC 到完全形成的 ATC。随后他们检查了许多额外的蛋白,这些蛋白能反映细胞身份、增殖、运动以及基质支持情况。在这些区域中,经典上皮特征如 E-cadherin 和 CK8/18 稳步下降,而与细胞运动性和形态改变相关的标志物(如波形蛋白)则上升。提示快速细胞分裂的蛋白在更未分化的区域增加。与此同时,周围的支持细胞——癌症相关成纤维细胞——以及免疫细胞,尤其是某些巨噬细胞,数量增多且更趋活化,它们产生的蛋白也有所增加。
当肿瘤支架变为敌对环境
肿瘤支架或细胞外基质发生了显著变化。在未分化区域,类似成纤维细胞的细胞沉积了更多的Ⅲ型和Ⅵ型胶原以及一种叫 TGFBI 的基质蛋白,这些纤维更粗、更纠结,方向多样而非平滑平行排列。这种重构的网络可能使组织力学上更为刚性。在这些较硬的区域,一种对压力敏感的信号蛋白 YAP 在癌细胞和支持细胞中更为活跃。相同的区域还显示出更多 DNA 损伤迹象和一种炎症性细胞死亡形式,并伴有 S100 蛋白的释放,这类蛋白可作为危险信号并进一步引发炎症。作者提出,这种压迫、细胞死亡和慢性炎症的组合,可能有利于那些已突变、能耐受应激并能经历类上皮-间质转变的癌细胞存活和扩散。
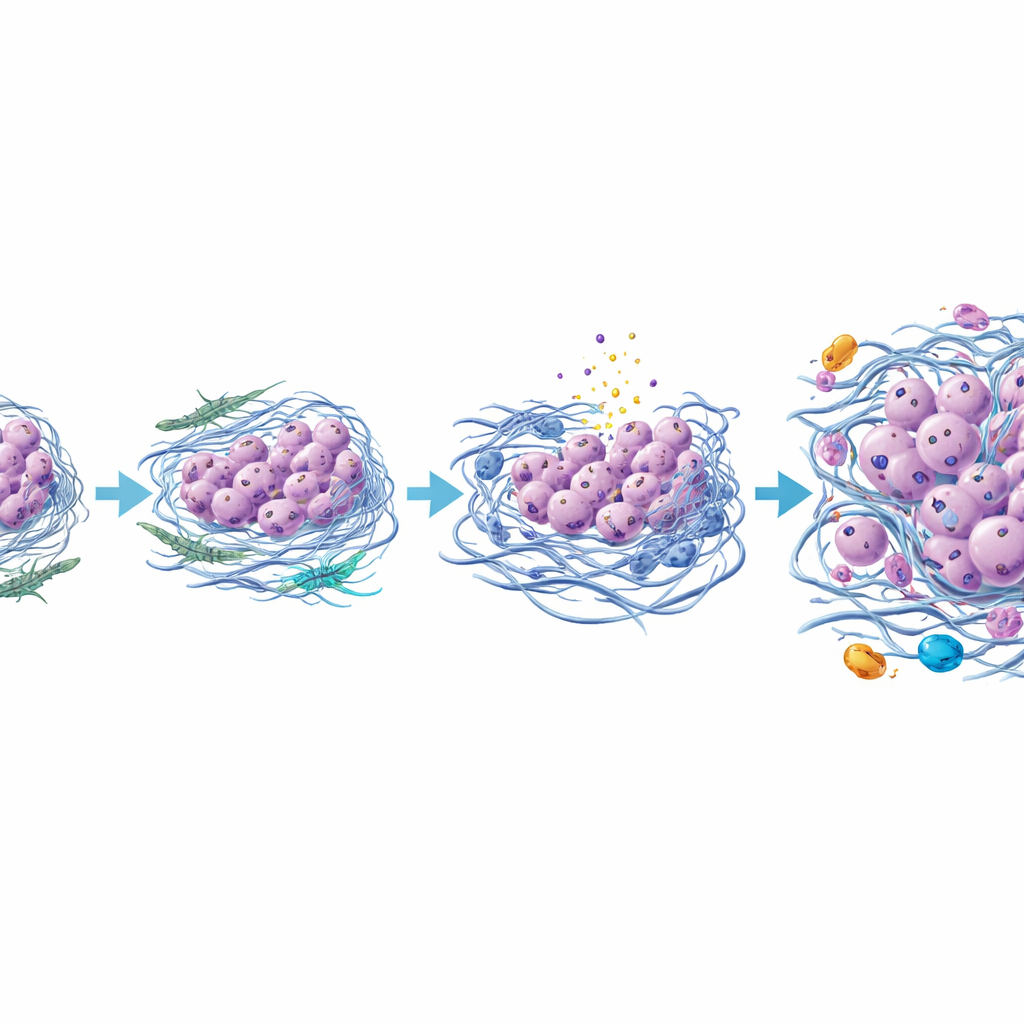
一种关于甲状腺肿瘤变得致命的新图景
综合这些发现,研究提示未分化甲状腺癌的出现不仅仅依赖于额外的基因突变,更与肿瘤周围邻里的重塑有关。当乳头状肿瘤细胞与邻近支持细胞相互作用时,部分成纤维细胞演变为更具攻击性的亚型,使周围基质增厚并变硬,压迫易感细胞致死,并招募炎性免疫细胞。存活下来的更具韧性的癌细胞逐步失去原有的甲状腺特征,获得更具运动性和侵袭性的身份,最终形成未分化肿瘤。尽管这项工作基于单例详尽研究,仍需在更多患者中验证,但它引入了一种强大的成像工具和一个详细模型,其中针对肿瘤的支持细胞、基质或炎症信号可能有助于预防或延缓甲状腺癌中最令人担忧的转化之一。
引用: Cohen, T., Suzuki, K., Matsuda, K. et al. Visualizing malignant progression: in situ CD109-based spatial immunofluorescence assay delineates papillary to anaplastic thyroid carcinoma transformation within the tumor microenvironment. Sci Rep 16, 8682 (2026). https://doi.org/10.1038/s41598-026-41927-z
关键词: 未分化甲状腺癌, 乳头状甲状腺癌, 肿瘤微环境, 细胞外基质刚性, 空间免疫荧光