Clear Sky Science · zh
使用常规、成像和纳米流式细胞术技术分析支气管上皮细胞来源的胞外囊泡
为什么肺里的微小“气泡”很重要
我们的肺由不断与免疫系统“对话”的细胞覆盖,尤其是在吸入灰尘、污染或病原体时。这种“对话”很大程度上通过被称为胞外囊泡的显微小囊泡进行——由细胞释放的脂质和蛋白质包裹体。这些囊泡可以加重或缓解肺部疾病,未来可能作为哮喘、慢性阻塞性肺病(COPD)和纤维化等疾病的早期预警信号。本研究探讨如何使用不同类型的先进激光仪器来测量这些难以捉摸的颗粒,目标是将这些测量变得对研究和未来临床检测更为实用。
来自气道细胞的隐形信息
胞外囊泡(EVs)是几乎所有细胞释放到血液、尿液以及覆盖气道的薄液层中的微小膜囊。来自人体支气管上皮细胞——覆盖气道的细胞——的EV已与多种肺功能相关:它们能影响过敏的发展、帮助抵抗肺部感染、在COPD中塑造气道结构,甚至限制肺组织的瘢痕形成。由于它们携带来自母细胞的蛋白、脂质和遗传物质片段,EV可作为肺部健康或疾病的指纹,甚至有望自身成为治疗手段。挑战在于它们体积极小、异质性高且数量稀少,导致难以准确观察和计数。
超越缓慢且分散的检测方法
传统上,科学家依赖几种独立的方法来研究EV。超速离心或尺寸排阻色谱用于分离;纳米颗粒追踪分析(NTA)根据颗粒运动估算大小和数量;电子显微镜提供详细图像。尽管这些方法强大,但速度慢、劳动强度大,不适合常规或临床使用。关键是,它们难以判断每个囊泡携带了哪些特定蛋白。流式细胞术——一种广泛用于分析血液和免疫细胞的技术——提供了更为简化的替代方案。它让颗粒逐个通过激光,测量光散射(与大小相关)和荧光(来自染料或抗体)。近期的仪器设计有望将流式细胞术推进到最小囊泡的尺度,从而有可能让一台设备在一次运行中完成囊泡的定尺寸、计数和特征描述。
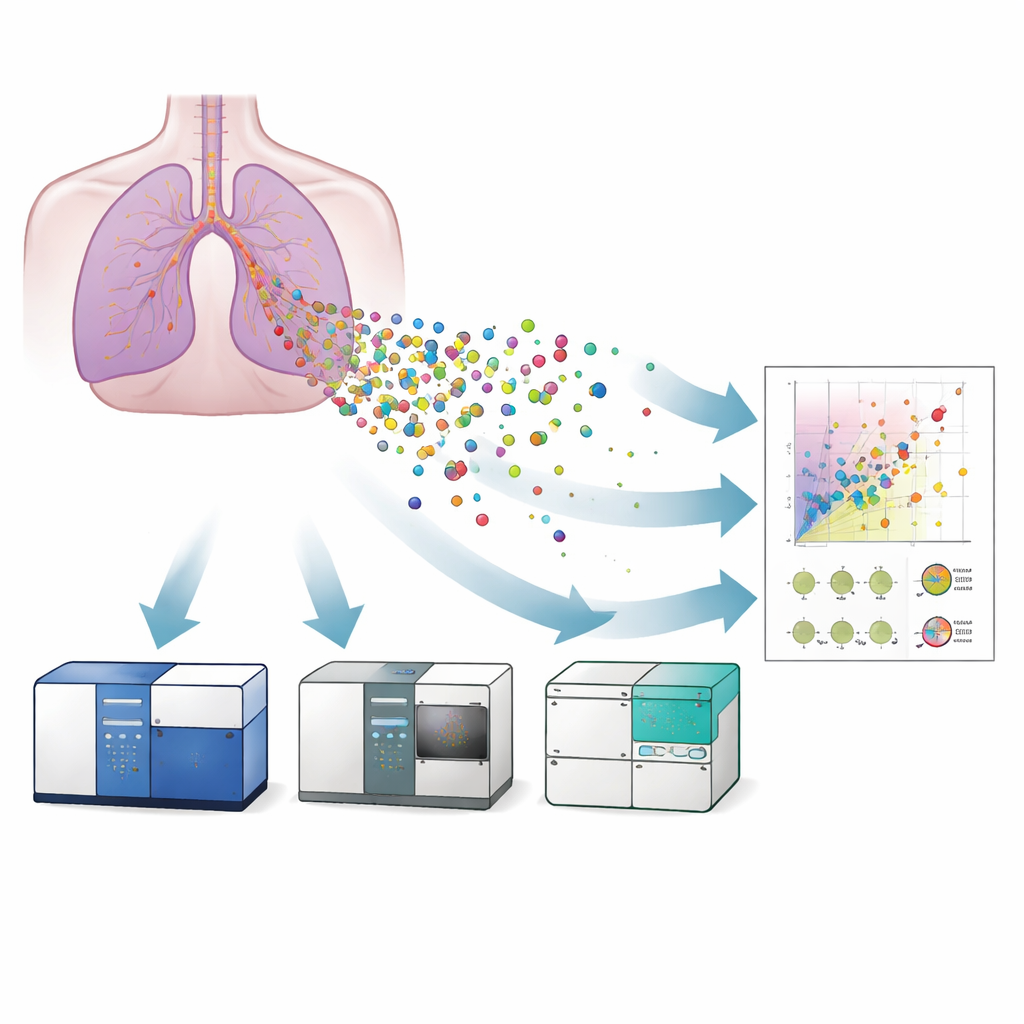
三台仪器,共同目标
研究者比较了三种用于研究来源于体外培养的人类支气管上皮模型的EV的流式细胞术类型:常规流式细胞仪、成像流式细胞仪和纳米流式细胞仪。首先,他们使用电子显微镜和超分辨率显微镜确认了囊泡的存在及其典型形态,并显示囊泡携带称为四跨蛋白(CD9、CD63、CD81)的表面蛋白——这些是识别EV的常规标记。随后,他们用经过校准的参考微球和脂质体标准将每台仪器的光学信号转换为近似的囊泡尺寸。纳米流式细胞仪可检测到约40纳米大小的囊泡,成像仪器可到约55纳米,而常规仪器在约120纳米以下检测力较弱。这意味着只有更灵敏的系统才能完整捕获最小且可能在医学上最为相关的囊泡。
标记与计数囊泡
为了确保测量的是完整且具有生物学活性的囊泡而非碎片,团队使用了一种名为calcein-AM的染料。该染料只有在穿过完整膜并被囊泡内部的酶处理后才会发光。研究人员仔细调整染料浓度,使其在标记囊泡时信号强烈且背景最小,选择了在样品稀释系列中呈现清晰线性响应的浓度。随后将calcein与针对囊泡表面四跨蛋白的荧光抗体结合,使仪器能够区分携带不同标志组合的囊泡。研究组还测量了每台设备对这些荧光标签的灵敏度——即囊泡上需要存在多少抗体分子才能被可靠检测到。成像流式细胞术通常比常规仪器提供更低的检测阈值,因此更适合检测仅携带少量标志蛋白的颗粒。
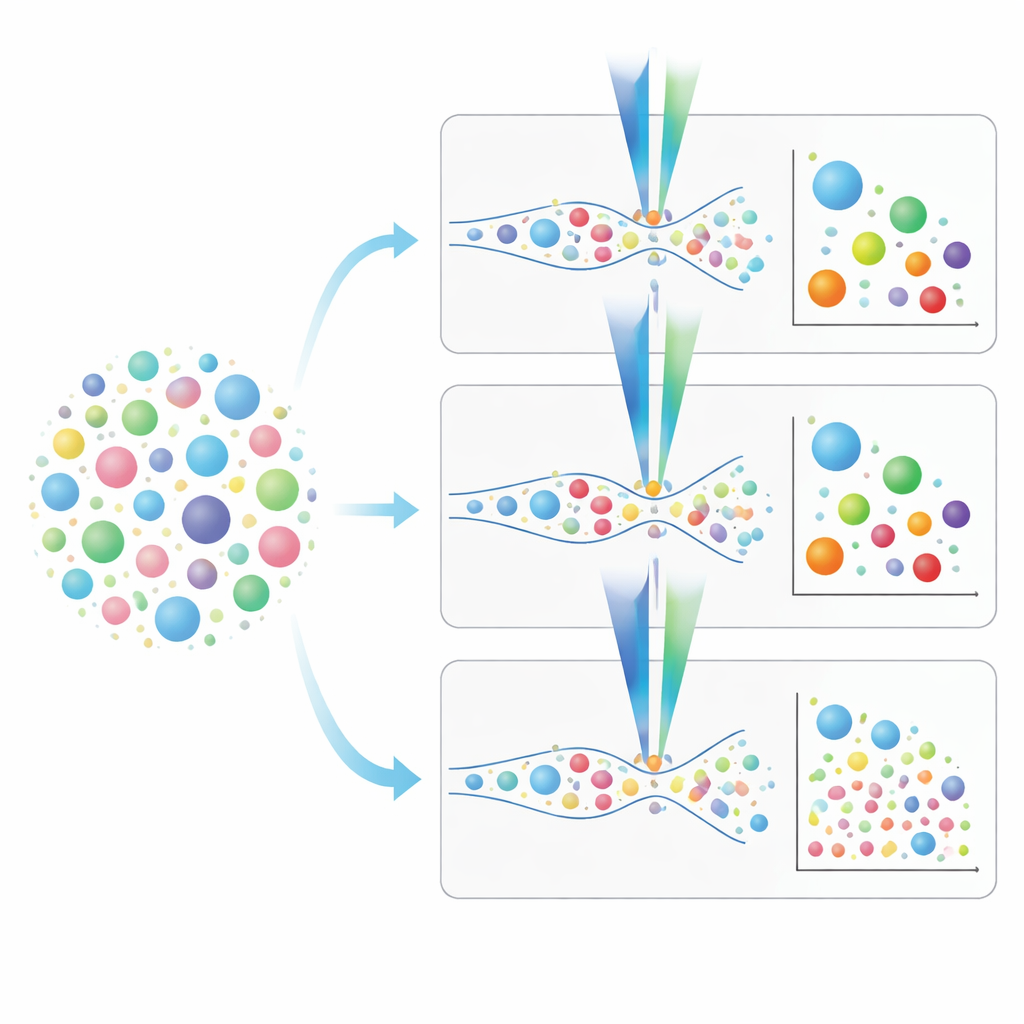
为肺囊泡研究选择合适工具
通过这次正面比较,得出了一幅实用的图景。常规流式细胞仪速度更快,能在不事先分离样本的情况下进行分析,但它们会漏掉许多可能携带关键疾病信号的最小囊泡。成像和纳米流式细胞仪虽然速度较慢,而且纳米仪器更依赖于预处理清理样本,但它们能检测到更小的尺寸并支持更丰富的囊泡表面标志“指纹”分析。作者列出了逐步的染色和校准策略,强调了解每种荧光标签检测限的重要性,并展示了如何避免来自也会标记碎片或非囊泡颗粒的染料产生的误导信号。通俗地说,他们为研究者提供了一条路线图,帮助决定哪种仪器和方案最适合其肺EV研究问题,从而推进将这些显微信使作为理解、诊断并最终治疗呼吸系统疾病的实用工具的目标。
引用: Hopkins, G., Browne, W., Tucis, D. et al. Bronchial epithelial cell-derived extracellular vesicle analysis using conventional, imaging, and nanoscale flow cytometry technologies. Sci Rep 16, 11162 (2026). https://doi.org/10.1038/s41598-026-41848-x
关键词: 胞外囊泡, 肺上皮, 流式细胞术, 呼吸系统疾病, 生物标志物分析