Clear Sky Science · zh
使用MR温度成像对微波消融术协议优化的离体定量评估:目标温度与消融时长
实时观察肿瘤治疗
当医生用热能消除肝脏肿瘤时,希望在治疗过程中准确看到器官哪些部位被破坏。磁共振成像(MRI)提供了一种“看到体内温度”的方法,随着热量扩散可以显示温度变化。本研究探讨在微波消融过程中,医生在保持MRI温度图清晰可靠的情况下,能够安全加热肝组织到何种温度及持续多长时间——这是朝着更精确、更微创的癌症治疗迈出的重要一步。
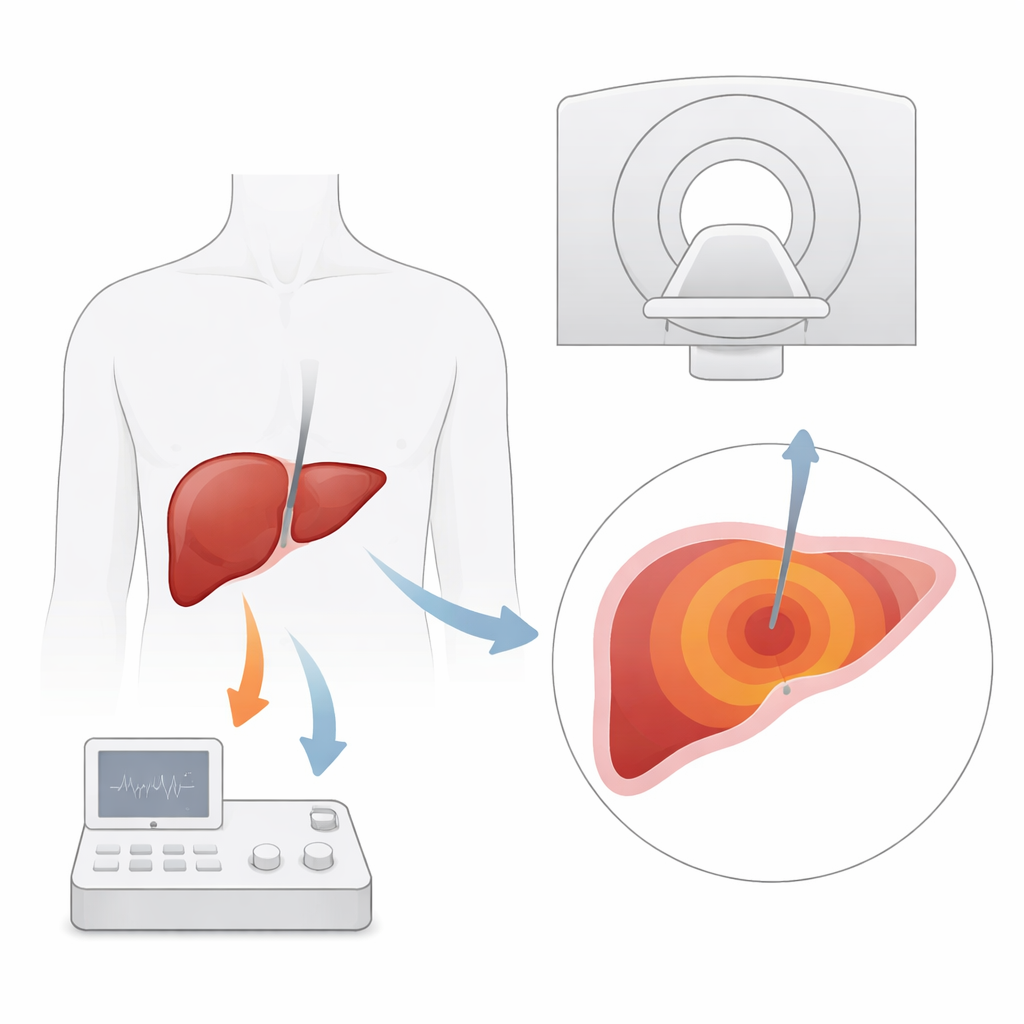
为何基于热的肝脏治疗需要更好的“视野”
微波消融通过一根细针传递能量,将肿瘤组织加热致死。对于无法接受手术的肝癌或转移瘤患者,这种方法尤为重要。传统的影像工具如超声和CT可用于引导针位,但难以清晰显示小肿瘤或在治疗过程中追踪热量扩散范围。MRI的优势在于不仅能高分辨率显示软组织,还能利用水分子的特性测量温度变化。理论上,这使医生能够实时观察肝脏的热图,并确保整个肿瘤及安全边界被充分破坏。
过高温度会让视野模糊
实际上,当组织被加热到很高温度时,MRI温度图可能变得不可靠。高温会使组织中的水沸腾,形成微小气泡,扭曲磁场。这些扭曲会在温度图上表现为错误的温度读数和异常形状,使判定真实消融区的边界变得困难。研究人员假设,通过使用稍低的目标温度可以获得更干净、更可信的MRI图,即便这可能意味着治疗区域更小。他们的目标是找到在图像清晰度与足够组织破坏之间取得最好平衡的目标温度与加热时长组合。
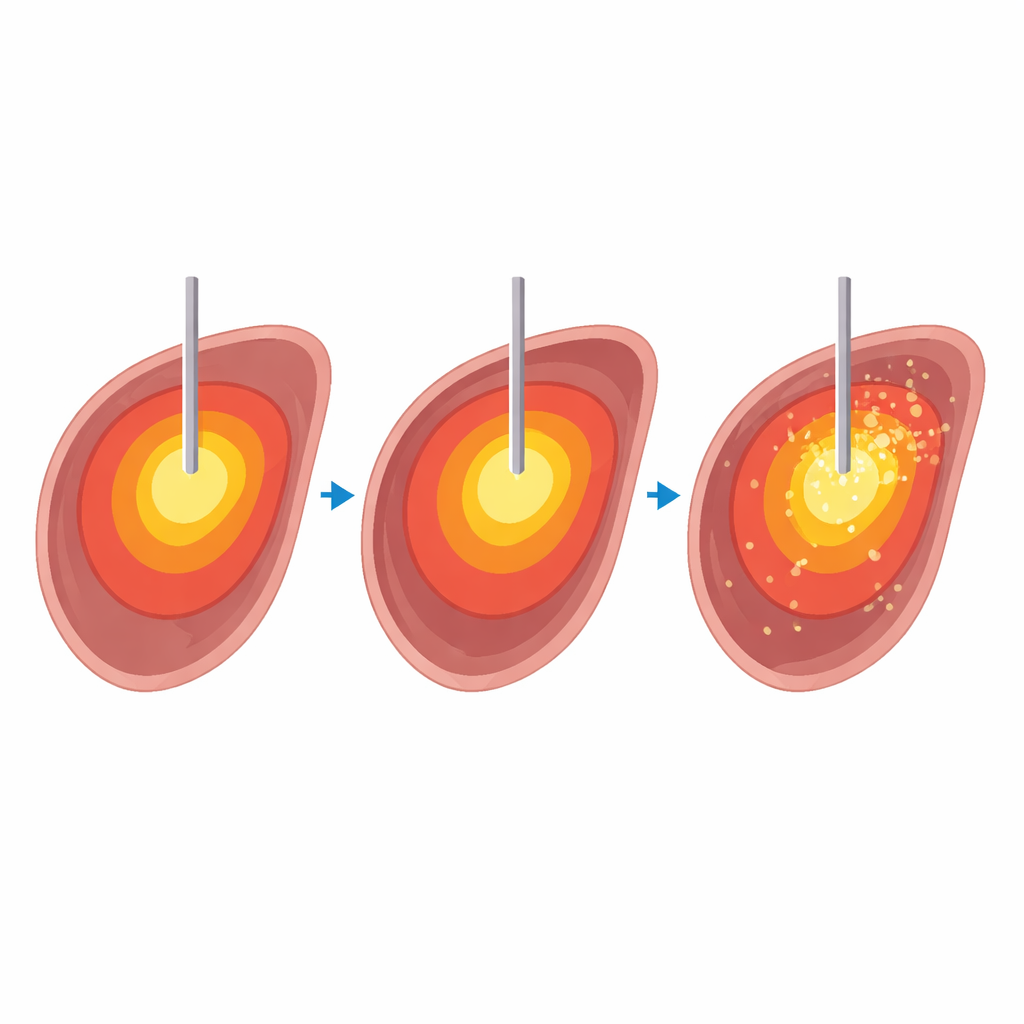
在供体动物肝脏上测试加热设置
为安全且精确地进行研究,团队在十块屠宰后不久取下的牛肝上执行了32次微波消融。在1.5特斯拉的MRI扫描仪内,他们将肝组织加热到四个目标温度——60、80、100和120摄氏度,持续四个不同时间段,范围为5到15分钟。在每次消融过程中,快速MRI序列每隔几秒生成三维温度和“热剂量”图。加热结束后,研究者沿针道切开肝脏,测量肉眼可见的坏死组织面积,并与MRI图预测的面积比较。两位放射科医生按五分制评估MRI温度图质量,考虑加热区的圆度与规则性,以及气体和针产生的伪影干扰程度。
较低温度的灼烧带来更清晰的图像
实验显示出明确的权衡关系。更高温度产生更大的坏死区,这是预期中的结果,但在100摄氏度以上时,MRI温度图明显恶化。在更高温度下,消融形状变得不规则,气体相关的畸变导致针附近出现看似下降甚至为负的温度值。相比之下,在60和80摄氏度时,MRI图更平滑、更圆,更与组织切片中真实病变大小一致。统计分析证实,在较低温度下MRI推导的面积与实际坏死面积高度一致,而在较高温度下相关性减弱或消失。延长加热时间在一定程度上能弥补较低温度导致的总损伤,但仍无法完全达到120摄氏度时观察到的最大病变面积。
一种更安全、更智能的双阶段消融策略
基于这些发现,作者提出了一个对未来MRI引导治疗具有实用意义的折衷方案。第一阶段在约80摄氏度加热15分钟可提供良好平衡:图像质量高,消融区适中,组织学检查显示有效细胞死亡。对于需要更大治疗范围的病例,他们建议采用双阶段方法:先用较低温度阶段绘制干净的热图并验证覆盖范围,然后在确认针位和边界令人满意后,在第二阶段提高温度以扩大坏死区域,接受在最后提升温度时温度图的可信度会降低这一事实。
这对未来病患护理的意义
对非专业读者而言,关键结论是“把热度调低一些”事实上可以让基于热的癌症治疗在一定程度上更安全、更精确——至少在受控的实验条件下是如此。较低的目标温度带来了更清晰的MRI温度图,使得识别真正被破坏的组织更容易。缺点是较冷的灼烧产生的病变更小,因此医生可能需要更长时间或多阶段治疗来覆盖大肿瘤。由于本研究在无血流、无呼吸运动的离体动物肝脏上进行,还需进一步在患者中验证。然而,这项研究指向一种使用MRI不仅用于定位针道,而且用于实时监视和微调加热的治疗方案,有望改善肝脏肿瘤患者的治疗效果。
引用: Nardone, L., Tan, A.S.M., Bour, P. et al. Quantitative ex vivo assessment of target temperature and ablation duration for protocol optimization of microwave ablation procedures with mr thermometry. Sci Rep 16, 8153 (2026). https://doi.org/10.1038/s41598-026-41656-3
关键词: 微波消融, 磁共振温度成像, 肝癌, 热消融, 影像引导治疗