Clear Sky Science · zh
DUSP29并不调控骨骼肌共培养模型中黑色素瘤与肌母细胞的相互作用
为什么肌肉对癌症扩散的抵抗很重要
当癌症在体内转移时,常常在肺、肝或骨等部位停留。有趣的是,我们的骨骼肌——约占体重的一半——很少成为这些危险病灶的归宿。这个谜题已困扰医生和科学家一个多世纪。本文总结的研究在这一更大难题中提出了一个聚焦问题:肌肉细胞本身及一种在肌肉中富集的蛋白DUSP29,是否直接抑制癌细胞,还是肌肉的保护作用完全源自其他因素?
游走的癌细胞罕见落脚的地方
临床上即便是在癌症广泛转移的患者中,医生也很少在骨骼肌中发现转移灶。一个设想是肌细胞为进入的肿瘤细胞创造了不友好的环境,可能通过分泌化学信号或迫使癌细胞改变行为来实现。早期在小鼠中的研究提示,当皮肤癌细胞(黑色素瘤)与未成熟肌细胞相邻生长时,它们会失去部分色素,甚至开始呈现类似肌细胞的特征。基于此,作者将注意力集中到一种特定蛋白DUSP29上——该蛋白在肌肉中的表达远高于其他组织,且属于一类已知能控制生长和存活通路的酶,这些通路常被癌症劫持。
在培养皿中测试肌肉–肿瘤遭遇
为了探究这些假设,研究者建立了一个受控的实验室模型,使用两种研究透彻的小鼠细胞系:黑色素瘤细胞(B16F10)和肌母细胞(C2C12)。他们以不同的比例将这两种细胞混合在同一培养皿中,从等量到肌母细胞远多于肿瘤细胞。在部分实验中,细胞直接接触;在另一些实验中,黑色素瘤细胞仅暴露于从肌母细胞培养物中收集的液体培养基,以捕捉肌细胞释放的可溶性因子。数日内,团队使用标准的变色检测法测量存活和分裂的细胞数,并通过流式细胞术检测程序性细胞死亡的迹象,这种技术可以区分活细胞、濒死细胞和死亡细胞。
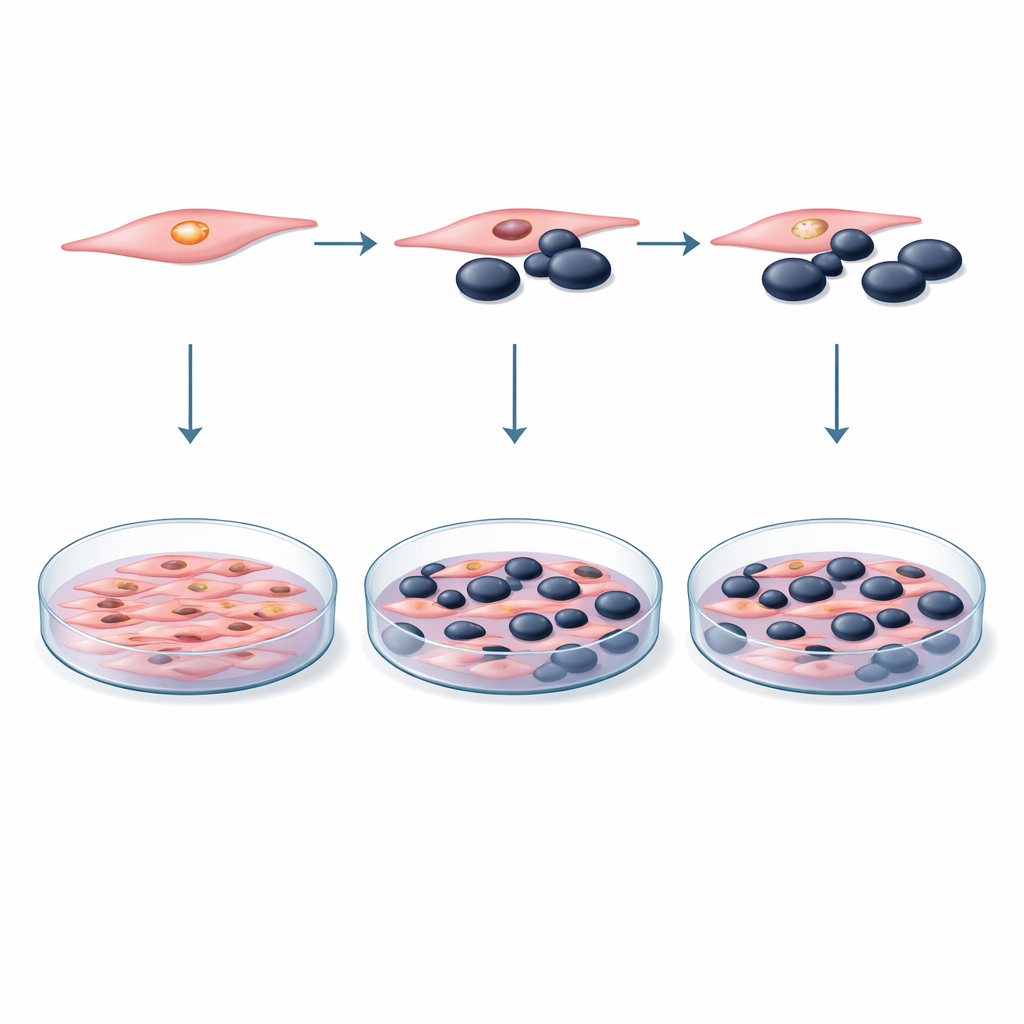
把DUSP29放到显微镜下
研究的第二部分集中在DUSP29本身。首先,科学家确认肌母细胞确实在可观程度上产生该蛋白的遗传信息。随后他们使用小干扰RNA(siRNA)——短片段基因序列,像有针对性的“关闭开关”——显著降低肌细胞中的DUSP29水平。严谨的对照实验显示,传递用的化学试剂和对照siRNA本身不会损害细胞。在DUSP29被下调后,改造过的肌母细胞再次与黑色素瘤细胞共同培养,或将其培养基用于黑色素瘤培养。研究者在多个时间点重复了相同的细胞存活和死亡测试,以观察沉默这种肌肉富集蛋白是否会把天平倾向于有利或不利于肿瘤细胞。
没有变化本身就是重要结果
在所有这些实验中,结果以其平淡无奇而令人注目。无论黑色素瘤细胞单独培养还是与肌母细胞并存、是否直接接触,其存活率在正常实验变异范围内基本不变。共培养既没有引发黑色素瘤细胞额外的细胞死亡,也没有促进其生长。在肌母细胞中敲低DUSP29同样未能改变黑色素瘤细胞的活力,尽管该基因在肌细胞中的活性被显著降低。换言之,在这些短期、简化的条件下,既没有邻近的肌母细胞,也没有DUSP29的有无,能显著引导黑色素瘤细胞走向存活或毁灭。
这对肌肉–癌症之谜意味着什么
这些发现表明,骨骼肌相对不易发生转移的保护性不太可能来自黑色素瘤细胞与邻近肌母细胞之间的简单直接对话,也不太可能仅由DUSP29在早期相互作用中独自发挥作用。相反,肌肉的抵抗力更可能源于更复杂的因素组合——其致密的结构、收缩产生的机械力、独特的代谢化学特性以及在这一培养皿系统中未能捕捉到的众多其他信号分子。通过明确指出一种可行机制的不起作用之处,这项工作帮助缩小了寻找肌肉如何阻止大多数转移性癌症的范围,并指引未来研究转向更真实的组织模型、不同的肿瘤类型以及肌肉与癌细胞相遇时的更广泛环境。
引用: Ön, S., İlhan, H.A., Günenç, D. et al. DUSP29 does not regulate melanoma–myoblast interactions in a skeletal muscle co-culture model. Sci Rep 16, 8372 (2026). https://doi.org/10.1038/s41598-026-41300-0
关键词: 骨骼肌转移, 黑色素瘤, 肿瘤–肌肉相互作用, DUSP29, 肿瘤微环境