Clear Sky Science · zh
使用弱监督下软混合专家视觉变换器的全癌种冰冻切片分类
为什么这在手术室很重要
当外科医生切除疑似肿瘤时,通常只有几分钟来确定是否已将所有癌变组织切除。病理学家需争分夺秒地检查一块快速冷冻的组织切片,并在患者仍在手术台上时给出判断。模糊的切片、隐匿的肿瘤和紧迫的时间限制都会影响这一高压流程。本文所述研究探讨了人工智能(AI)系统如何在现实医院可用的设备上,帮助病理学家快速且可靠地区分多种器官中的良性与恶性组织。
一种快速检测及其内在挑战
冰冻切片分析是现代外科的常用手段:将一小块组织冷冻、切片、染色并在显微镜下观察,以判断其为良性还是恶性,以及切缘是否清洁。与用于常规诊断的永久切片不同,冰冻切片常出现裂纹、折叠和染色不均等伪影。对边缘病例不同病理学家可能意见不一,且时间始终紧迫。这些问题在较小或繁忙的医院尤为严重,在那里少数专家需覆盖多种癌症类型。作者认为,稳健的计算机辅助系统可使冰冻切片决策更一致、更快速并更广泛可用。
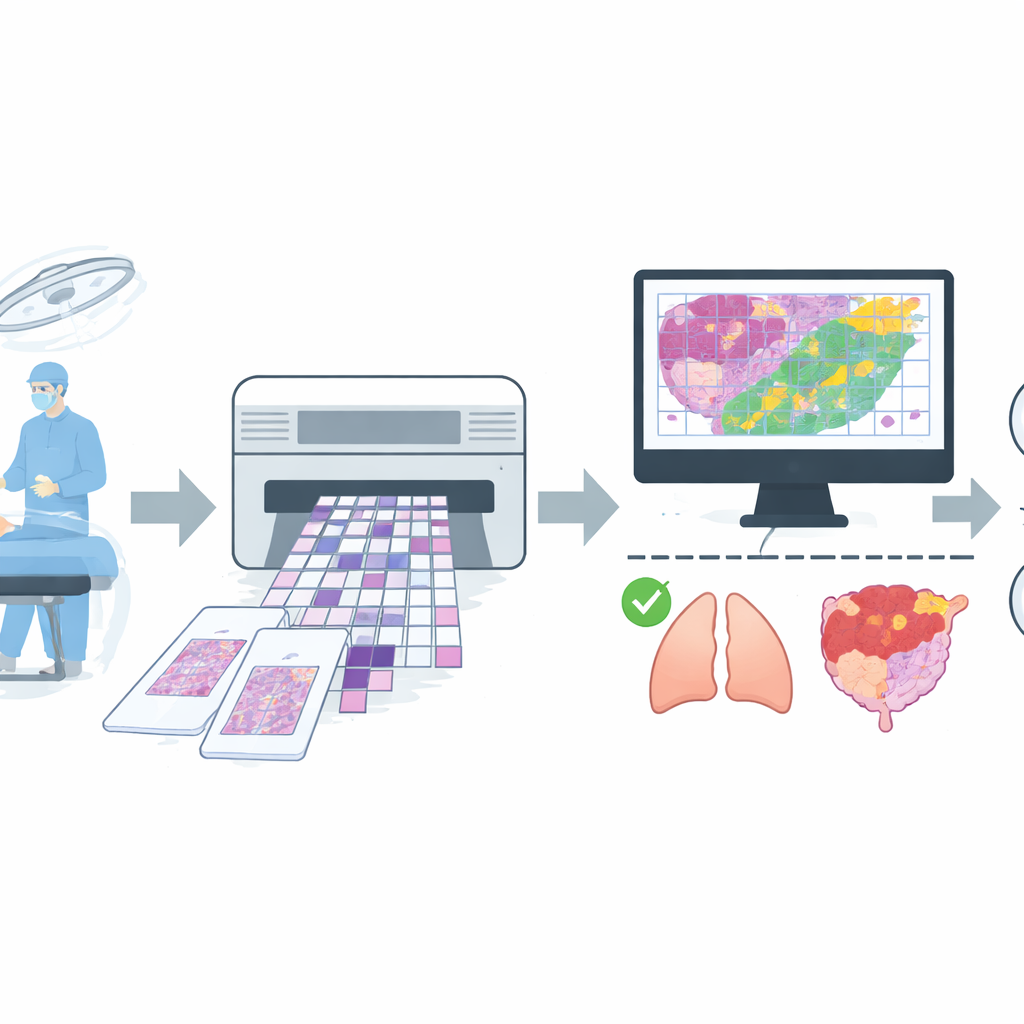
构建广泛且贴近真实场景的图像集
为训练这样的辅助系统,团队汇集了来自一家大型医院常规手术的海量数字图像。他们收集了来自超过2600名患者的4754张整片冰冻组织切片图像,并应用严格的质量规则剔除存在严重伪影或诊断不确定的切片。最终数据集包含4667张切片,每张均基于快速冰冻读片与随后更为仔细的永久切片报告的一致意见被简单标注为良性或恶性。切片覆盖常见部位如肺、乳腺、甲状腺、淋巴结和女性生殖器官,以及胃、肝、皮肤等较少见部位的混合组。数据被划分为训练、微调和最终测试的独立组,并严格确保同一患者的图像不会出现在多个组中。
AI如何从弱线索中学习
研究人员基于一种称为视觉变换器(Vision Transformer)的神经网络构建模型,该类网络擅长在大幅图像中发现模式。每张巨大的组织图像被自动切割成许多较小的图块和补丁,以便在标准图形硬件上处理。一个关键创新是用“软混合专家”替代网络的一部分——这是一组许多小型专门分支,每个分支关注不同的视觉模式。系统不是对专家进行硬开关,而是平滑地混合它们的贡献,这样可稳定训练并更好地利用有限数据。由于病理学家未对肿瘤勾画精确轮廓,模型只能在弱监督下学习:它只知道整张切片是良性还是恶性。多实例学习策略将恶性切片中最可疑的补丁提升为正样本,使网络能够逐步聚焦于最具信息量的区域。
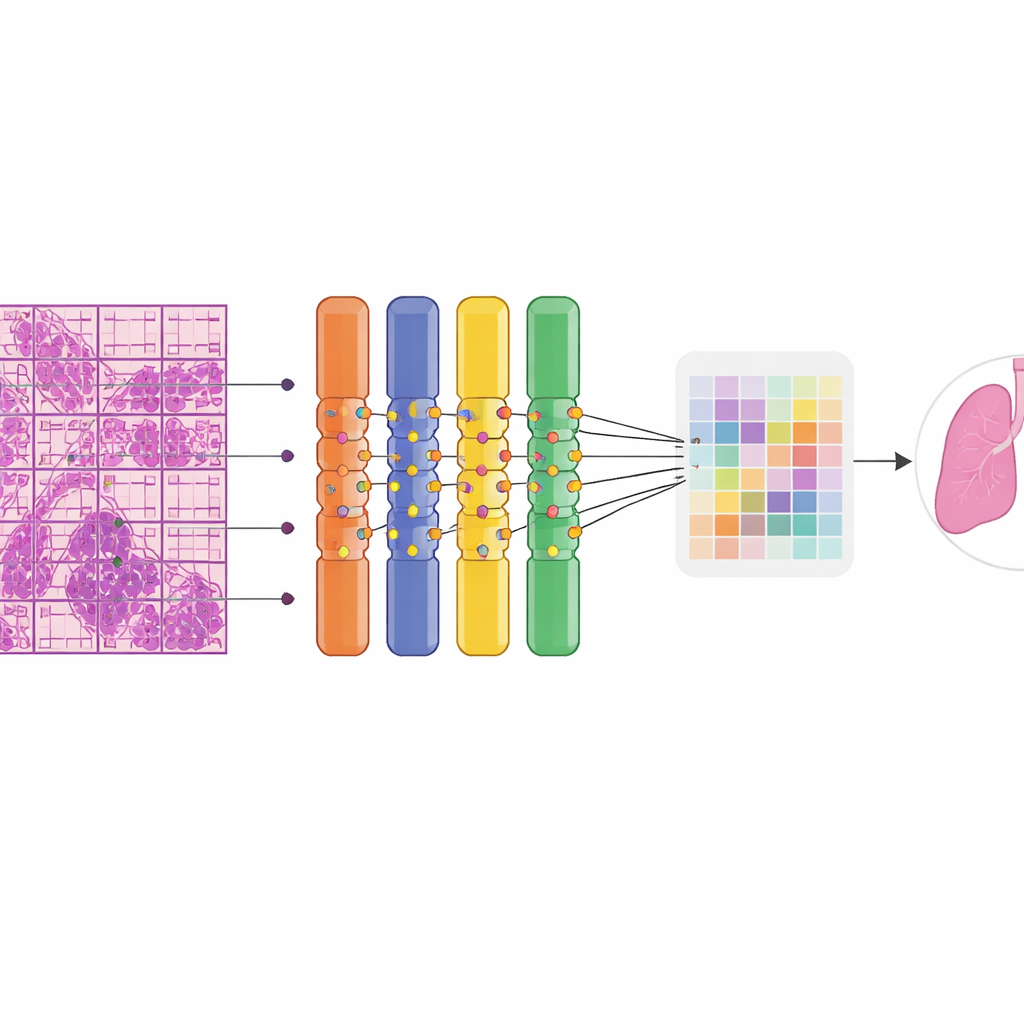
系统在实践中的表现如何
在对669张未见过的切片进行测试时,AI在良性与恶性组织的区分上表现出高准确性。总体上约正确分类了90%的病例,并在概率阈值范围内显示出出色的区分能力。敏感性(将真实恶性切片标记为可疑的概率)约为五成到八成之间,而特异性(将良性切片正确判断为良性的概率)更高。重要的是,跨器官的表现保持稳健:在测试集中,它完美检测出了所有肺和乳腺的恶性病例,并且在女性附件肿瘤和其他混合器官等较少见组上也有良好表现。覆盖在切片上的颜色热图显示,模型的注意力集中在专家病理学家识别为肿瘤的区域,包括淋巴结内的转移灶,同时在很大程度上忽略正常结构。该系统运行高效,内存占用低于5 GB,适合在常见显卡上运行,而非依赖昂贵的计算集群。
局限、失误与改进空间
作者还分析了AI出错的情况。假阴性常见于极为稀疏的癌细胞、扫描区域模糊或被大量炎性反应掩盖的恶性灶。假阳性则常出现在在显微镜下类癌症表现的良性情况,如反应性增生或被扭曲的冰冻组织。由于常规外科流程中不包含对肿瘤区域的详细标注,团队无法精确量化热图与专家标注的一致性,只能依赖定性评审。某些器官类型,如舌头或某些软组织肿瘤,样本仍然不足,提示需要更大规模、多中心的数据集来扩展系统的适用范围。
这对患者和医院意味着什么
总体而言,该研究表明,经过精心设计的AI系统能够准确且可解释地辅助外科病理学的一项核心任务:实时决定多种器官的组织是良性还是恶性。通过仅使用切片级标签、在广泛可用的硬件上运行,并为人工复核突出显示可疑区域,该模型为实现更一致的冰冻切片决策提供了实用路径。对患者而言,这可能意味着在一次手术中获得更充分的信息以指导治疗;对医院,尤其是专家人手有限的机构而言,这指向了一个更公平地提供高质量癌症护理的未来,其中先进的数字工具发挥重要作用。
引用: Wu, J., Yang, M., Li, J. et al. Pan-cancer frozen section classification using a soft mixture of experts vision transformer under weak supervision. Sci Rep 16, 10297 (2026). https://doi.org/10.1038/s41598-026-40924-6
关键词: 冰冻切片, 数字病理学, 癌症诊断, 视觉变换器, 弱监督学习