Clear Sky Science · zh
用于胃肠病变监测与精确靶向药物递送的可解释人工智能
更智能的扫描、更安全的治疗
许多人因癌症药物的严重副作用而望而却步。这项研究设想了一个未来:小型可吞咽摄像头、智能算法与微观药物载体协同工作,使强效药物只在真正需要的部位释放。通过将肠道病灶的即时可视化与现场治疗闭环连接,作者们旨在使胃肠医疗更精确、创伤更小且更安全。
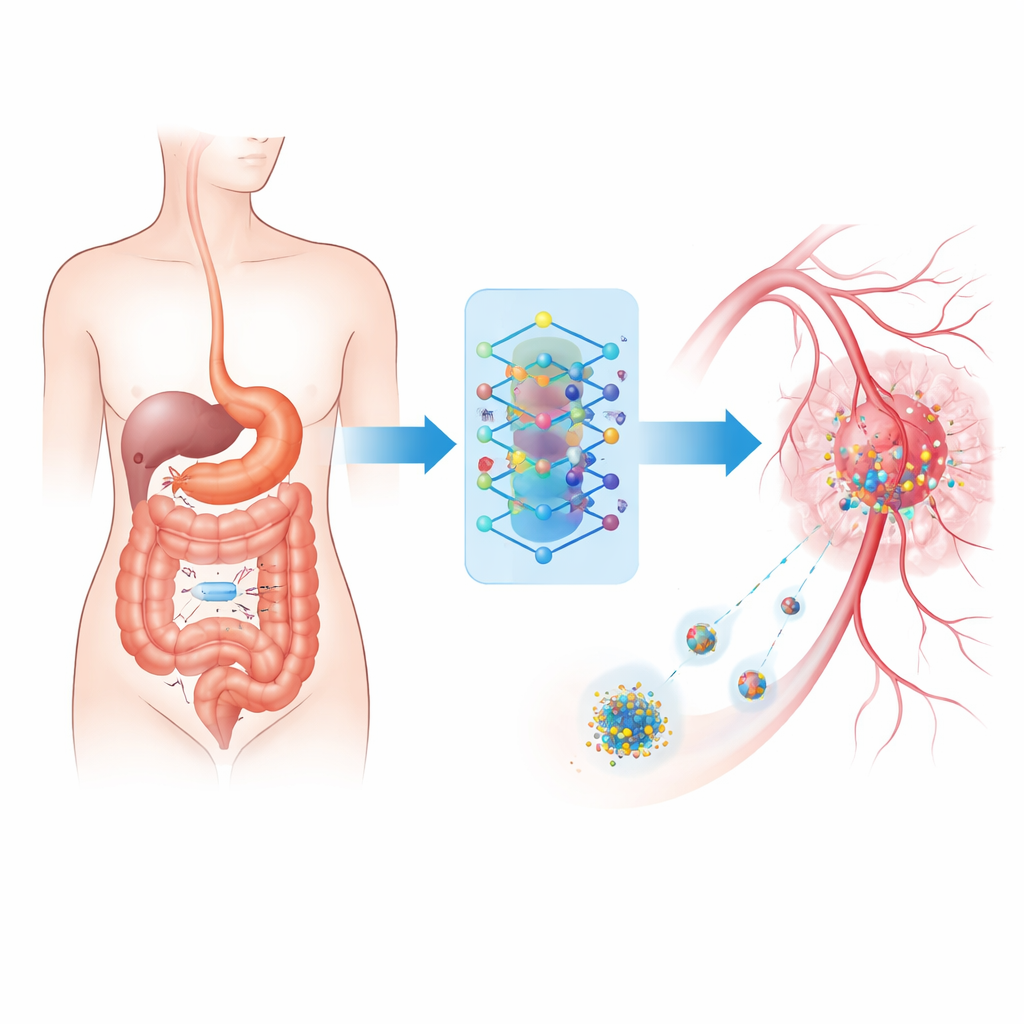
小小摄像头的旅程
系统的核心是一种无线可摄取成像装置——维生素大小的胶囊在消化道内自然移动,同时拍摄数万张图像。与其完全依赖医生来逐一审阅这些海量图像,胶囊将图像发送到体外的可穿戴单元。在那里,一台紧凑型计算机使用先进的模式识别软件,将正常组织与可能癌变或严重发炎的可疑病变区分开来。该方案类似于医院现有的胶囊内镜,但进行了升级,以实现实时工作并直接连接治疗工具。
作为决策者的人工智能
可穿戴单元运行一个经过精心训练的图像分析模型,基于现代计算机视觉技术。该模型通过大量公开的内镜和组织图像学习识别25种不同的胃肠病变——从息肉和溃疡到严重炎症。为应对某些疾病远比其他疾病罕见的事实,作者采用了两阶段训练:先学习每种病况的一般视觉特征,然后微调模型以确保危险但罕见的发现不会被忽视。在测试中,这种方法对图像的分类准确率超过九成,对与癌症相关的类别表现尤为出色。
“黑盒”内的可视化
由于可能影响给药剂量的自动诊断必须得到医疗人员的信任,作者采用了可解释人工智能技术来展示哪些图像区域驱动了模型的决策。热图式覆盖层突出显示系统认为重要的确切区域。对这些解释图不仅进行了目视检查,还用定量测试进行评分,这些测试衡量在去除或增加被高亮的区域时模型置信度的变化、解释在重复训练中的稳定性以及与专家绘制病变轮廓的重叠程度。在多个方法中,一种名为 LayerCAM 的方法产生了最忠实且一致的解释,帮助医生验证系统确实在“看”正确的部位。
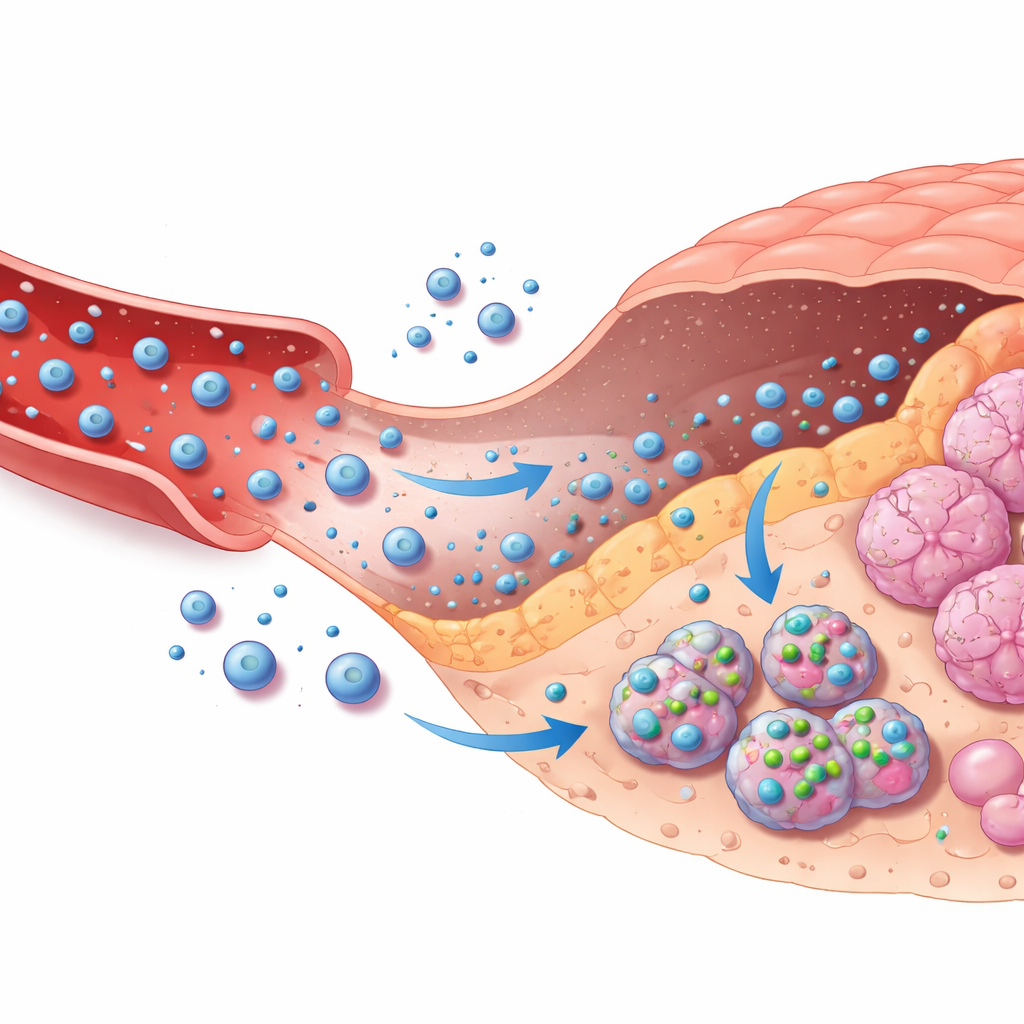
引导体内药物载体
框架的第二部分将基于图像的决策与靶向化疗递送连接起来。作者对一种常用抗癌药物多柔比星(doxorubicin)从外部泵经血液循环、渗入肿瘤组织、进入肿瘤细胞并最终被清除的过程进行了建模。该过程用一个多区室数学模型来描述,跟踪血液、周围组织和细胞内的药物浓度。根据 AI 判定病变恶性的置信度及其严重程度,一个简单的规则系统在无治疗、温和治疗或强力治疗之间选择,并调整药物载纳米粒子释放货物的速度及输注时长。一个安全层持续监测细胞内的预测药物水平,并在接近安全上限时自动降低剂量,即使 AI 过于自信也会如此。
保护隐私与防止滥用
由于同一链路既传输图像也可传输治疗命令,安全性至关重要。作者提出了一种轻量级隐私方案,使用混沌数学映射对生物医学信号进行扰码处理,然后通过体内纳米网络传输,从而使被截获的数据难以解读。其上层为可穿戴网关,负责设备认证并验证控制信号是否匹配预期的物理模式,帮助阻止伪造命令。仿真显示,不同隐私设置如何以小幅检测准确率损失换取更强保护,并识别出在保持临床性能高的同时显著限制数据泄露的工作点。结合严格的剂量上限、紧急断开规则和安全日志,这些措施旨在使系统对意外和攻击都具有韧性。
这对患者意味着什么
简而言之,这项工作描绘了一个体内“即见即治”闭环可能的工作方式:可吞咽的摄像头发现可疑部位,智能助手以透明的推理解释所见,受控的药物递送系统对病变组织给予受限且聚焦的剂量。该研究仍属理论并基于仿真,但表明这种闭环设计在 AI 出错或个体条件差异存在时,仍能兼顾疗效靶向性与严格的安全限制。如能在实践中实现,此类系统或能将粗放的化疗转变为更为精确和个性化的胃肠疾病治疗工具。
引用: Kamal, I.R., El-Zoghdy, S.F. & Soliman, R.F. Explainable AI for gastrointestinal lesion surveillance and precision targeted drug delivery. Sci Rep 16, 9807 (2026). https://doi.org/10.1038/s41598-026-40882-z
关键词: 胃肠成像, 可解释人工智能, 靶向药物递送, 纳米医药, 胶囊内镜