Clear Sky Science · zh
用以吖嗪-a 功能化的植物来源金纳米颗粒用于对 A549 肺癌细胞的强效光动力疗法
更环保的光学手段攻击肺癌
肺癌是全球最致命的癌症之一,许多现有治疗在杀伤肿瘤的同时也会损伤健康组织。本研究探索了一种更温和、更具选择性的策略,将植物来源的金颗粒与光敏染料结合,在体外选择性地破坏肺癌细胞。目标是利用“绿色”纳米技术和激光光照,使癌细胞受到强烈打击,而周围健康细胞在很大程度上得以保留。
将药用植物变成微小的金色帮手
研究人员以 Dicoma anomala 为起点,这是一种传统用于治疗多种疾病的非洲药用植物。他们没有使用刺激性化学试剂,而是用植物叶提取物将溶解的金盐还原成微小的金纳米颗粒。植物化合物既起到还原剂的作用,又为颗粒提供包覆,使其稳定,形成直径约 90–100 纳米、带负表面电荷的球形颗粒,有助于防止团聚。这种环保过程制备出均一且长期稳定的颗粒,适合医学用途。
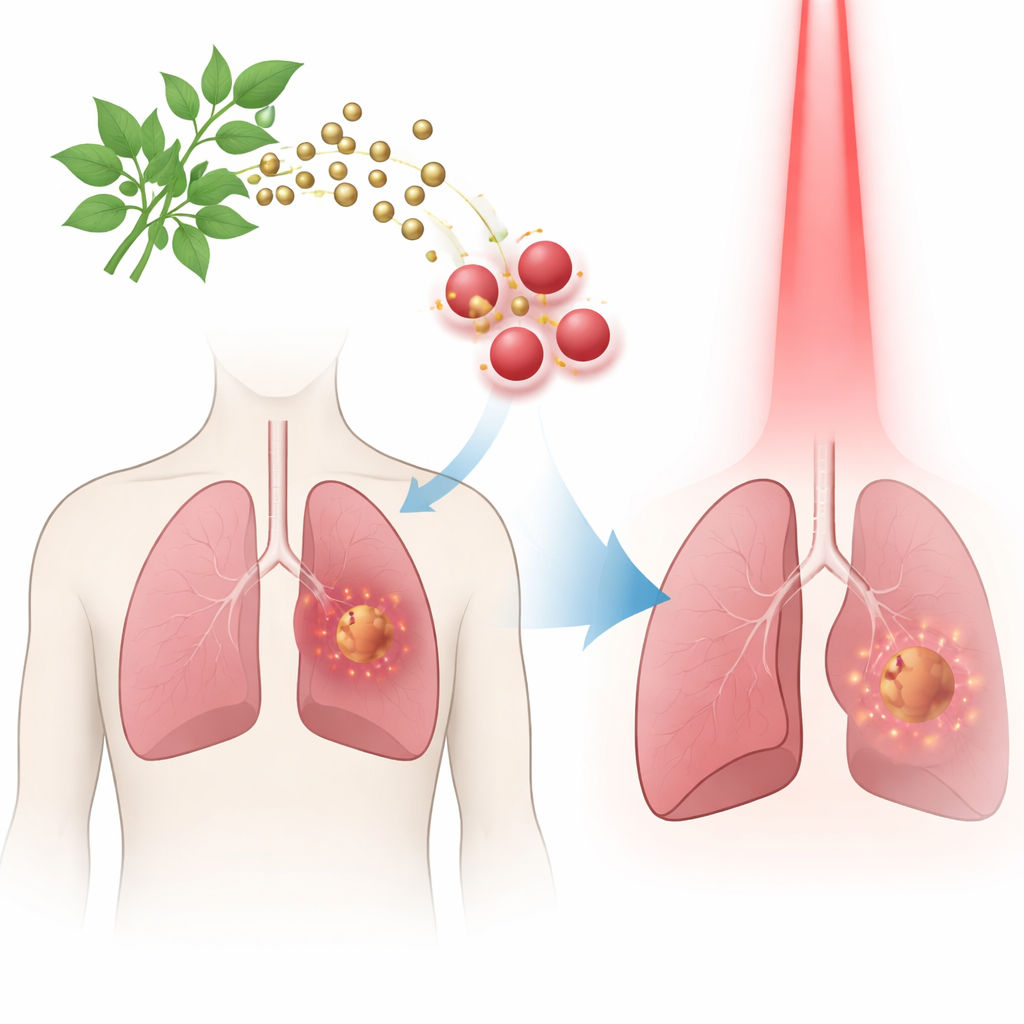
载入光激活药物
随后,团队将一种名为 pheophorbide‑a 的光敏剂(这是一种仅在红光照射时产生毒性的染料)连接到金纳米颗粒表面。通过薄膜水合法,他们构建了一个纳米缀合体,约 40% 的加入药物稳定地与颗粒结合。详尽的测量结果证实金芯和染料都存在并发生化学结合,而不是简单混合。所得复合体能在水中保持分散,这是注入血液时非常重要的特性。
测试光对癌细胞的杀伤力
为了评估这种混合材料的抗癌能力,科学家们将人类 A549 肺癌细胞在培养皿中暴露于不同剂量的纳米缀合体。部分细胞保存在暗处,另一部分用红色激光照射,激光波长选择可强烈激活 pheophorbide‑a 并比较短波长更易穿透组织。在暗处,处理过的细胞在形态和行为上与未处理细胞相似:形态正常、代谢水平维持较高且少有细胞死亡。然而,一旦开启激光,细胞代谢迅速下降,肺癌细胞开始按剂量依赖性发生萎缩、脱落并破裂。
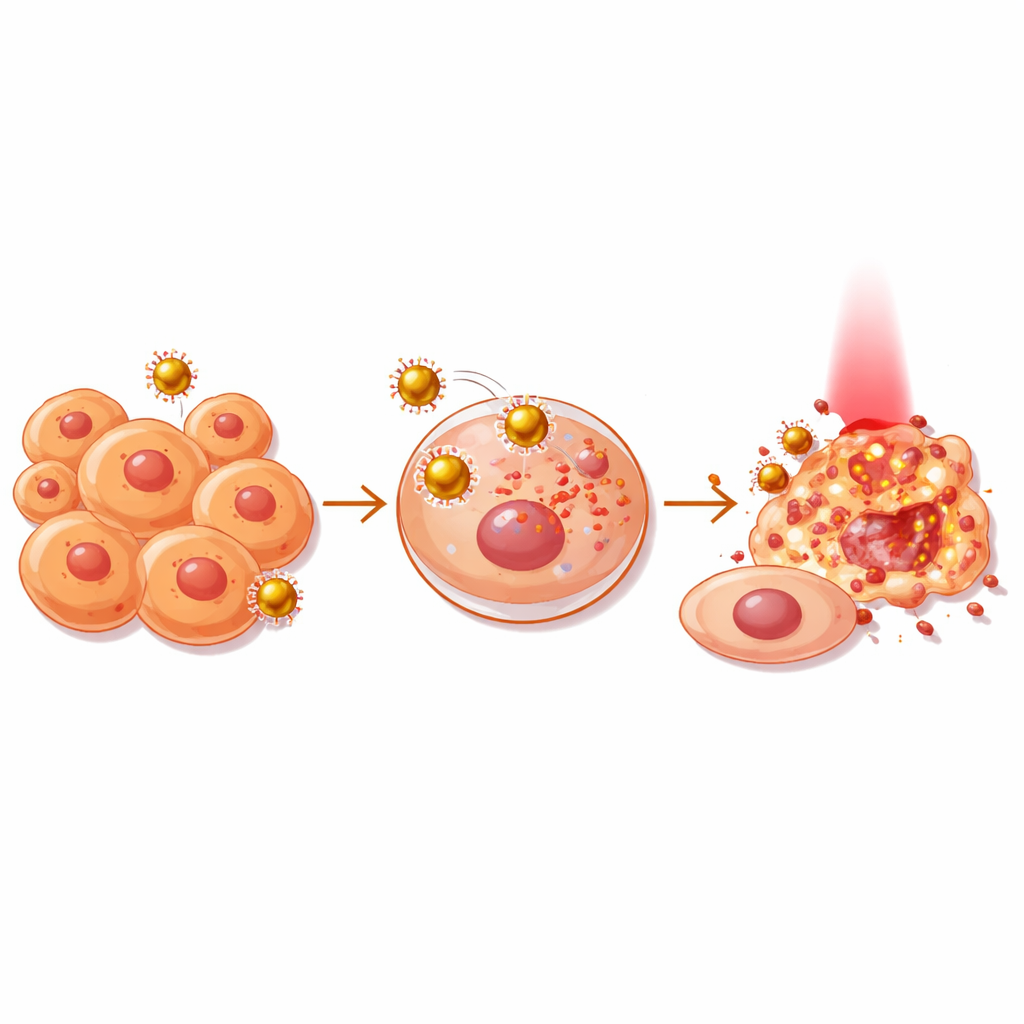
这些颗粒如何触发细胞自杀
选择性的关键在于活性氧(reactive oxygen species, ROS)——当载药金颗粒吸收红光时产生的短寿命、反应性强的含氧分子。团队仅在受光照样本中测得这些分子显著上升,表明治疗在未照光时基本处于惰性状态。染色检测和基于荧光的流式细胞术表明,许多经处理的癌细胞进入了凋亡——一种程序化的细胞自杀,通常比混乱的细胞坏死更可控。同时,经受相同处理的正常皮肤来源细胞表现出更高的抵抗性,呈现出有利的选择指数,表明存在一个治疗窗口,在该窗口内癌细胞比健康细胞受更大影响。
这对未来肺癌治疗意味着什么
这项体外研究表明,将植物来源的金纳米颗粒与光激活染料结合,可能产生一种智能疗法:在暗处稳定且基本无害,而在照光时对肺癌细胞具有强毒性。尽管该研究在二维细胞培养中进行,尚未进入动物或临床试验,但它为一种可能比许多常规方案更精确、损伤更小的治疗奠定了重要基础。通过在三维肿瘤模型和整体生物体中的进一步测试,这一绿色纳米技术平台有朝一日或可支持仅在需要部位照光的肺癌疗法,而让身体其他部分保持“黑暗”。
引用: Zahra, M., Abrahamse, H. & George, B.P. Plant-derived gold nanoparticles functionalized with pheophorbide-a for potent photodynamic therapy against A549 lung cancer cells. Sci Rep 16, 9819 (2026). https://doi.org/10.1038/s41598-026-40697-y
关键词: 肺癌, 光动力疗法, 金纳米颗粒, 绿色纳米技术, 纳米医学