Clear Sky Science · zh
与胰腺炎相关的胰凝乳蛋白酶 C (CTRC) 变体 p.R240Q 通过破坏远程静电相互作用选择性损害胰蛋白酶原降解
这对胰腺健康为何重要
慢性胰腺炎是一种疼痛且长期的胰腺炎症,可导致糖尿病、消化问题以及生活质量显著下降。本研究探讨了为何某些人因其消化酶中的微小遗传变化而更易受累。通过聚焦于一种保护性酶的单一基因变体,研究人员展示了如何一个细微的分子变化就能将胰腺内的平衡从保护转向自我伤害。
消化系统内置的安全机制
我们的胰腺产生强效的蛋白质分解酶,这些酶通常以非活性形式释放到肠道。其中一种前体胰蛋白酶原有时会过早在胰腺内部被激活。一旦发生,它就可能从内部开始消化胰腺并触发炎症。为防止这种情况,机体使用若干防护措施,包括抑制蛋白(SPINK1)和另一种消化酶胰凝乳蛋白酶 C(CTRC)。CTRC 有双重作用:它有助于在需要的时间和地点激活消化酶,但也会切割多余的胰蛋白酶原,防止其转变为活性胰蛋白酶并造成伤害。遗传到功能减弱的 CTRC 的人群已知具有更高的慢性胰腺炎风险。
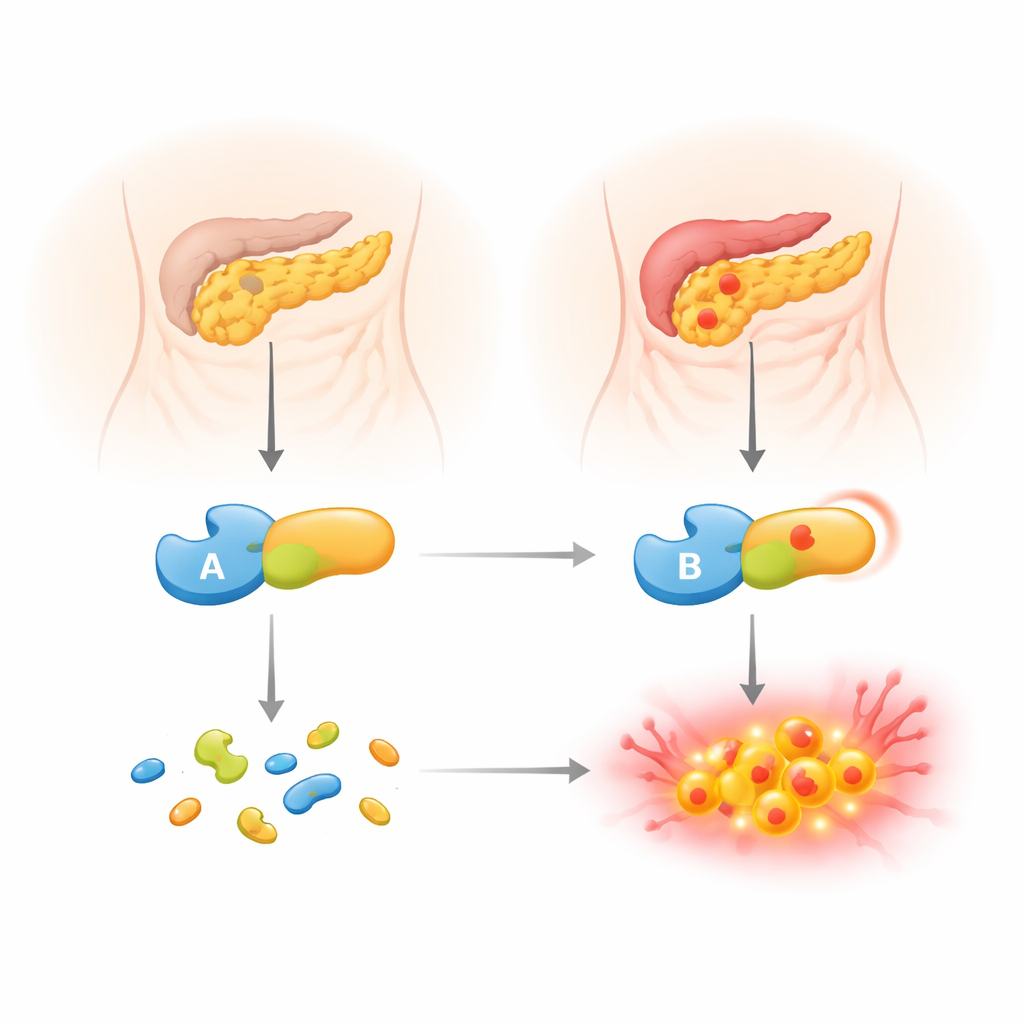
显微镜下的罕见基因变化
研究团队集中研究一种罕见的 CTRC 变体 p.R240Q,该变体在一名斯洛伐克的儿童发病型慢性胰腺炎患者和其发病的父亲中被发现。该变体在酶表面改变了单个构建基块,将带正电的残基替换为中性残基。大型基因数据库通常将其归类为可能无害,但它在若干年轻病患中出现。为查明其真实作用,作者将来自该家族的遗传信息与详细的实验室研究相结合。他们将变体酶和正常 CTRC 并列比较,观察细胞对其的产生与分泌情况、在标准测试底物上的活性,以及它与要控制的关键物质——胰蛋白酶原之间的相互作用。
活性正常,但靶向失准
首先,研究人员表明,细胞对 p.R240Q 酶的产生和分泌与正常版本相当,因此该变体并不导致折叠错误或合成失败。在使用小合成肽和乳蛋白(β-酪蛋白)的体外测定中,变体的表现与正常 CTRC 相当甚至略优。这表明其切割能力完好。但令人为之一惊的是,在与胰腺炎最相关的反应——分解人阳离子胰蛋白酶原方面,变体酶明显低效——降解胰蛋白酶原的速度大约慢四到五倍,且在防止胰蛋白酶原自发激活为胰蛋白酶方面表现远差。在自发激活实验中,为了抑制胰蛋白酶水平,需用到远多于正常酶量的变体 CTRC。
被破坏的静电“牵引束”
为了解这一现象的原因,作者借助 CTRC 的结构模型。在 CTRC 抓握底物的槽周围,存在由若干带电氨基酸形成的一圈正电荷,其中就包括 p.R240Q 变动的位点。CTRC 需要切割的胰蛋白酶原区域带有很强的负电荷,因此这圈正电荷像一个远程的“牵引束”,将胰蛋白酶原引导到正确位置。将其中一个正电位中和后,p.R240Q 变体削弱了这种远距离的吸引力。酶的切割利性仍在,但受损的引导系统使胰蛋白酶原的结合效率下降,从而减少被安全降解的量。那些不依赖该电荷模式的其他底物仍能被正常处理,这解释了实验中观察到的高度选择性缺陷。
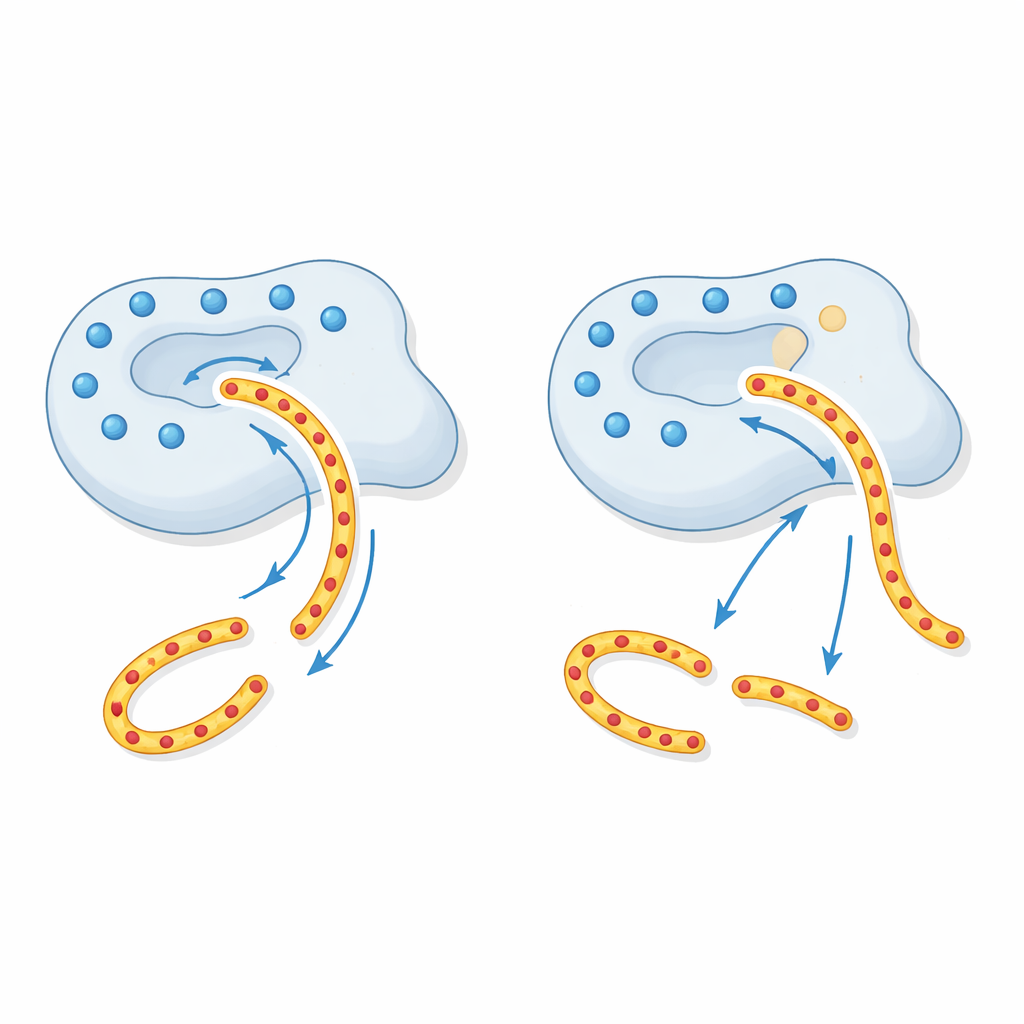
对患者与检测的意义
临床上,患病的男孩和他的父亲还携带第二个有害的 CTRC 变体,且父亲存在诸如大量饮酒等额外生活方式风险因素。这与慢性胰腺炎常由多种遗传和环境因素叠加导致的观念相符。这项工作表明,常见预测工具判定为无害的变体依然可能以非常特定的方式具有危险性。对于基因检测,结论明确:在评估 CTRC 变体是否增加胰腺炎风险时,科学家必须在真实靶标——胰蛋白酶原——上进行测试,而不仅仅依赖通用的实验底物。通俗地说,这项研究揭示了酶“引导表面”的微小改变如何悄然破坏胰腺的关键安全锁之一,使易感个体更易陷入慢性炎症。
引用: Nagy, Z.A., Sándor, M., Hegyi, E. et al. Pancreatitis-associated chymotrypsin C (CTRC) variant p.R240Q selectively impairs trypsinogen degradation through disruption of long-range electrostatic interactions. Sci Rep 16, 8937 (2026). https://doi.org/10.1038/s41598-026-40633-0
关键词: 慢性胰腺炎, 胰凝乳蛋白酶 C, 胰蛋白酶原, 基因变体, 消化酶