Clear Sky Science · zh
细胞黏附分子1在结缔组织肥大细胞中上调,并可能参与IgE介导的脱颗粒反应
为何抑制过敏细胞很重要
凡是经历过突发瘙痒、荨麻疹或肿胀的人,都曾感受过肥大细胞的威力——这些免疫细胞静置于皮肤中,直到遇到过敏原被激活。当这些细胞反应过度时,会引发荨麻疹和特应性皮炎等疾病。该研究考察了肥大细胞表面一种鲜为人知的蛋白——CADM1,结果显示用特异性抗体降低其水平,能在小鼠中温和但可测量地减弱过敏性皮肤反应。该工作提示了一种在不完全抑制免疫系统的前提下微调过敏反应的新思路。
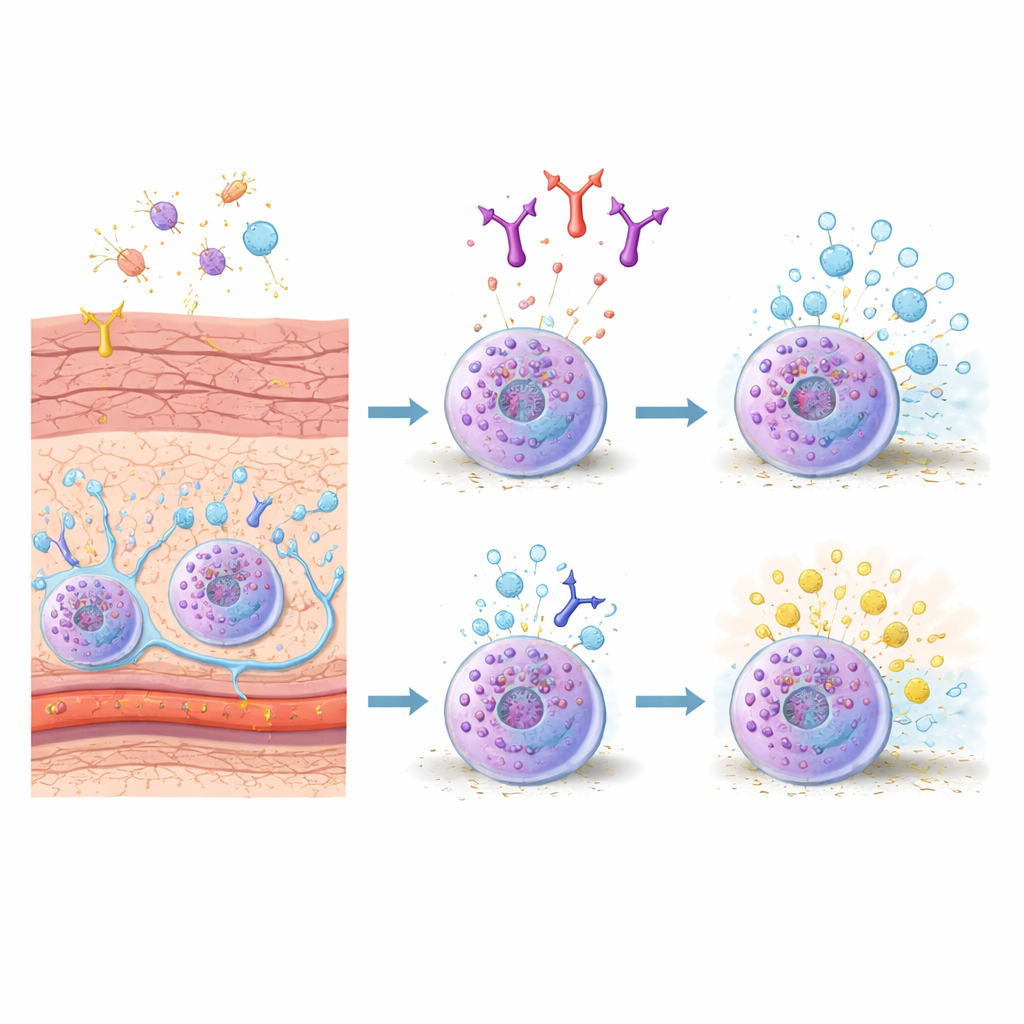
认识皮肤的报警细胞
肥大细胞驻守在面向外界的组织中,如皮肤和肠道,充当报警触发器。在小鼠中,一类主要的亚型——结缔组织肥大细胞,位于皮肤及更深的组织,对与过敏相关的刺激反应强烈。当其表面受体结合识别过敏原的IgE抗体时,这些细胞会迅速释放装满组胺、酶和信号分子的颗粒——这些物质使血管通透、组织肿胀并激活神经。由于肥大细胞在突发过敏和持续性炎症中都起关键作用,研究者一直在探索更精确地抑制其活性的办法。
一种粘附性表面蛋白成为焦点
作者把注意力放在一种名为CADM1的分子上,该分子以帮助细胞与邻近细胞(包括神经和皮肤支持细胞)黏附的“胶水”作用著称。早期研究表明,肥大细胞表面的CADM1可增强其与神经纤维的接触,并可能加剧特应性皮炎模型中的慢性瘙痒。但此前尚不清楚CADM1是否也会影响肥大细胞在皮肤中对快速IgE驱动的过敏反应的细胞内应答。为探究这一点,研究团队在体外通过将骨髓来源的肥大细胞与成纤维细胞共同培养、模拟皮肤微环境,从而诱导出类结缔组织的肥大细胞。他们发现,这类结缔组织样肥大细胞相比骨髓来源的细胞显著上调了CADM1,提示CADM1可能是皮肤型肥大细胞的一个标志。
一种能调低细胞爆发的抗体
研究者随后使用了一种经工程改造的抗体,称为3E1,能结合CADM1的外部区域。在培养的结缔组织样肥大细胞中,短时暴露于3E1可明显降低细胞表面的CADM1,而不影响其他关键分子。当这些细胞用IgE致敏然后暴露于模型过敏原时,对照组细胞大量释放了一种颗粒酶,这是脱颗粒的读出指标。预处理3E1的细胞释放的酶显著减少——大约减少五分之一。值得注意的是,同一抗体并未削弱骨髓来源肥大细胞的反应,也不影响由神经相关信号(P物质)引发的激活,表明其对皮肤型肥大细胞中IgE通路具有选择性作用。
细胞内部:重塑骨架与颗粒运输
为了解CADM1如何影响这类快速反应,团队通过荧光显微镜观察细胞内的关键事件。在对照的结缔组织样肥大细胞中,暴露于过敏原后迅速诱导分泌颗粒的形成与移动,并伴随细胞膜下方肌动蛋白“骨架”的剧烈重排——这些变化有助于颗粒向表面移动并融合。接受3E1处理后,早期的颗粒信号明显减弱,肌动蛋白的常见重塑也被强烈抑制。换言之,降低CADM1并未阻止过敏原与其受体结合,但确实阻碍了细胞重新组织其内部支架和运输系统,从而妨碍了全面释放。
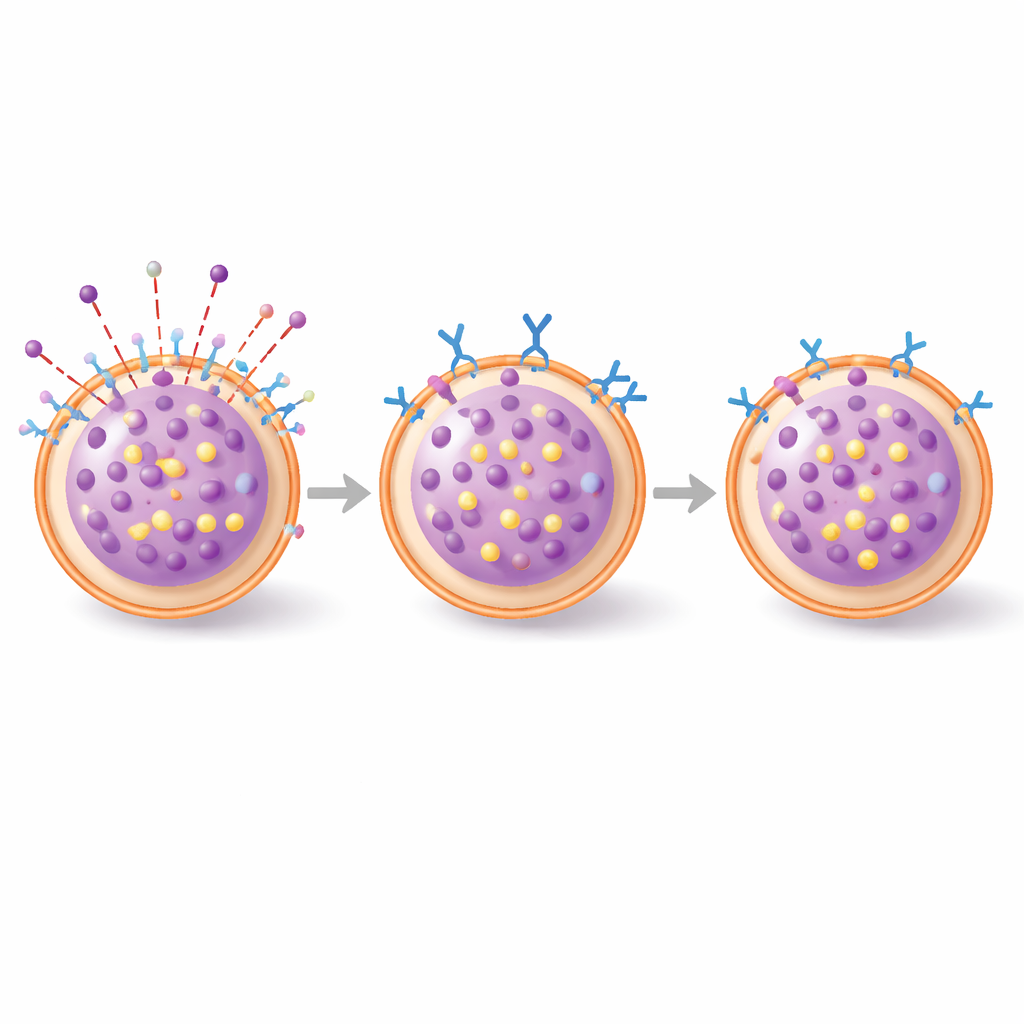
从培养皿到活体皮肤
研究者接着转入一种称为被动皮肤性过敏反应的小鼠模型:在该模型中,用IgE致敏的动物在耳部接受少量化学过敏原。静脉注射3E1抗体后再进行挑战的老鼠仍出现肿胀,但显微分析显示,其皮肤中处于释放颗粒过程的肥大细胞比例低于对照动物。作为肥大细胞活化的组织标记,胰蛋白酶也呈下降趋势。抑制效应虽温和,尤其在非常早的时间点上不明显,但反应开始几小时后变得更清晰,说明该抗体更像是对进行中脱颗粒的部分制动,而非完全阻断最初的触发步骤。
对未来过敏治疗的意义
总体而言,这项研究表明CADM1不仅仅是细胞间的黏合带:在皮肤型肥大细胞中,它还支持驱动IgE介导的过敏爆发所需的内部重塑和颗粒移动。通过用3E1抗体结合CADM1并使其从细胞表面去除,研究者能够在体外减弱脱颗粒并在小鼠的过敏性皮肤反应中降低肥大细胞的活化。尽管效应适中且研究限于动物模型,但这些发现提出了靶向CADM1的治疗策略可能有助于选择性地缓和皮肤中有害的肥大细胞反应——有望减轻急性过敏皮疹,或在进一步研究下用于慢性疾病如特应性皮炎——而无需对免疫系统进行广泛抑制。
引用: Hagiyama, M., Yoneshige, A., Takeuchi, F. et al. Cell adhesion molecule 1 is upregulated in connective tissue mast cells and potentially contributes in IgE-mediated degranulation. Sci Rep 16, 9432 (2026). https://doi.org/10.1038/s41598-026-40526-2
关键词: 肥大细胞, 过敏性皮肤反应, IgE脱颗粒, 细胞黏附分子1, 靶向抗体治疗