Clear Sky Science · zh
利用计算机辅助药物设计技术发现羟基三唑作为潜在的糖氧化酶‑I抑制剂
为什么阻断一个微小的细胞清道夫可以抗癌
癌细胞常常生长过快,以至于被自身代谢废物淹没。它们的生存伎俩之一是内置的清理系统,用以解毒糖代谢产生的有害副产物。本研究探讨如何关闭该清理队伍中的一个关键成员——一种称为糖氧化酶‑I的酶,研究团队借助计算机从数万种分子中筛选,并在实验中检验最有前景的候选物。目标是发现新的药物“起点”,未来可能帮助医生从内部选择性地毒杀癌细胞。
我们细胞内的隐藏废物系统
每个细胞不断分解糖以产生能量,这一过程会产生一种反应性废物化学物质——甲基乙二醛。在正常水平下,机体通过糖氧化酶系统将甲基乙二醛转化为无害的乳酸,这是一条依赖辅因子谷胱甘肽的两步通路。糖氧化酶‑I是这一链中第一且最关键的一步。以极高速燃烧糖的癌细胞严重依赖糖氧化酶‑I来防止甲基乙二醛达到毒性水平。如果该酶被阻断,甲基乙二醛会累积并将受损细胞推向程序性死亡。这使糖氧化酶‑I成为攻击肿瘤代谢基本弱点的有吸引力的抗癌药物靶点。
用硅与统计搜寻化学空间
研究者没有在实验室中逐一测试随机物质,而是使用计算机辅助药物设计来搜索一个超过5万种小分子的商业库。专用软件首先清理和标准化每个分子,然后预测其在接近生理pH下的三维构型和行为。快速的虚拟筛选步骤对每个候选物在糖氧化酶‑I活性位点的适合度进行评分。团队随后应用关于分子大小、溶解性及其他药物相似性属性的简单规则,剔除那些在体内不太可能起作用的分子。更详细的对接程序则检查最有前景分子如何在酶内取向,特别是它们如何接触并抓取位于糖氧化酶‑I化学反应核心的锌金属原子。
一种抓住酶金属核心的新方式
早期阻断糖氧化酶‑I的努力集中在众所周知的化学基团上,如羧酸和羟肟酸,这些基团善于配位金属,但常常存在稳定性差或不良副作用的问题。本研究则发现了一类不同的“抓金属”单元:羟基三唑环。在16种被列为高位并购买进行实验测试的分子中,带有该环的化合物——代号SPB07393SC——脱颖而出。在虚拟对接中,其羟基三唑基团伸向锌原子,而两个芳香环则嵌入酶的疏油口袋。对该复合体进行数十纳秒的计算机模拟表明,该分子保持紧密结合,距离稳定,蛋白整体保持紧致,并维持持久的氢键网络。
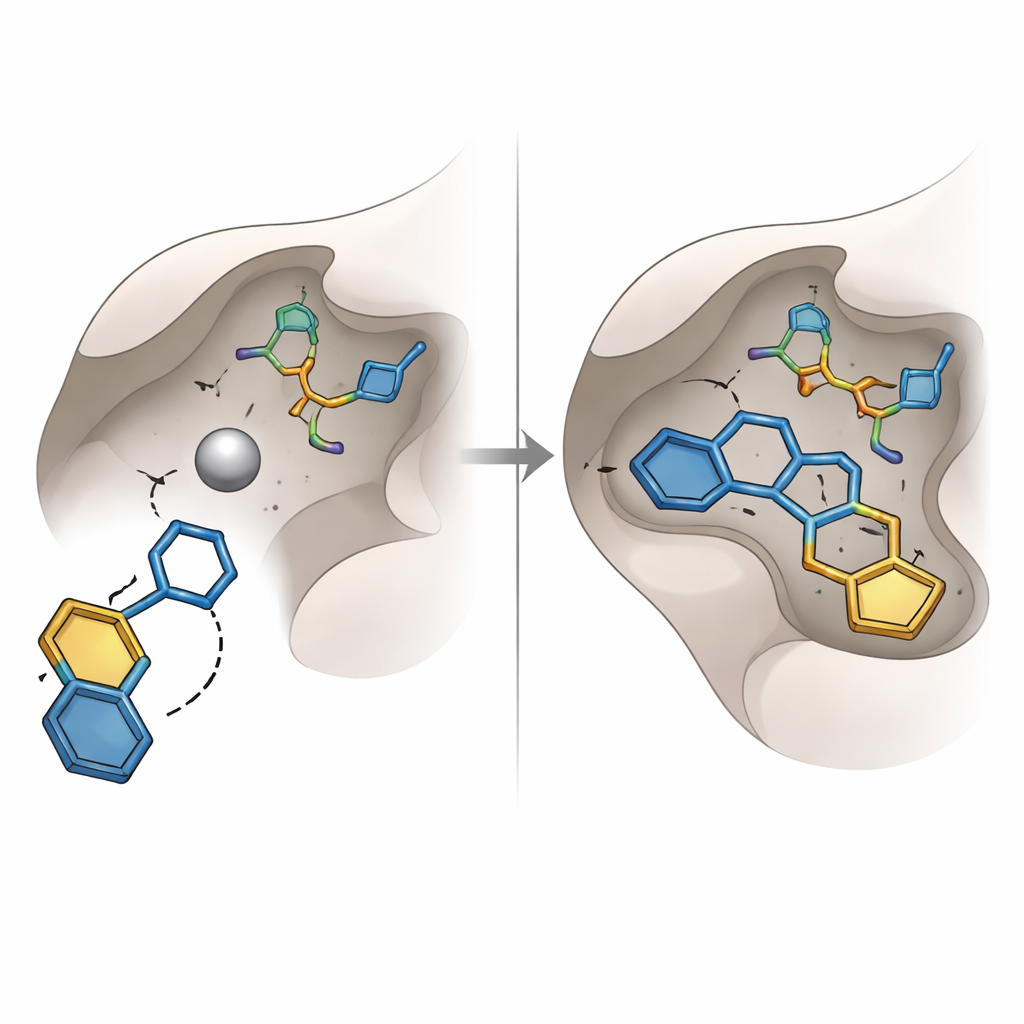
将预测付诸检验
为验证计算模型是否转化为真实世界的效应,团队在板式测定中测量了所选分子对纯化人源糖氧化酶‑I活性的抑制效果。16个候选物中有15个在测试条件下仅显示出弱或可忽略的抑制,突显了仅依靠静态对接评分的局限性。相比之下,SPB07393SC对该酶表现出强抑制作用,IC中等微摩尔级的效力使其成为一个稳健的早期“命中”而非终成药物。附加的软件预测该分子应具备可接受的溶解性、良好的吸收、在必要时到达大脑的能力以及较低的某些遗传毒性或肝毒性风险,但这些安全性预测仍需实验确认。
这对未来抗癌药物意味着什么
这项工作将羟基三唑引入作为将药物候选物锚定到糖氧化酶‑I核心锌原子的一种新方式,扩展了药物设计者可用的化学策略清单。尽管SPB07393SC本身仅是一个起点,但其酶抑制能力、预测的类药性行为及在动力学模拟中显示的稳定结合,使其成为值得进一步精细化修饰的有前途骨架。更广泛地说,该研究既展示了计算引导筛选的优势——能迅速将庞大的化学库缩小到少数现实的竞争者——也表明了其局限性:仍需谨慎的实验验证来揭示哪些分子确实能使癌细胞赖以处理毒性废物的酶失活。
引用: Al-Qazzan, M., Al-Balas, Q., Alnajjar, B. et al. Discovery of hydroxytriazole as a potential glyoxalase-I inhibitor utilizing computer-aided drug design techniques. Sci Rep 16, 9945 (2026). https://doi.org/10.1038/s41598-026-40497-4
关键词: 糖氧化酶 I, 癌症代谢, 计算机辅助药物设计, 配位锌的抑制剂, 分子对接