Clear Sky Science · zh
MEOX1–PAX1轴协调调控胶质母细胞瘤肿瘤细胞恶性表型和调节性T细胞分化
这项脑癌研究为何重要
胶质母细胞瘤是最致命的脑癌之一,部分原因在于肿瘤既能迅速生长,又能隐匿于机体防御之外。本研究揭示了肿瘤细胞内的一条分子“指挥链”,它不仅助长了肿瘤的侵袭性行为,还教会邻近的免疫细胞退守。解码这条链条后,研究提出了一种同时攻击癌细胞及其免疫屏障的潜在策略。
一种解除防御能力的致命肿瘤
胶质母细胞瘤以手术、放疗和化疗后易复发著称。其一原因是肿瘤的“敌对”周边环境,即肿瘤微环境。该环境并非充满抗癌细胞,反而常含有实际保护肿瘤的免疫细胞。其中最重要的是调节性T细胞(Tregs),这类白细胞在正常情况下可防止过度炎症。但在胶质母细胞瘤中,Tregs在肿瘤周围积聚,帮助肿瘤躲避免疫攻击。
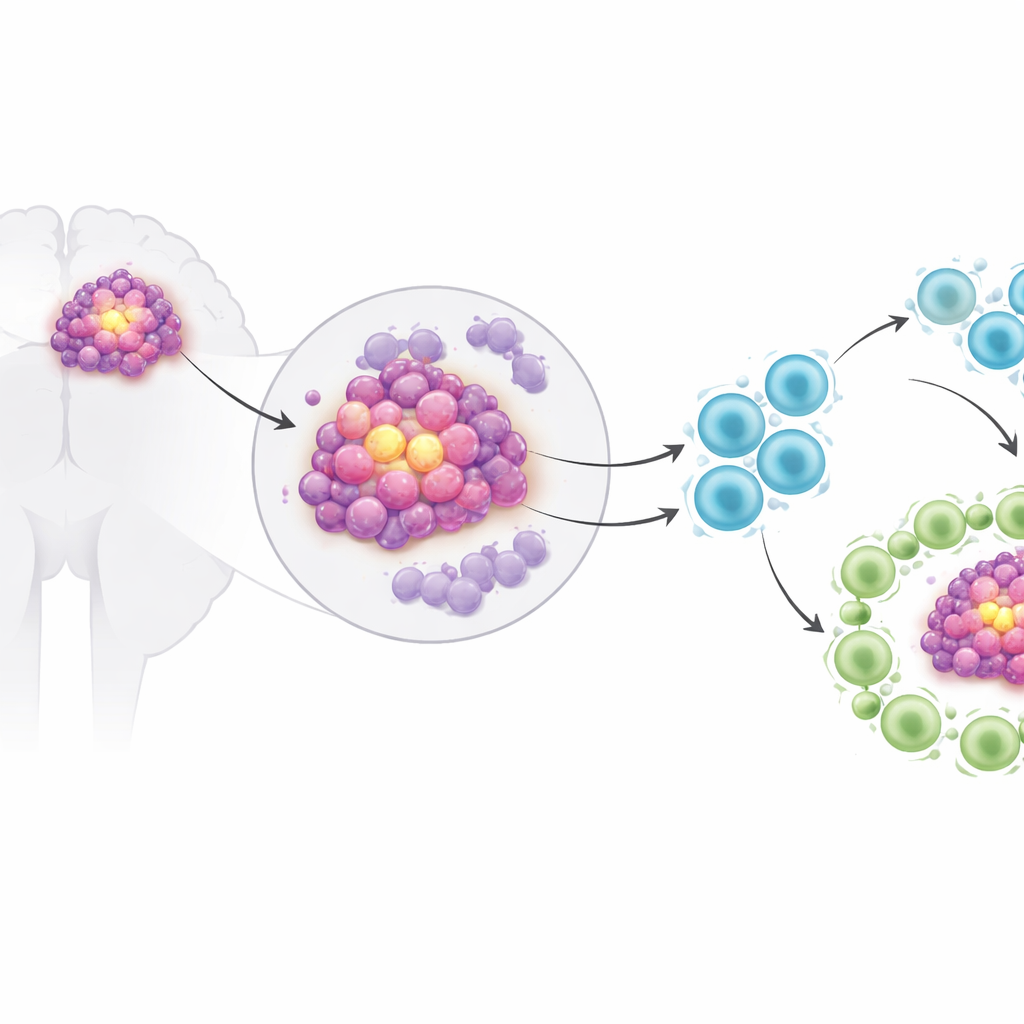
肿瘤细胞内的两个关键开关
研究者聚焦于两种在细胞内起基因开关作用的蛋白:MEOX1和PAX1。先前工作将MEOX1与癌症生长联系起来,并提示其可能影响免疫细胞;而PAX1更常被认为是抑制肿瘤、控制细胞生长的抑癌因子。在体外培养的胶质母细胞瘤细胞中,研究团队发现上调MEOX1会使肿瘤细胞分裂更快、迁移更强并更易穿透屏障,同时降低细胞凋亡倾向。下调MEOX1则产生相反效果,减慢生长并增加细胞死亡。他们进一步证明,MEOX1通过抑制PAX1来发挥这些作用;当恢复PAX1水平时,MEOX1造成的有害效应大多消失。
从肿瘤开关到免疫重塑
研究不仅考察了肿瘤生长,还探讨了这一区内调控如何影响免疫细胞。科学家将人类胶质母细胞瘤细胞与纯化的CD4 T细胞共培养,CD4 T细胞可分化为具有攻击性的辅助T细胞或具有抑制性的Tregs。他们发现,当肿瘤细胞中的PAX1降低时,更多的邻近T细胞转变为Tregs;而增加PAX1则减少了呈抑制性表型的T细胞数量。来自一例胶质母细胞瘤患者的组织样本显示,肿瘤区域的Tregs数量高于邻近非肿瘤脑组织,与体外结果一致。这些结果表明,肿瘤细胞内的PAX1水平是将局部免疫细胞倾向于肿瘤保护性角色的关键因素。
单一轴线,肿瘤的双重优势
综合数据支持这样的模型:胶质母细胞瘤细胞中高表达的MEOX1降低了PAX1,从而给予肿瘤双重优势。在癌细胞内部,这一变化促进了生长、迁移并增强抗凋亡能力;在细胞外部,它有助于将普通T细胞转化为在肿瘤周围定居并抑制免疫攻击的Tregs。由此,MEOX1–PAX1轴将肿瘤侵袭性的内在驱动与免疫抑制的外在屏障连接起来,形成一个紧密相联、有利于肿瘤生存的系统。
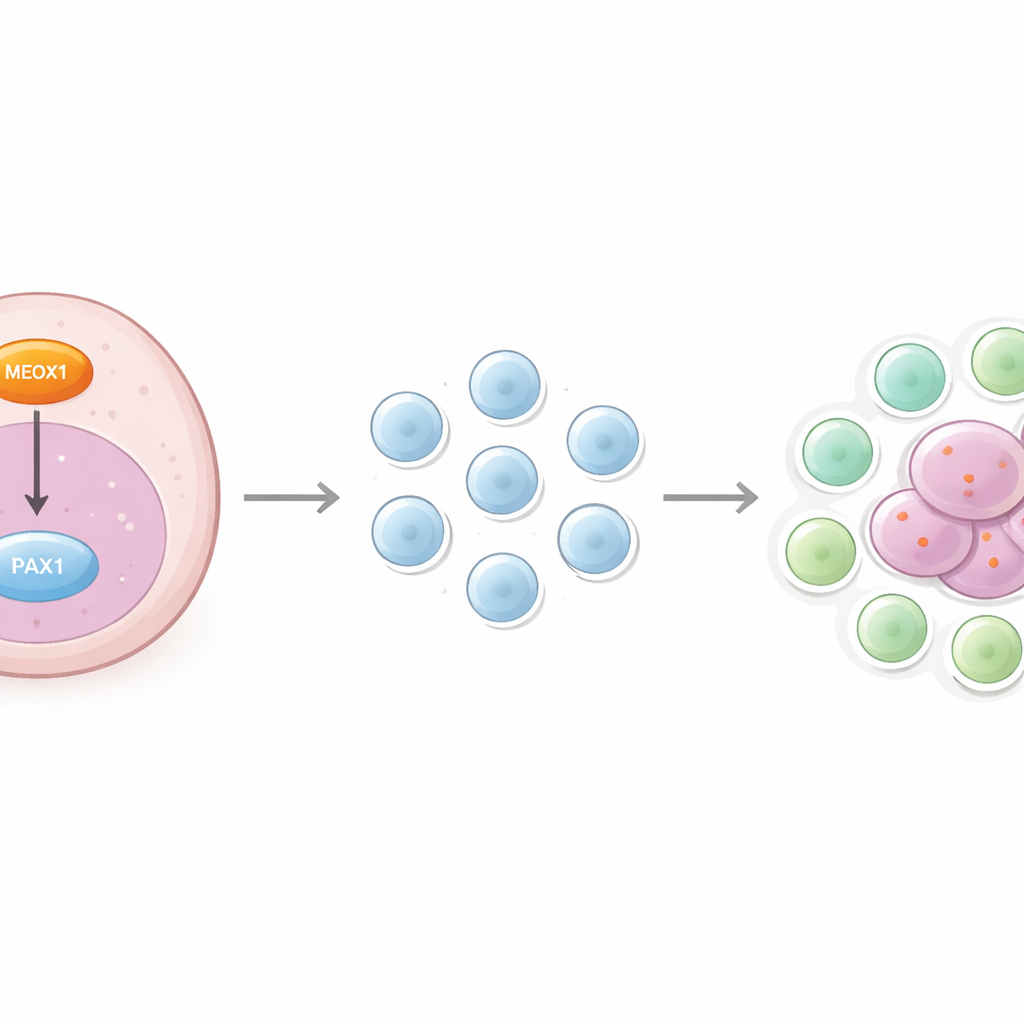
这对未来治疗可能意味着什么
对于面临胶质母细胞瘤的患者,这些发现强调了一个有前景的治疗思路:靶向MEOX1–PAX1轴以同时打击肿瘤及其免疫屏障。抑制MEOX1或恢复PAX1活性的药物可能在减缓肿瘤生长的同时,降低肿瘤微环境中Tregs的数量,从而可能提升现有治疗手段(包括免疫疗法)的效果。尽管这些结果来自细胞和组织实验,尚需在活体模型中验证,但它们提供了更清晰的地图,说明胶质母细胞瘤如何智胜免疫系统——并指向了把优势重新转回患者一方的新方法。
引用: Pan, P., Wang, R., Lv, P. et al. The MEOX1-PAX1 axis coordinately regulates tumor cell malignancy and Treg differentiation in glioblastoma. Sci Rep 16, 9136 (2026). https://doi.org/10.1038/s41598-026-40453-2
关键词: 胶质母细胞瘤, 肿瘤微环境, 调节性T细胞, 肿瘤免疫抑制, 癌症信号通路